
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 11.10.2024 Штучний інтелект у фармації: перспективи, переваги та потенційні ризики
- Новини 27.08.2024 Вакансії медсестри у Вінниці: особливості та вимоги до кандидатів
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
Влияние препаратов для лечения ожирения на факторы кардиоваскулярного риска: систематический обзор и метаанализ рандомизированных контролируемых клинических исследований
Резюме. Предпосылки исследования. Несмотря на широкое применение препаратов для лечения ожирения с целью профилактики его осложнений, их влияние на факторы кардиоваскулярного риска остается неясным до настоящего времени. Мы провели всесторонний систематический обзор и метаа- нализ с целью оценки влияния препаратов для лечения ожирения на факторы кардиоваскулярного риска.
Методы исследования и основные полученные данные. Мы произвели систематический поиск соответствующей литературы по базам Medline, EmBase, Cochrane Central Register of Controlled Trials, спискам литературы статей и материалам конференций. В обзор были включены рандомизированные плацебо-контролируемые исследования по изучению воздействия препаратов для лечения ожирения на факторы кардиоваскулярного риска в сравнении с плацебо. В целом при приеме орлистата снижение массы тела составило 2,39 кг (95% ДИ: от –3,34 до –1,45), снижение уровня общего холестерина — 0,27 ммоль/л (95% ДИ: от –0,36 до –0,17), снижение уровня ЛПНП — 0,21 ммоль/л (95% ДИ: от –0,30 до –0,12), снижение уровня глюкозы натощак — 0,12 ммоль/л (95% ДИ: от –0,20 до –0,04), снижение величины САД — 1,85 мм рт.ст. (95% ДИ: от –3,30 до –0,40), снижение величины ДАД — 1,49 мм рт.ст. (95% ДИ: от –2,39 до –2,58). Сибутрамин статистически достоверно снижал лишь массу тела и уровень триглицеридов. Римонабант был ассоциирован со статистически достоверным снижением массы тела, величины САД и ДАД. Других статистически значимых различий между применением препаратов для лечения ожирения и плацебо выявлено не было.</p>
Заключение/значимость исследования. Согласно полученным данным, применение препаратов для лечения ожирения было связано со снижением массы тела независимо от вида применяемого препарата. Орлистат и римонабант могут снижать кардиоваскулярный риск. Тем не менее сибутрамин может иметь прямое влияние на факторы кардиоваскулярного риска.
Введение
Сердечно-сосудистые заболевания являются ведущей причиной ранней заболеваемости и смертности среди мужского и женского населения во всем мире [1–4]. Число пациентов с ожирением и избыточной массой тела быстро возрастает, что приводит к повышению распространенности серьезных кардиоваскулярных событий и других системных заболеваний и вызывает общественную озабоченность из-за потребности в значительных материальных затратах как со стороны общества, так и со стороны родственников пациентов [5–7]. В течение нескольких последних десятилетий отдельные рандомизированные контролируемые клинические исследования уже показали снижение риска кардиоваскулярных исходов и других системных заболеваний при снижении массы тела. В практической деятельности врача первым этапом в лечении ожирения является модификация образа жизни. Тем не менее модификация образа жизни имеет свои ограничения при необходимости в длительном снижении массы тела, особенно при лечении подросткового ожирения. Фактически более 80 % приверженных к лечению пациентов не способны достичь снижения массы тела при модификации пищевого поведения и образа жизни. Модификация образа жизни не оказывала достаточного влияния на снижение массы тела, что заставило исследователей обратить внимание на эффективные дополнительные методы профилактического лечения [7–12]. Одним из таких видов лечения является применение препаратов для лечения ожирения, влияние которых на снижение массы тела очевидно. Тем не менее остается неясным влияние препаратов для лечения ожирения на факторы кардиоваскулярного риска [7, 13]. Предыдущий обзор [14] предоставил доказательства влияния препаратов для лечения ожирения на снижение массы тела у подростков с ожирением, однако не привел достоверных доказательств влияния препаратов для лечения ожирения на факторы кардиоваскулярного риска.
В недавнее время были проведены несколько рандомизированных контролируемых клинических исследований [15, 16] по изучению препаратов для лечения ожирения. Данные вышеупомянутых исследований нуждаются в оценке для формулирования определенного вывода об эффективности применения препаратов для лечения ожирения. По этой причине мы провели систематический обзор и метаанализ всех имеющихся данных рандомизированных контролируемых клинических исследований, включая последние данные о связи между медикаментозными средствами для похудения, факторами кардиоваскулярного риска и любыми возможными побочными реакциями.
Методы исследования
Источники данных, стратегия поиска и критерии включения
Критериям включения в наш метаанализ соответствовали англоязычные рандомизированные контролируемые клинические исследования и обзоры литературы по применению препаратов для лечения ожирения независимо от состояния публикации (опубликовано, не опубликовано, в прессе, в процессе выполнения). Поиск соответствующей литературы осуществлялся с помощью следующих действий:
- Электронный поиск. Поиск с использованием ключевых слов «римонабант», «сибутрамин», «орлистат», «ожирение» и «рандомизированное контролируемое клиническое исследование» производился по электронным базам данных EmBase, Medline и Кокрановскому центральному регистру контролируемых исследований для статей, датированных не ранее 20.09.2010. Все списки литературы из отчетов о нерандомизированных контролируемых клинических исследованиях были обработаны вручную с целью поиска статей, соответствующих критериямв ключения.
- Другие источники. Мы связались с авторами для получения любой возможной дополнительной опубликованной либо неопубликованной информации и произвели поиск по протоколам ежегодных собраний Специализированного реестра Кокрановской группы по ожирению (Cochrane Obesity Group Specialized Register). В дополнение в мета-Реестре контролируемых клинических исследований (metaRegister of Controlled Trials) мы произвели поиск продолжающихся рандомизированных контролируемых клинических исследований, которые были зарегистрированы как завершенные, но на тот момент не были опубликованы. Подходящие для наших целей исследования отбирались по медицинским предметным рубрикам, описанию методов, популяции пациентов и виду вмешательства. Проведение данного обзора и отчет по нему были выполнены согласно требованиям PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analysis) 2009 года (Контрольный список S1) [17].
Поиск по литературным источникам, сбор данных и оценка их качества производились по стандартизированной схеме двумя авторами (Xiu-Qiang Ma и Jian Lu) независимо. При наличии любого рода разногласий между этими двумя авторами для формирования единого мнения привлекался третий автор (Yu-Hao Zhou).
В нашу работу были включены все завершенные рандомизированные плацебо-контролируемые клинические исследования, оценивающие влияние препаратов для лечения ожирения и содержащие данные о как минимум одном исходе, связанном с факторами кардиоваскулярного риска.
Поиск по литературным источникам, сбор данных и оценка их качества производились по стандартизированной схеме двумя авторами (Xiu-Qiang Ma и Jian Lu) независимо. При наличии любого рода разногласий между этими двумя авторами для формирования единого мнения привлекался третий автор (Yu-Hao Zhou).
В нашу работу были включены все завершенные рандомизированные плацебо-контролируемые клинические исследования, оценивающие влияние препаратов для лечения ожирения и содержащие данные о как минимум одном исходе, связанном с факторами кардиоваскулярного риска.
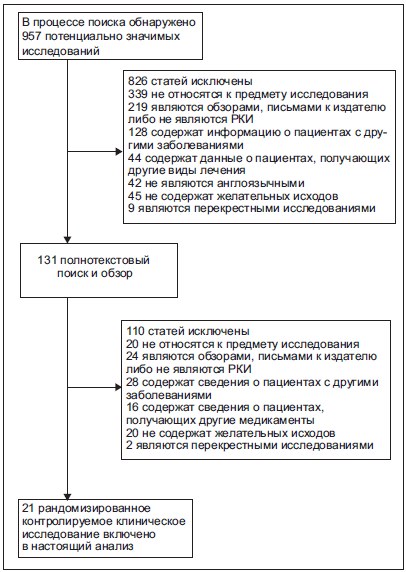
Рисунок 1. Блок-схема, отображающая процесс поиска в литературных источниках и включения исследований в анализ
Сбор и оценка данных
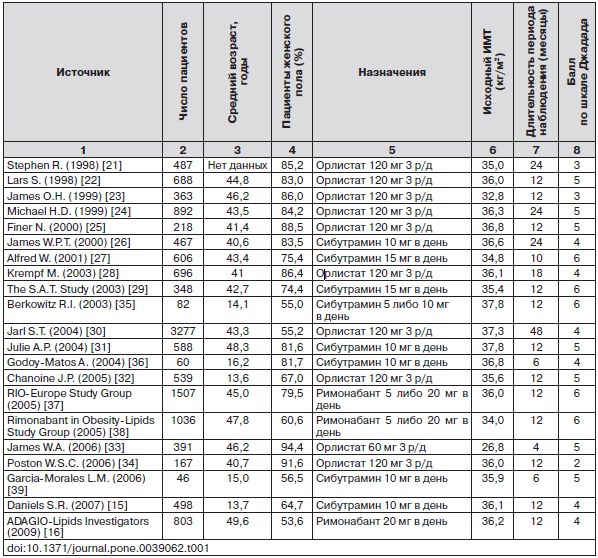
Одним из авторов (Yu-Hao Zhou) была разработана стандартная процедура сбора данных, после чего три других автора (Cheng Wu, Jia Guo, Xiao-Fei Ye) проверили все исследования на соответствие критериям включения, а также по стандартизированному алгоритму собрали и представили в виде таблиц все необходимые данные. Собранные данные содержали сведения об исходных характеристиках пациента, виде и дозе препарата для лечения ожирения, длительности периода наблюдения, изменениях в весе, факторах кардиоваскулярного риска, а также любых возможных побочных исходах. Разногласия касательно сбора данных разрешались путем общего обсуждения. Качество исследования оценивалось по шкале Джадада (Jadad scores) [18] (Jin-Fang Xu, Yu-Hao Zhou), которая учитывает сведения о рандомизации исследования, неразглашении данных о распределении пациентов по группам лечения либо плацебо, маскировании данных, завершенности периода наблюдения и применении ITT-анализа.
Таблица 1. Дизайн и характеристика исследований, включенных в систематический обзор и метаанализ
Статистический анализ
Величины относительного риска (ОР) и средней разницы (СР) с 95% доверительным интервалом (ДИ) были рассчитаны по исходам исследований до группировки данных. Мы использовали ОР с 95% ДИ для бинарных данных с целью оценки влияния препаратов для лечения ожирения на развитие нежелательных явлений и СР с 95% ДИ для непрерывных данных с целью оценки влияния препаратов для лечения ожирения на снижение веса и факторы кардиоваскулярного риска, такие как уровень общего холестерина, уровень ЛПНП, уровень ЛПВП, уровень триглицеридов, уровень глюкозы натощак, величину САД и ДАД. С целью изучения возможной гетерогенности в ожидаемых результатах лечения мы выполнили одномерный метарегрессионный анализ по подгруппам и сравнили общие результаты данного анализа, учитывавшего вид препарата для лечения ожирения, средний возраст пациентов, длительность периода наблюдения и качество исследования. Для всех ожидаемых эффектов препаратов мы использовали модель со случайными уровнями факторов [19] и статистическую обработку по методу Мантела — Ханзела (Mantel-Haenszel Statistics). Гетерогенность результатов лечения в различных исследованиях была оценена визуально по воронкообразному графику и статистически с помощью I2-статистики. Значения I2 в пределах 0–40 % указывают на незначительную гетерогенность, 30–60 % — умеренную гетерогенность, 50–90 % — существенную гетерогенность и 75–100 % — довольно высокую, значимую гетерогенность [20]. Все значения P были получены при расчете двустороннего теста, значения p, не превышающие 0,05, считались значимыми для всех включенных исследований. Все виды анализов выполнялись при помощи Stata (версия 10.0).
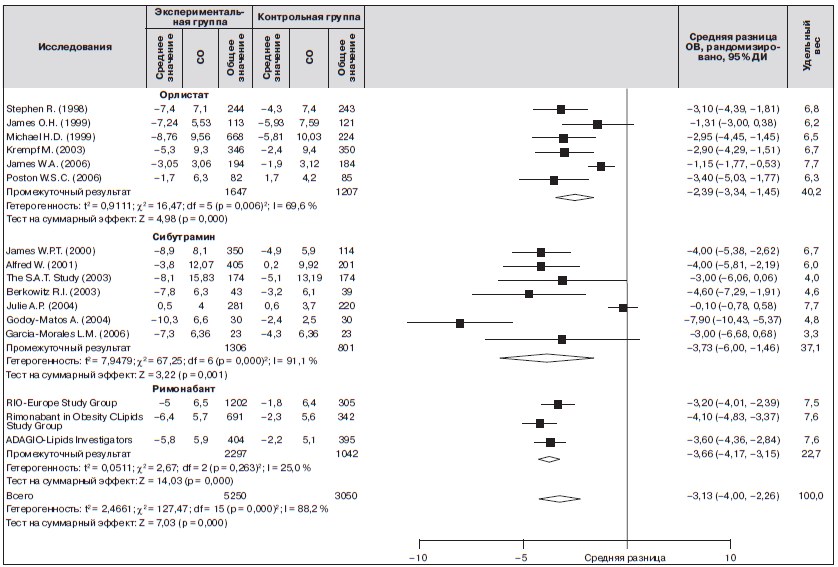
Рисунок 2. Средняя величина снижения массы тела (кг) при применении сибутрамина и орлистата: ДИ — доверительный интервал; ОВ — обратная вариация; СО — стандартное отклонение
Результаты
В ходе первичного электронного поиска мы отобрали 957 потенциально важных статей, в дальнейшем 826 из них были исключены после предварительного просмотра. Оставшееся 131 исследование было подвергнуто детальной оценке, после чего было отобрано 21 рандомизированное клиническое исследование [15, 16, 21–39], соответствующее нашим критериям включения (рис. 1 и протокол S1). Данное 21 исследование содержало информацию о 13 759 пациентах с ожирением (среднее число пациентов: 655, диапазон: от 46 до 3277 пациентов). В табл. 1 сведены основные характеристики включенных исследований и их участников. Период наблюдения составил от 4 до 48 месяцев, 14,7 месяца в среднем. 10 из числа включенных исследований изучали применение орлистата [21–25, 28, 30, 32–34], 3 [16, 37, 38] — применение римонабанта и оставшиеся 8 [15, 26, 27, 29, 31, 35, 36, 39] — применение сибутрамина. Поскольку не все включенные исследования содержали данные о ключевых индикаторах качества исследований, мы оценили его с использованием предварительно заданных критериев шкалы Джадада. В целом пять исследований набрали 6 баллов, семь — 5 баллов, шесть — 4 балла, два — 3 балла и оставшееся одно исследование — 2 балла.
Данные о влиянии препаратов для лечения ожирения на снижение массы тела в сравнении с плацебо были доступны в 16 исследованиях (рис. 2). В целом следует отметить, что применение препаратов для лечения ожирения приводило к достоверному снижению массы тела на 3,13 кг (95% ДИ: от –4,00 до –2,26) в сравнении с плацебо. Более того, орлистат, сибутрамин и римонабант обеспечивали снижение массы тела на 2,39 кг (95% ДИ: от –3,34 до –1,45), 3,73 кг (95% ДИ: от –6,00 до –1,46) и 3,66 кг (95% ДИ: от –4,17 до –3,15) соответственно.
Данные о влиянии препаратов для лечения ожирения на факторы кардиоваскулярного риска были разделены на семь групп, например, уровень общего холестерина, уровень ЛПНП, уровень ЛПВП, уровень триглицеридов, уровень глюкозы натощак, величины САД и ДАД (рис. 3). В целом применение орлистата обеспечивало снижение уровня общего холестерина на 0,27 ммоль/л (95% ДИ: от –0,36 до –0,17), уровня ЛПНП — на 0,21 ммоль/л (95% ДИ: от –0,30 до –0,12), уровня глюкозы натощак — на 0,12 ммоль/л (95% ДИ: от –0,20 до –0,04), величины САД — на 1,85 мм рт.ст. (95% ДИ: от –3,30 до –0,40) и величины ДАД — на 1,49 мм рт.ст. (95% ДИ: от –2,39 до –0,58). Более того, сибутрамин статистически достоверно оказывал влияние на снижение массы тела (СР = –3,73 кг, 95% ДИ: от –6,00 до –1,46) и снижение уровня триглицеридов (СР = –0,13 ммоль/л, 95% ДИ: от –0,26 до –0,00). Римонабант оказывал выраженное влияние на снижение массы тела (СР = –3,66 кг, 95% ДИ: от –4,17 до –3,15), снижение величины САД (СР = –1,63 мм рт.ст., 95% ДИ: от –2,76 до –0,51) и ДАД (СР = –1,60 мм рт.ст., 95% ДИ: от –2,8 до –0,39).
Также было отмечено, что в некоторых исследованиях имеются сообщения о нежелательных явлениях, в 12 исследованиях имеются данные об общем числе нежелательных явлений. В целом применение препаратов для лечения ожирения повышало риск медикаментозно обусловленных нежелательных явлений на 8 % в сравнении с плацебо (ОР: 1,08, 95% ДИ: от 1,02 до 1,14, рис. 4). Аналогичным образом применение препаратов для лечения ожирения повышало риск развития заболеваний желудочно-кишечного тракта на 73 % (ОР: 1,73, 95% ДИ: от 1,40 до 2,15), риск развития артериальной гипертензии — на 86 % (ОР: 1,86, 95% ДИ: от 1,28 до 2,71), риск развития тахикардии — на 195 % (ОР: 2,95, 95% ДИ: от 1,56 до 5,58) и риск возникновения сухости во рту — на 371 % (ОР: 4,71, 95% ДИ: от 1,63 до 13,65). Применение препаратов для лечения ожирения не было связано с развитием инфекционных заболеваний и паразитарных инвазий, появлением головной боли, сыпи, боли в животе, инфекциями верхних дыхательных путей, простудными заболеваниями и фарингитом.
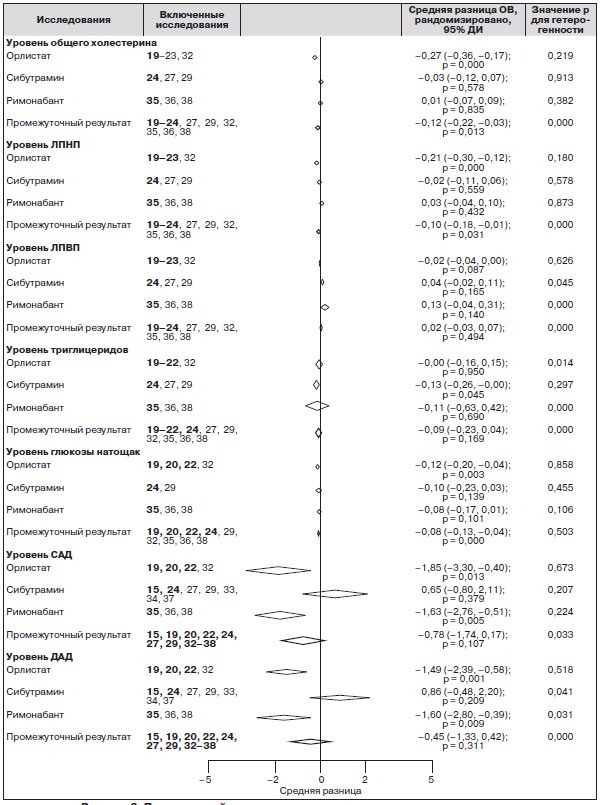
Рисунок 3. Подгрупповой анализ влияния препаратов для лечения ожирения на факторы кардиоваскулярного риска в зависимости от вида применяемого препарата
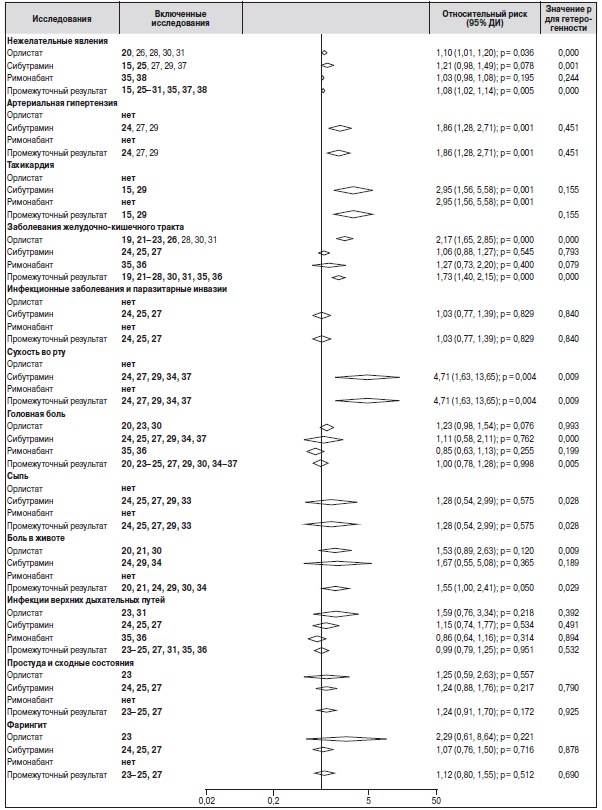
Рисунок 4. Обобщение данных по относительным рискам всех нежелательных явлений
В большинстве включенных исследований результаты по снижению массы тела, а также уровней ЛПВП и триглицеридов имели признаки гетерогенности. Несмотря на это, мы провели последовательное исключение каждого исследования из совокупного анализа таким образом, чтобы данные исключения не повлияли на наши результаты. Следовательно, мы провели подгрупповой анализ, чтобы свести к минимуму последствия гетерогенности включенных исследований по среднему возрасту, длительности периода наблюдения и качеству исследования (табл. 2). Анализ в подгруппах был проведен по таким признакам, как снижение массы тела, а также снижение уровней ЛПВП и триглицеридов. Полученные данные продемонстрировали присутствие признаков гетерогенности в результатах большинства включенных исследований.
Также уменьшению гетерогенности способствовало проведение подгруппового анализа по виду применяемых препаратов для лечения ожирения. Тем не менее в некоторых подгруппах был достигнут однозначный результат, что может говорить о включении небольшого количества исследований в эти подгруппы.
Обсуждение
Ожирение остается наиболее частой причиной возникновения сердечно-сосудистых заболеваний, инсульта, сахарного диабета второго типа и других системных заболеваний [40]. Согласно данным некоторых исследований, ожирение уменьшает продолжительность жизни на 4,8–7,1 года у людей старше 40 лет и связано со значительным бременем социального обеспечения [41, 42]. Несмотря на то, что многие препараты для лечения ожирения в значительной мере влияют на снижение массы тела, некоторые исследования [15, 43] указывают на недостаточную изученность их влияния на факторы кардиоваскулярного риска.
Результаты настоящего метаанализа продемонстрировали значительное снижение массы тела, а также уровней общего холестерина, ЛПНП и глюкозы натощак при применении препаратов для лечения ожирения. В то же время повышался риск развития нежелательных явлений, тахикардии, заболеваний желудочно-кишечного тракта, артериальной гипертензии и появления сухости во рту.
Учитывая повышенный кардиоваскулярный риск у пациентов с сахарным диабетом, гиперлипидемией, гипергликемией и артериальной гипертензией [44, 45], мы ужесточили критерии включения в настоящее исследование с целью изучения влияния препаратов для лечения ожирения на факторы кардиоваскулярного риска без учета воздействия сопутствующей патологии.
Участники отдельных исследований, включенных в наш метаанализ, соответствовали нашим критериям включения. Пациенты с сердечно-сосудистыми заболеваниями либо другими факторами кардиоваскулярного риска исключались из анализа. Более того, неконтролируемая гипертензия, снижение веса более чем на 4 кг за последние 3 месяца, оперативное вмешательство для снижения веса и послеоперационная спаечная болезнь в анамнезе, булимия либо злоупотребление слабительными средствами, прием любых препаратов, влияющих на массу тела либо уровень липидов плазмы, в течение месяца до включения в исследование, а также наркотическая и алкогольная зависимость являлись критериями исключения из настоящего анализа [15, 21–34].
В недавнее время некоторые рандомизированные контролируемые клинические исследования [41, 43, 46] продемонстрировали прямое влияние препаратов для лечения ожирения на снижение массы тела и факторы кардиоваскулярного риска у лиц с ожирением. Более того, в исследовании Daniels [15] было показано, что сибутрамин может оказывать прямое влияние на сердечно-сосудистую систему у подростков с ожирением. Согласно заключению того же исследования, данные о повышении кардиоваскулярного риска при приеме сибутрамина отсутствовали, что может объясняться непосредственным влиянием снижения массы тела на факторы кардиоваскулярного риска. Таким образом, мы ограничили исходные характеристики пациентов с ожирением этими двумя группами с целью изучения связи между приемом препаратов для лечения ожирения и факторами кардиоваскулярного риска.
Согласно данным предыдущих исследований [45, 47], препараты для лечения ожирения могут снижать массу тела, что, в свою очередь, способствует снижению кардиоваскулярного риска. Тем не менее прямое влияние препаратов для лечения ожирения на величину кардиоваскулярного риска остается недоказанным. Более того, ожирение обычно сопровождается рядом сопутствующих патологий, особенно у пациентов старших возрастных групп. Целью проведения нашего систематического обзора и метаанализа была оценка собственной корреляции между приемом препаратов для лечения ожирения и величиной кардиоваскулярного риска.
Предыдущий метаанализ [14] продемонстрировал лишь влияние препаратов для лечения ожирения на факторы кардиоваскулярного риска у подростков, причем корреляция между приемом препаратов и величиной кардиоваскулярного риска была слабой. Настоящий метаанализ показывает, что применение препаратов для лечения ожирения может снижать кардиоваскулярный риск по таким факторам, как уровень общего холестерина, ЛПНП и глюкозы натощак, однако не влияет на уровень триглицеридов, величину САД и ДАД.
Орлистат может играть важную роль в снижении величин САД и ДАД, уровня общего холестерина, ЛПНП и глюкозы натощак. Несмотря на сообщения о снижении кардиоваскулярного риска по некоторым факторам, орлистат оказывает слабое влияние на его величину. Причиной данного существенного различия может служить снижение массы тела. Преимущество орлистата перед сибутрамином может объясняться принадлежностью первого к классу препаратов для лечения ожирения, которые имеют прямое и специфическое действие на расщепление жиров в просвете желудка и тонкой кишки. По этой же причине орлистат оказывает слабое влияние на факторы кардиоваскулярного риска [22].
Прием сибутрамина способствовал повышению кардиоваскулярного риска, что объясняется его гипертензивным действием. На фоне повышения артериального давления возрастает риск развития кардиоваскулярных событий, особенно у людей с высоким риском и сердечно-сосудистыми заболеваниями в анамнезе [7]. Наше исследование продемонстрировало, что гипертензия, как медикаментозно обусловленное побочное явление, чаще встречалась в группе приема сибутрамина в сравнении с плацебо. Данное побочное явление имеет прямое влияние на факторы кардиоваскулярного риска и способствует более частому развитию значимых сердечно-сосудистых событий.
Новый препарат для лечения ожирения римонабант в значительной мере снижает массу тела. Более того, он обладает способностью эффективно снижать величины САД и ДАД. В предыдущем исследовании [38] было продемонстрировано, что применение римонабанта приводило к значительному уменьшению жировых отложений в области живота и, соответственно, снижению кардиоваскулярного риска. Изолированное применение римонабанта не устранит существующую эпидемию ожирения, однако, согласно данным нашего исследования, может существенно снизить массу тела и величину кардиоваскулярного риска.
Применение препаратов для лечения ожирения не влияло на уровень ЛПВП и триглицеридов, что может объясняться модификацией их действия под влиянием других препаратов для лечения ожирения. При применении римонабанта может наблюдаться значительное повышение уровня ЛПВП, причиной этого может служить ограниченное число исследований, содержащих соответствующие данные. Применение орлистата либо сибутрамина не оказывало прямого воздействия на уровень ЛПВП либо триглицеридов.
Наше исследование имеет следующие ограничения:
- Выводы любого метаанализа основываются на объединенных данных, как опубликованных, так и освещенных в отдельных авторских исследованиях. Информация о пациентах и исходные сведения были для нас недоступны, что препятствовало проведению более подробного анализа и формулированию более четких выводов.
- На наши выводы о связи препаратов для лечения ожирения с факторами кардиоваскулярного риска могли повлиять длительность периода наблюдения и дозировка лекарственного средства.
- Мы не обладали достаточной информацией для подробного изучения влияния препаратов для лечения ожирения на индекс массы тела, окружность талии и развитие побочных явлений.
- Пациенты с ожирением часто питаются согласно низкокалорийной диете с низким содержанием жира и ограничением углеводов, что также может влиять на кардиоваскулярные факторы риска.
Таким образом, в будущих исследованиях важно обратить внимание на пациентов с факторами кардиоваскулярного риска с целью проведения первичной профилактики сердечно-сосудистых заболеваний, а также комбинировать различные препараты для лечения ожирения с целью создания оптимальной схемы лечения, сводящей к минимуму побочные явления у пациентов с ожирением. Мы предлагаем следующие пути оптимизации продолжающихся на настоящий момент исследований:
- В будущих исследованиях следует создать стандартную форму для фиксации и отчета о развитии побочных эффектов в рамках клинического испытания, чтобы сделать возможной оценку побочных эффектов всех медикаментов.
- С целью выбора наилучшего препарата для лечения ожирения, его дозировки и длительности применения, следует более подробно изучить различные медикаменты, их дозировки и сроки применения [48].
- В будущих исследованиях следует более подробно фиксировать данные о снижении веса, индексе массы тела и окружности талии для предоставления более полной информации.
Список литературы
- Coutinho W.F. The obesity older female patient: CV risk and the SCOUT study // Int. J. Obes. 2007; 31: S26-S30.
- Hubert H.B., Feinleib M., McNamara P.M., Castelli W.P. Obesity as an independent risk factor for cardiovascular disease: a 26-year follow-up of participants in the Framingham Heart Study // Circulation 1983; 67: 968-77.
- Jousilahti P., Tuomilehto J., Vartiainen E., Pekkanen J., Puska P. Body weight, cardiovascular risk and coronary mortality: 15-year follow-up of middleaged men and women in Eastern Finland // Circulation 1996; 93: 1372-9.
- National Task Force on the Prevention and Treatment of Obesity. Overweight, obesity, and health risk // Arch. Intern. Med. 2000; 160: 898-904.
- Mokdad A.H., Bowman B.A., Ford E.S., Vinicor F., Marks J.S. et al. The continuing epidemics of diabetes and obesity in the United States // JAMA 2001; 286: 1195-1200.
- Allison D.B., Fontaine K.R., Manson J.E., Stevens J., VanItallie T.B. Annual deaths attributable to obesity in the United States // JAMA 1999; 282: 1530-1538.
- SCOUT Investigators. Effect of Sibutramine on cardiovascular outcomes in overweight and obese subjects // N. Engl. J. Med. 2010; 363: 905-17.
- OBES-002 Study Group. A randomized double-blind placebo-controlled study of the long-term efficacy and safety of topiramate in the treatment of obese subjects // Int. J. Obes. 2004; 28: 1399-1410.
- Goldstein D.J. Beneficial health effects of modest weight loss // Int. J. Obes. 1992; 16: 397-415.
- Wing R.R., Hill J.O. Successful weight loss maintenance // Annu. Rev. Nutr. 2001; 21: 323-41.
- Kramer F.M., Jeffery R.W., Forster J.L., Snell M.K. Longterm follow-up of behavioral treatment for obesity: patterns of weight regain among men and women // Int. J. Obes. 1989; 13: 123-136.
- Ayyad C., Andersen T. Long-term efficacy of dietary treatment of obesity: a systematic review of studies published between 1931 and 1999 // Obes. Rev. 2000; 1: 113-119.
- Poston W.S.C., Reeves R.S., Haddock C.K., Stormer S., Balasubramany et al. Weight loss in obese Mexican Americans treated for 1-year with orlistat and lifestyle modification // Int. J. Obes. 2003; 27: 1486-1493.
- Czernichow S., Lee C.M.Y., Barzi F., Greenfield J.R., Baur L.A. et al. Efficacy of weight loss drugs on obesity and cardiovascular risk factors in obese adolescents: a meta-analysis of randomized controlled trials // Obesity 2010; 11: 150-158.
- Daniels S.R., Barbara L., Scott C., Styne D., Sothem M. et al. Cardiovascular effects of Sibutramine in the treatment of obese adolescents: results of a randomized, double-blind, placebocontrolled study // Pediatrics 2007; 120: e147-e157.
- ADAGIO-Lipids Investigators. Effect of Rimonabant on the High-Triglyceride/Low HDL-Cholesterol Dyslipidemia, Intraabdominal Adiposity, and Liver Fat: The ADAGIO-Lipids Trial // Arterioscler. Thromb. Vasc. Biol. 2009; 29; 416-423.
- Moher D., Liberati A., Tetzlaff J., Altman D.G., Grp P. Preferred Reporting Items for Systematic Reviews and Meta-Analyses: The PRISMA Statement // Plos. Medicine 2009; 6.
- Jadad A.R., Moore R.A., Carroll D., Jenkinson C., Reynolds D.J. et al. Assessing the quality of reports of randomized clinical trials: is blinding necessary? // Control Clin. Trials 1996; 17: 1-12.
- Ades A.E., Lu G., Higgins J.P. The interpretation of random-effects metaanalysis in decision models // Med. Decis. Making 2005; 25: 646-54.
- Deeks J.J., Higgins J.P.T., Altman D.G. Analyzing data and undertaking meta-analyses // Higgins J., Green S., eds. Cochrane Handbook for Systematic Reviews of Interventions 5.0.1. Oxford, UK: The Cochrane Collaboration, 2008; chap 9.
- Stephan R., Lars S., Rudolf N., Meinders A.E., Noseda G. et al. Weight loss, weight maintenance, and improved cardiovascular risk factors after 2 years treatment with orlistat for obesity // Obes. Res. 1998; 8: 49-61.
- Lars S., Aila R., Teis A., Boldrin M., Golay A. et al. Randomised placebocontrolled trial of orlistat for weight loss and prevention of weight regain in obese patients // Lancet 1998; 352: 167-73.
- James O.H., Hauptman J., James W.A., Fujioka K., O'Neil P.M. et al. Orlistat, a lipase inhibitor, for weight maintenance after conventional dieting: a 1-y study // Am. J. Clin. Nutr. 1999; 69: 1108-16.
- Michael H.D., Hauptman J., DiGirolamo M., Foreyt J.P., Halsted C.H. et al. Weight control and risk factors reduction in obese subjects treated for 2 years with orlistat: a randomized controlled trial // JAMA 1999; 281 (3): 235-242.
- Finer N., James W.P.T., Kopelman P.G., Lean M.E., Williams G. One-year treatment of obesity: a randomized, double-blind, placebo-controlled, multicenter study of orlistat, a gastrointestinal lipase inhibitor // Int. J. Obes. 2000; 24: 306-313.
- James W.P.T., Astrup A., Finer N., Hilsted J., Kopelman P. et al. Effect of Sibutramine on weight maintenance after weight loss: a randomised trial // Lancet 2000; 356: 2119-25.
- Alfred W., Jutta K. Long-term weight loss with Sibutramine: a randomized controlled trial // JAMA 2001; 286 (11): 1331-1339.
- Krempf M., Louvet J.P., Allanic H., Miloradovich T., Joubert J.M. et al. Weight reduction and long-term maintenance after 18 months treatment with orlistat for obesity // Int. J. Obes. 2003; 27: 591-597.
- S.A.T. study Group. Weight reduction by Sibutramine in obese subjects in primary care medicine: the S.A.T. study // Exp.Clin. Endocrinol. Diabetes 2004; 112: 201-207.
- Jarl S.T., Boldrin M.N., Hauptman J., Sjostrom L. XENical in the prevention of Diabetes in Obese Subjects (XENDOS) study: a randomized study of orlistat as an adjunct to lifestyle changes for the prevention of type 2 diabetes in obese patients // Diabetes Care 2004; 27: 155-161.
- Julie A.P., Raebel M.A., Conner D.A., Lanty F.A., Vogel E.A. et al. The longterm outcomes of Sibutramine effectiveness on weight (LOSE Weight) study: Evaluation the role of drug therapy within a weight management program in a group-model health maintenance organization // Am. J. Manag. Care 2004; 10: 369-376.
- Chanoine J.P., Hampl S., Jensen C., Boldrin M., Hauptman J. Effect of orlistat on weight and body composition in obese adolescent: a randomized controlled trial // JAMA 2005; 293 (23): 2873-2883.
- James W.A., Schwartz S.M., Hauptman J., Boldrin M., Rossi M. et al. Lowdose orlistat effects on body weight of mildly to moderately overweight individuals: a 16 week, double-blind, placebo-controlled trial // Ann. Pharmacother. 2006; 40: 1717-23.
- Poston W.S.C., Haddock C.K., Pinkston M.M., Pace P., Reeves R.S. et al. Evaluation of a primary care-oriented brief counseling intervention for obesity with and without orlistat // J. Int. Med. 2006; 260: 388-398.
- Berkowitz R.I., Wadden T.A., Tershakovec A.M., Cronquist J.L. Behavior Therapy and Sibutramine for the Treatment of Adolescent Obesity. A Randomized Controlled Trial // JAMA 2003; 289: 1805-1812.
- Godoy-Matos A., Carraro L., Vieira A., Oliveira J., Guedes E.P. et al. Treatment of Obese Adolescents with Sibutramine: A Randomized, Double-Blind, Controlled Study // J. Clin. Endocrinol. Metab. 2004; 0263.
- RIO-Europe Study Group. Effects of the cannabinoid-1 receptor blocker rimonabant on weight reduction and cardiovascular risk factors in overweight patients: 1-year experience from the RIOEurope study // Lancet 2005; 365: 1389-97.
- Rimonabant in Obesity-Lipids Study Group. Effects of Rimonabant on Metabolic Risk Factors in Overweight Patients with Dyslipidemia // N. Engl. J. Med. 2005; 353: 2121-34.
- Garcia-Morales L.M., Berber A., Macias-Lara C.C., Lucio-Ortiz C., Del-Rio-Navarro B.E. et al. Use of Sibutramine in Obese Mexican Adolescents: A 6-Month, Randomized, Double-Blind, Placebo-Controlled, Parallel-Group Trial // Ciin. Ther. 2006; 28: 770-782.
- Goldstein D.J., Rampey A.H. Jr, Enas G.G., Potvin J.H., Fludzinski L.A. et al. Fluoxetine: a randomized clinical trial in the treatment of obesity // Int. J. Obes. 1994; 18: 129-135.
- UK Multimorbidity Study Group. Randomised trial of the effect of orlistat on body weight and cardiovascular disease risk profile in obese patients: UK Multimorbidity Study // Int. J. Clin. Pract. 2002; 56 (7): 494-499.
- Toplak H., Ziegler O., Keller U., Hamann A., Godin C. et al. X-PERT: weight reduction with orlistat in obese subjects receiving a mildly or moderately reduce-energy diet. Early response to treatment predicts weight maintenance // Diabetes, Obesity and Metabolism 2005; 7: 699-708.
- Simone G.D., Romano C., Caprio C.D., Contaldo F., Salanitri T. et al. Effects of Sibutramine-induced weight loss on cardiovascular system in obese subjects // Nutrition, Metabolism and Cardiovascular Diseases 2005; 15: 24-30.
- Doggrell S.A. Tesfensine-a novel potent weight loss medicine // Expert Opin. Investig. Drugs 2009; 18(7): 1043-1046.
- Swinburn B.A., Carey D., Hills A.P., Hooper M., Marks S. et al. Effect of orlistat on cardiovascular disease risk in obese adults // Diabetes, Obesity and Metabolism 2005; 7: 254-262.
- The Orlistat Swedish Multimorbidity Study Group. The effect of orlistat on body weight and coronary heart disease risk profile in obese patients: The Swedish Multimorbidity Study // J. Int. Med. 2000; 248: 245-254.
- Richelsem B., Tonstad S., Toubro S., Niskanen L., Madsbad S. et al. Effect of orlistat on weight regain and cardiovascular risk factors following a very-lowenergy diet in abdominally obese patients: a 3-year randomized, placebocontrolled study // Diabetes Care 2007; 30: 27-32.
- Joseph Y., Richard W.T., Goldfarb N. Obesity management interventions: a review of the evidence // Population Health Management 2009; 12: 305-316.

Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


