
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
- Новини 26.10.2021 Аппаратура для УЗИ: применение, принципы работы, разновидности
- Новини 23.10.2021 Интимная пластика после родов: когда необходима операция
Орлистат у пациентов с сахарным диабетом: улучшение гликемического контроля и снижение массы тела
Примерно 1/5 населения Великобритании страдает ожирением [1]. Рост распространенности ожирения во всех возрастных группах является мировой тенденцией [2, 3], которая расценивается как эпидемия [4] и является одной из основных угроз для здоровья общества, поскольку приводит к повышению заболеваемости и смертности от сердечнососудистых, цереброваскулярных и некоторых онкологических заболеваний [5—7].
Ожирение ассоциируется с инсулинорезистентностью [8]; полагают, что одной из причин этого является повышение уровня свободных жирных кислот [9]. Инсулинорезистентность является одним из факторов, предопределяющих развитие сахарного диабета (СД) типа 2, который сам по себе ассоциируется с развитием макро- и микроангиопатий [10]. Избыточная масса тела встречается более чем у 80% пациентов с СД типа 2 [11]. Существует прямая зависимость между повышением индекса массы тела (ИМТ) и риском развития СД [12]. При этом получается «порочный круг»: ожирение служит одной из причин СД, а инсулинотерапия может приводить к увеличению массы тела [13].
Даже умеренное снижение массы тела может обусловить значительное уменьшение риска сердечно-сосудистых событий [14]. Известно, что снижение массы тела приводит к улучшению гликемического контроля [15], что также сопряжено с уменьшением проявлений диабетических макро- и микроангиопатий [16]. Есть свидетельства того, что физическая активность и лечебные диеты способствуют снижению массы тела у пациентов с СД [17, 18].
Орлистат (Ксеникал, «Ф. Хоффманн-Ля Рош Лтд.», Швейцария) представляет собой ингибитор желудочно-кишечных липаз, используемый для лечения ожирения. Его эффект обусловлен снижением всасывания жиров из пищи в желудочно-кишечном тракте [19]. Клинические исследования показали, что применение Орлистата в сочетании с диетотерапией более эффективно, чем диетотерапия и плацебо [20, 21]. Этот эффект отмечался и у пациентов с СД типа 2 [22—25], и у пациентов с нарушенной глюкозотолерантностью, у которых был снижен риск развития СД типа 2 [26].
Дополнительно было показано, что у пациентов с СД типа 2 терапия Орлистатом приводит к снижению факторов сердечно-сосудистого риска: снижается уровень холестерина в сыворотке крови и систолическое АД (САД) [22, 25]. Было также показано, что при терапии Орлистатом уровень глюкозы в крови снижался в большей степени и контролировался лучше, чем при эквивалентной потере массы тела при диетотерапии и при выполнении физических упражнений [27]. Такое улучшение гликемического контроля также приводит к уменьшению потребности в инсулинотерапии [25].
В ходе исследования оценены эффективность применения Орлистата при СД и затраты на лечение пациентов, получавших Орлистат в течение первых 6 мес терапии в рамках реальной клинической практики. Кроме того, определяли взаимосвязь между улучшением гликемического контроля и изменением массы тела обследованных.
МЕТОДЫ
В проведенном проспективном клиническом исследовании проанализирован клинический опыт, накопленный в Wythen-shawe Hospital, Manchester, UK в период с мая 2000 г. по май 2003 г. Для участия в исследовании отбирали пациентов с избыточной массой тела (ИМТ>28 кг/м2) и СД, которым было показано лечение Орлистатом [28]. Эти пациенты получали терапию Орлистатом в специализированной клинике по лечению ожирения. Обязательным этапом терапии были также коррекция пищевого поведения и повышение физической активности. Желание достичь успеха определялось способностью пациентов добиться снижения массы тела на 2,5 кг за 4-недельный период до начала приема Орлистата [29]. К исследованию допускались все пациенты, прошедшие собеседование у диетолога, отвечающие рекомендациям NICE (National Institute for Clinical Excellence) по Орлистату, готовые определять уровень глюкозы в амбулаторных условиях и ежемесячно посещать клинику по лечению ожирения.
Пациенты посещали цикл групповых образовательных занятий, предлагаемых диетологом, на которых их обучали, как оценивать содержание жира в пище, и давали советы по снижению потребления жира до 50 г/сут. Пациенты заполняли дневник питания в течение 1 нед перед каждым посещением клиники. Им рекомендовалось регулярно выполнять физические упражнения по 30 мин 5 раз в неделю.
До начала исследования у пациентов определяли массу тела, рост, уровень HbA1c, тип СД и собирали следующие данные: возраст, пол и сопутствующая терапия. Повторно показатели определяли через 3, 6, 12 и 24 мес терапии. Дозы инсулина и пероральных сахароснижающих препаратов уменьшали в случае повторного снижения уровня глюкозы в крови <4 ммоль/л при амбулаторном контроле или при возникновении клинической гипогликемии; дозы инсулина корректировали на 5-10%.
РАСЧЕТ ЗАТРАТ
Затраты на пероральные сахароснижающие препараты оценивали, основываясь на последних данных Британского национального формуляра [30]. Поскольку точных данных по инсулинам, которые использовали пациенты, не было, стоимость инсулина оценивали как число введенных инсулиновых единиц в сутки, умноженное на среднюю в Великобритании стоимость единицы человеческого инсулина — £ 0,0148 [26].
СТАТИСТИЧЕСКИЙ АНАЛИЗ
Применялось программное обеспечение SPSS. Сравнение показателей массы тела, HbA1c и доз инсулина осуществляли с помощью t-теста для зависимых выборок и однофакторного дисперсионного анализа (One-Way ANOVA). Множественная линейная регрессия (с использованием метода «Enter») применялась для выявления возможных предикторов изменения дозы инсулина. Во всех тестах использовалось значение а 0,05.
СТАТИСТИЧЕСКАЯ ЗНАЧИМОСТЬ И ПОДСЧЕТ РАЗМЕРА ВЫБОРКИ
В соответствии с клиническими данными этой популяции исходное среднее значение HbA1c составило 7,6 (SD (стандартное отклонение)=1,3). При условии односторонней нулевой гипотезы (что H1<H0), а также выборе значений Р=80% и а=5% размер выборки, необходимой для обнаружения небольшого изменения в среднем уровне HbA1c (А5%), был равен 72. Чтобы компенсировать ожидаемые потери за счет выбывающих пациентов на уровне не менее 25%, было решено включить в исходную группу 100 пациентов.
РЕЗУЛЬТАТЫ
Исходные данные
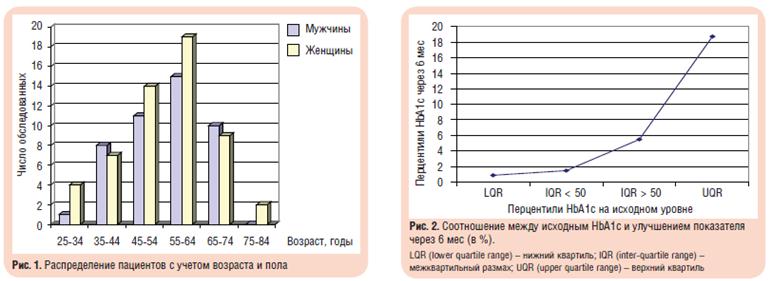
У 91 из 100 включенных в исследование пациентов (45 мужчин и 55 женщин) был СД типа 2. Средний возраст составил: для мужчин 54,5 года (SD=10,8), для женщин — 54,8 года (SD=11,6). Данные о возрасте и поле обследованных приведены на рис. 1. Общая длительность СД составляла 8 лет (соответственно 16,0 и 7,8 года для пациентов с СД типа 1 и 2).
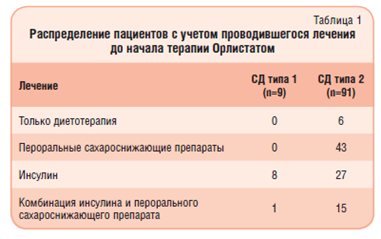
На исходном уровне средний показатель ИМТ составлял 39,5 кг/м2 (SD=6,5); масса тела у мужчин — 126,2 кг (SD=23,7), у женщин — 98,1 кг (SD=18,0). Средний уровень HbA1c, измеренный у 93 пациентов, был 7,6% (SD=1,5), причем почти у 4/5 из них он оказался >6,5%, т.е. выше рекомендованного в Великобритании критического значения, позволяющего избежать развития диабетической ангиопатии у пациентов с СД типа 2 [31]. На инсулинотерапии находился 51 пациент; средняя суточная доза инсулина составляла 130 ЕД (SD=135,4). 57 пациентов получали пероральные сахароснижающие препараты; в том числе 45 — метформин, 15 — препараты сульфонилмочевины, 14 — гликлазид, 1 — толбутамид и 2 — росиглитазон (табл. 1).
Обследование через 6 мес
Из 100 пациентов, включенных в исследование, 82 прошли обследование через 6 мес. Из них у 42 (51,2%) обследованных масса тела снизилась более чем на 5%. Ни у одного пациента не произошло повышения этого показателя. Средняя потеря массы тела составила 7,1 кг (p<0,001), т.е. 6,2% (SD=4,0%).
Прекратили лечение Орлистатом 18 пациентов: 6 — из-за таких нежелательных явлений, как диарея и пачканье одежды (из них 5 не следовали предписанной диете), у 2 пациентов были острые заболевания или госпитализация, не связанные с приемом Орлистата, у 4 пациентов курс терапии прервал лечащий врач, 1 пациент не пришел на обследование, 1 пациентка забеременела, 2 потеряли интерес к проекту (1 из них — по семейным причинам) и 2 отказались из-за отсутствия эффекта при терапии Орлистатом, несмотря на соблюдение всех рекомендаций.
В среднем уровень HbA1c понизился на 0,62% (p<0,001). Среди пациентов, находившихся в начале исследования на инсулинотерапии, 4 (8,0%) прекратили ее через 6 мес. У всех 4 пациентов был СД типа 2, причем 3 из них через 6 мес не прекратили прием пероральных сахароснижающих препаратов. Средняя доза инсулина понизилась со 130 до 90 ЕД (SD=124,1; p<0,001).
Среди пациентов, принимавших только пероральные гипогликемические препараты, у 20 (44,4%) доза их понизилась (статистически незначимо) — из них 7 (35,0%) принимали метформин, 9 (45,0%) — препараты сульфонилмочевины и 4 (20,0%) — гликлазид. Между исходным уровнем HbA1c и улучшением показателя в процентном выражении через 6 мес очевидна экспоненциальная зависимость (рис. 2). Однофакторный дисперсионный анализ (One-Way ANOVA) показал, что разница в среднем процентном улучшении HbA1c между группами квартилей по исходному HbA1c обладает высокой татистической значимостью (p=0,006). Между пациентами, принимавшими инсулин и пероральные препараты, на исходном уровне не было значимых отличий в среднем снижении уровня HbA1c.
HbAlc и потеря массы тела через 24 мес
Через 24 мес 23 пациента продолжали принимать Орлистат. В период с 6-го по 24-й месяц средняя масса тела у них понизилась до 104,7 кг (SD=32,9) после 6 мес лечения и до 99,7 кг (SD=32,4) — после 24 мес лечения (p=0,002); за этот же период средний уровень HbA1c значимо не изменился. Среди 27 пациентов, которые не принимали Орлистат, ни средняя масса тела, ни уровень HbA1c в период с 6-го по 24-й месяц статистически значимо не изменились. Корреляция между улучшением чувствительности к инсулину и изменением ИМТ
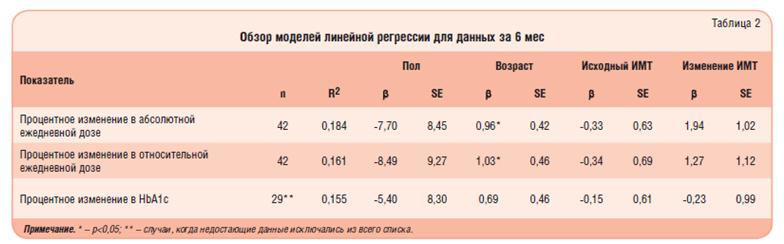
Через 6 мес не обнаружено корреляции между изменением абсолютной дозы инсулина или дозы инсулина в перерасчете на 1 кг (каждая переменная была представлена как % от исходного значения) и изменением массы тела или ИМТ (каждая переменная тоже была представлена как % от исходного значения). Эти результаты получили подтверждение при применении множественной линейной регрессии: после контроля переменных пол, возраст и ИМТ на исходном уровне ни изменения массы тела, ни изменения ИМТ не предсказывали ни абсолютного, ни относительного изменения в дозе инсулина (табл. 2). Возраст был статистически значимым прогностическим фактором абсолютного и относительного изменения дозы инсулина; каждый дополнительный год жизни ассоциировался с уменьшением дозы инсулина на 1%. Однако возраст не ассоциировался с улучшением показателя HbA1c.
Затраты
В целом средняя стоимость лечения СД в день составляла £1,16 исходно и £0,83 — через 6 мес (p<0,001). При условии, что терапия остается постоянной, годовая экономия была эквивалентна £120 на пациента. В случае инсулинзависимого СД стоимость инсулинотерапии в день понижалась с £1,92 до £1,33, а эквивалентная годовая экономия составила £218.
Обсуждение
Снижение массы тела и гликемический контроль являются одинаково важными факторами в лечении пациентов с СД. Однако инсулинотерапия ассоциируется с увеличением массы тела. Данное исследование, основанное на реальном клиническом опыте, подтверждает положительное влияние Орлистата на снижение массы тела и гликемический контроль у пациентов с СД. Ранее это влияние было продемонстрировано в клинических исследованиях [22—25]. Мы также отметили, что улучшение этих показателей не исчезло после 24-месячного периода.
Средняя потеря массы тела в данном исследовании составила 6,2%, что соответствует результатам 4 клинических исследований, в которых для групп пациентов, принимающих Орлистат, данный показатель в среднем составлял 6,2% [22]; 5,4% [23]; 4,6% [24] и 3,9% [25]. Во всех 4 исследованиях потеря массы тела в процентном выражении была гораздо выше в группах Орлистата, чем в контрольной (плацебо). Однако в этих исследованиях результаты наблюдались в конце 12-месячного, а не 6-месячного периода. В настоящем исследовании для пациентов, которые получали терапию Орлистатом в течение 24 мес, средняя общая потеря массы тела между 6-м и 24-м месяцами составила 4,8%.
В модели множественной линейной регрессии, примененной к пациентам, принимавшим Орлистат, проводилось тестирование на исходном уровне ИМТ пола, возраста и процентных изменений ИМТ через 6 мес в качестве показателей, предсказывающих процентное изменение в абсолютной дозе инсулина и при пересчете ее на 1 кг. Анализ показал, что снижение дозы инсулина происходило независимо от потери массы тела. Интересно, что только возраст оказался статистически значимым фактором. Объяснение этого факта может быть связано с согласием пациентов на проведение лечения и их приверженности терапии, но каких-либо данных по приверженности терапии не собирали. Однако этот эффект наблюдался независимо от изменения массы тела, поэтому может считаться показателем приверженности пациентов терапии. Таким образом, возможно, что относительное действие Орлистата на чувствительность к инсулину увеличивается с возрастом.
При улучшении гликемического контроля снижается частота развития макро- и микроангиопатий [16]. Улучшение гликемического контроля выражалось как в уменьшении числа пациентов, которым требовался инсулин, так и в снижении средней дозы инсулина для больных, находившихся на инсулинотерапии. Дополнительно отмечалось снижение доз пероральных сахароснижающих препаратов.
По результатам исследования UKPDS, проведенного у пациентов с СД типа 2, средняя стоимость интенсивной инсулинотерапии составила £230 в год [32]. Однако репрезентативность выборки была искажена строгими критериями отбора; в реальности, как свидетельствует данное исследование, затраты гораздо выше. Проведенное исследование показывает, что в исходный период средняя стоимость только одной инсулинотерапии составляет £704 в год; у обследованных через 6 мес это значение снизилось до £486. Экономия лишь на сахароснижающих препаратах составила £120 в год для всей группы в целом и £218 — для подгруппы больных, принимающих инсулин, что достоверно возмещает затраты по использованию Орлистата.
Поскольку данное исследование основывалось на реальном клиническом опыте, не представляется возможным определить, насколько отмеченные эффекты можно было отнести за счет действия Орлистата, а не изменения образа жизни или диеты после консультации с диетологом. Осложняющим фактором, как упоминалось выше, стало отсутствие наблюдения за приверженностью пациентов терапии. Однако у 20% пациентов отмечались специфические нежелательные явления, свидетельствующие о приеме Орлистата [33].
Данное исследование показало, что лечение Орлистатом (Ксеникалом) приводит к статистически значимому снижению массы тела, а также к улучшению гликемического контроля и снижению объема сопутствующей сахароснижающей терапии. Зависимость между снижением гликемических показателей по мере увеличения возраста представляется весьма интересной и требует дальнейшего изучения.
Литература
- Joint Health Surveys Unit on behalf of the Department of Health. Health survey for England: cardiovascular disease 1998. London: The Stationery Office, 1999.
- Storing up problems, the medical case for a slimmer nation. Report of a working party, Royal College of Physicians, Royal College of Paediatrics and Child Health, Faculty of Public Health. London: Royal College of Physicians, 2004.
- Flegal K. M., Carroll M. D., Kuczmarski R. J. et al. Overweight and obesity in the United States: prevalence and trends, 1960-1994 // Int. J. Obes. Relat. Metab. Disord. - 1998; 22: 39-47.
- National Audit Office. Tackling obesity in England. London: The Stationery Office, 2001.
- Calle E. E., Thun M. J. Obesity and cancer // Oncogene. - 2004; 23: 6365-6378.
- Arik T. H., Desser K. B., Benchimol A. Obesity and heart disease // Ariz Med. - 1985; 42: 12-13.
- Shinton R., Sagar G., Beevers G. Body fat and stroke: unmasking the hazards of overweight and obesity // J. Epidemiol. Community Health. - 1995; 49: 259-264.
- Kim S. H., Abbasi F., Reaven G. M. Impact of degree of obesity on surrogate estimates of insulin resistance // Diabetes. Care. - 2004; 27: 1998-2002.
- Boden G. Free fatty acids - the link between obesity and insulin resistance // Endocr Pract. - 2001; 7: 44-51.
- Morgan C. L., Currie C. J., Stott N. C. et al. The prevalence of multiple diabetes-related complications // Diabet Med. - 2000; 17: 146-151.
- Astrup A., Finer N. Redefining type 2 diabetes: «diabesity» or «obesity dependent diabetes mellitus?» // Obes Rev. - 2000; 1: 57-59.
- Ford E. S., Williamson D. F., Liu S. Weight change and diabetes incidence: findings from a national cohort of US adults // Am J. Epidemiol. - 1997; 146: 214-222.
- Hickey M. E., Hall T. R. Insulin therapy and weight change in Native-American NIDDM patients // Diabetes Care. - 1993; 16: 364-368.
- Vidal J. Updated review on the benefits of weight loss // Int. J. Obes. Relat. Metab. Disord. - 2002; 26 (Suppl. 4): 25-28.
- Tuomilehto J., Lindstrom J., Eriksson J. G. et al. Prevention of type 2 diabetes mellitus by changes in lifestyle among subjects with impaired glucose tolerance // N. Eng. J. Med. - 344; 18: 1343-1350.
- Stratton I. M., Adler A. I., Neil H. A. et al. Association of glycaemia with macrovascular and microvascular complications of type 2 diabetes (UKPDS 35): prospective observational study // BMJ. - 2000; 321: 405-412.
- Miller Y. D., Dunstan D. W. The effectiveness of physical activity interventions for the treatment of overweight and obesity and type 2 diabetes // J. Sci. Med. Sport. - 2004; 7 (Suppl. 1): 52-59.
- Beebe C. A., Pastors J. G., Powers M. A. et al. Nutrition management for individuals with noninsulin-dependent diabetes mellitus in the 1990s: a review by the Diabetes Care and Education dietetic practice group // J. Am. Diet. Assoc. -1991; 91: 196-202.
- Guerciolini R. Mode of action of orlistat // Int J. Obes Relat Metab Disord. - 1997; 21: 12-23.
- Finer N., James W. P., Kopelman P. G. et al. One-year treatment of obesity: a randomized, double-blind, placebo-controlled, multi-centre study of orlistat, a gastrointestinal lipase inhibitor // Int. J. Obes Relat Metab Disord. - 2000; 24: 306-313.
- Sjostrom L., Rissanen A., Anderson T. et al. Randomised placebo-controlled trial of orlistat for weight loss and prevention of weight regain in obese patients // Lancet. - 1998; 352: 167-173.
- Hollander P. A., Elbein S. C., Hirsch I. B. et al. Role of orlistat in the treatment of obese patients with type 2 diabetes. A 1-year randomized double-blind study // Diabetes Care. - 1998; 21: 1288-1294.
- Hanefeld M., Sachse G. The effects of orlistat on body weight and glycae-mic control in overweight patients with type 2 diabetes: a randomised placebo-controlled trial // Diabetes Obes Metab. - 2002; 4: 415-423.
- Miles J. M., Leiter L., Hollander P. et al. Effect of orlistat in overweight and obese patients with type 2 diabetes treated with metformin // Diabetes Care. -2002; 25: 1671.
- Kelley D. E., Bray G. A., Pi-Sunyer F. X. et al. Clinical efficacy of orlistat therapy in overweight and obese patients with insulin-treated type 2 diabetes: A 1-year randomized controlled trial // Diabetes Care. - 2002; 25: 1033-1041.
- Heymsfield S. B., Segal K. R., Hauptman J. et al. Effects of weight loss with orlistat on glucose tolerance and progression to type 2 diabetes in obese adults // Arch Intern Med. - 2000; 160: 321-326.
- Kelley D. E., Kuller L. H., McKolanis T. M. et al. Effects of moderate weight loss and orlistat on insulin resistance, regional adiposity, and fatty acids in type 2 diabetes // Diabetes Care. - 2004; 27: 33-40.
- Summary of product characteristics for Xenical. Available from http:// www.emc.medicines.org.uk/emc/assets/c/html/ displaydoc. asp?documentid=1746#INDICATIONS [Accessed 4 Aug 2005].
- National Institute for Clinical Excellence. Orlistat for treatment of obesity in adults. Available from http://www.nice.org.uk/page. aspx?o=15731 [Accessed 29 Sept 2005].
- National Formulary. Available from http://www.bnf.org [Last Accessed 28 September 2005].
- PRODIGY guidance - diabetes type 2 - blood glucose management. Available from http://www.prodigy.nhs.uk/ guidance.asp?gt=Diabetes%20-%20 glycaemic%20control [Accessed 28 Sept 2005].
- National Institute for Clinical Excellence. 2000/026 NICE issues guidance on rosiglitazone for type 2 diabetes. Available from http:// www.nice.org.uk/page. aspx?o=38020 [Accessed 1 July 2005].
- Ballinger A. Orlistat in the treatment of obesity // Expert Opin Pharmacother. - 2000; 4: 841-847.
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


