
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
- Новини 26.10.2021 Аппаратура для УЗИ: применение, принципы работы, разновидности
- Новини 23.10.2021 Интимная пластика после родов: когда необходима операция
Нарушения менструального цикла у подростков и молодых женщин с ожирением
Ожирение играет большую роль в нарушении репродуктивного здоровья. Назначение Ксеникала® позволяет добиться восстановления менструальной функции у 78,9% больных, а у 26,3% — овуляторной функции. Проведение гормональной терапии у пациенток с ожирением должно сопровождаться назначением Ксеникала®, что позволяет добиться дальнейшего снижения массы тела (на 13,95% от исходного) и улучшения (либо стабильности) показателей метаболизма.
Ожирение играет большую роль в нарушении репродуктивного здоровья. Менструальная дисфункция, синдром поликистозных яичников (СПКЯ), гиперпластические процессы эндометрия (ГПЭ), бесплодие, невынашивание беременности, гестозы, гипотрофия плода — неполный список нарушений репродуктивного здоровья у женщин с ожирением [10, 21], и предпосылки к их развитию закладываются уже в детском и подростковом возрасте, с началом полового созревания девочки.
Несмотря на то, что в последние годы существенно изменились взгляды на патогенез формирования нарушений менструального цикла у женщин с ожирением, как показывает практика, клиницисты не уделяют должного внимания этой проблеме. До сих пор отсутствуют четко определенные показания к проведению терапии, направленной на снижение массы тела, и гормональному лечению у подростков и молодых женщин с ожирением для коррекции нарушений менструального цикла.
Целью настоящего исследования явилась разработка принципов лечения подростков и женщин раннего репродуктивного возраста с нарушениями менструального цикла на фоне ожирения.
Объект и методы исследования
В основу работы легли результаты обследования и лечения 62 пациенток, из них 28 подростков (средний возраст 17,4±1,4 лет) и 34 женщины раннего репродуктивного возраста (средний возраст 24,7±2,6 лет), страдающих нарушениями менструального цикла на фоне ожирения.
Отбор пациенток для исследования велся согласно следующим критериям:
- возраст 14-29 лет;
- период времени от менархе не менее 2 лет;
- индекс массы тела (ИМТ) более 29,9;
- нерегулярный менструальный цикл: олигоменорея (длительность межменструальных периодов от 36 до 180 дней), аменорея (отсутствие менструации в течение 6 и более месяцев), метроррагии (ациклические кровотечения);
- длительность нарушений менструального цикла не менее 6 месяцев до момента обращения;
- отсутствие гормональной терапии, по меньшей мере, в течение 3 месяцев до момента обращения. Критериями исключения явились:
- отказ от лечения;
- врожденные наследственные синдромы, ассоциированные с ожирением;
- эндокринопатии (гипотиреоз, синдром или болезнь Иценко-Кушинга, гиперпролактинемия, инсулинзависимый сахарный диабет и др.).
У всех пациенток до, в процессе и после лечения оценивали:
- антропометрические показатели: вес, рост, окружность талии (ОТ) и бедер (ОБ), определение соотношения ОТ/ОБ и индекса массы тела (ИМТ = вес, кг/(рост, м2);
- липидный спектр крови: общий холестерин (ХС), триглицериды (ТГ), холестерин липопротеидов высокой плотности (ХС ЛПВП) (ферментативный метод, биохимический анализатор «Konelab 60/60i», Финляндия). Расчетным методом определяли холестерин липопротеидов низкой плотности (ХС ЛПНП);
- углеводный обмен: проводили пероральный глюкозотолерантный тест (ПТТГ), с определением в сыворотке крови натощак и через 2 часа после углеводной нагрузки глюкозы (глюкозооксидантный метод, биохимический анализатор «Konelab 60/60i», Финляндия) и иммунореактивного инсулина (иммунохемилюминесцентный метод, автоматическая система IMMULITE® 2000 фирмы «DPC», США). Гиперинсулинемией (ГИ) считали повышение уровня инсулина выше 25 мкМЕ/мл натощак и/или выше 28,5 мкМЕ/мл через 2 часа после нагрузки глюкозой. Для определения инсулинорезистентности (ИР) использовали показатели индексов: HOMA—IR (Homeostasis Model Assessment) = глюкоза натощак (ммоль/л) х инсулин натощак (мкМЕ/мл)/22,5; Caro = глюкоза натощак (ммоль/л)/инсулин натощак (мкМЕ/мл). Значение индекса Caro <0,33 и значение индекса HOMA—IR >2,7 считали косвенными признаками наличия ИР;
- гормональный спектр крови: лютеинизирующий гормон (ЛГ), фолликулостимулирующий гормон (ФСГ), пролактин (Прл), эстрадиол (Е2), тестостерон (Т), андростендион (А) (иммунохемилюминесцентный метод, анализатор ADVIA Centaur® фирмы «Bayer Diagnostics», США); дигидроэпиандростендиона сульфат (ДГЭА-С), кортизол, половые стероиды связывающий глобулин (ПССГ) (автоматическая система IMMULITE® 2000 фирмы «DPC», США). Лептин определяли иммуноферментным методом при помощи тест-систем LEPTIN ELISA, Diagnostics Biochem Canada Inc. Гиперлептинемией считали повышение уровня лептина свыше верхней границы нормальных значений, предложенных фирмой-производителем (3,4-11,1 нг/мл для женщин). Соотношение ЛГ/ФСГ >2,5 считали маркером СПКЯ. Рассчитывали индекс свободных андрогенов (ИСА) и индекс свободных эстрогенов (ИСЭ);
- ультразвуковое исследование (УЗИ) органов малого таза проводили на сканере Logiq 500 PRO («GE Medical systems», США) с использованием абдоминального и вагинального конвексных датчиков частотой 3,5 и 7,5 МГц соответственно. Определяли размеры матки и яичников, величину срединного маточного эха (М-эхо) и соответствие его дню менструального цикла;
- гистероскопия с диагностическим выскабливанием стенок полости матки проводилась по показаниям по общепринятой методике с последующим гистологическим исследованием удаленных тканей.
На первом этапе лечения (6 месяцев) пациентки получали терапию, направленную на коррекцию массы тела. Эффект терапии оценивали по восстановлению регулярного менструального цикла. При отсутствии или неполном эффекте переходили на второй этап лечения (6 месяцев), где к основному лечению добавлялась гормонотерапия либо дидрогестероном, либо комбинированным оральным контрацептивом (КОК), содержащим дроспиренон.
В исследовании применялись: орлистат (Ксеникал®, «Ф. Хоффманн-Ля Рош Лтд.», Швейцария) в дозе 360 мг/сут; дидрогестерон (Дюфастон®) в циклическом режиме с 16-го по 25-й день менструального цикла у подростков и с 11-14-го дня менструального цикла у взрослых женщин в дозе 20 мг/сут; низкодозированный КОК, содержащий дроспиренон (Ярина®), по стандартной 21-дневной схеме с 7-дневными перерывами.
Статистическую обработку полученных результатов проводили по общепринятой методике с использованием компьютерных статистических программ Microsoft Excel 2003, BIOSTAT version 4.03, SPSS version 15,0 (США). Для изучаемых параметров определяли среднюю величину и стандартное отклонение. Применяли параметрические методы (дисперсионный анализ и парный критерий Стьюдента) и непараметрические статистические методы (критерий Манна-Уитни, критерий Крускала-Уоллиса, х2). Корреляционный анализ методом Пирсона проводили для нормально распределенных признаков, методом Спирмена для остальных. Значимыми различия между группами считались при уровне р<0,05.
Результаты исследования и их обсуждение
При анализе характеристик менструального цикла было обнаружено, что наиболее частым типом нарушений (у 60,7% подростков и 58,8% молодых женщин) была олигоменорея, однако с возрастом отмечалась тенденция к увеличению числа пациенток с метроррагиями на фоне олигоменореи. Наши данные подтверждают мнение других исследователей, которые указывают на превалирование олигоменореи в структуре аномалий менструального цикла у подростков [9] и молодых женщин [6], а также на частое формирование гиперплазии эндометрия и сопутствующих ей метроррагий при длительном существовании ановуляции на фоне ожирения. У каждой третьей женщины, обратившейся к нам с нарушениями менструального цикла, при гистологическом исследовании эндометрия были выявлены ГПЭ, причем у 25% больных они носили рецидивирующий характер.
На момент первичного обследования ожирение I степени наблюдалось у 41 (66,1%) пациентки, II степени - у 13 (21,0%), а III степени - у 8 (12,9%) пациенток. У всех пациенток (100%) величина ОТ превышала 80 см (89-й процентиль для подростков до 16 лет), отражая наличие висцерального ожирения [11, 24].
Нарушения углеводного обмена были обнаружены у всех пациенток: в ходе проведения ПТТГ в 100% случаев была выявлена стимулированная ГИ. Тощаковая ГИ и ИР наблюдались, соответственно, у 12 (42,9%) и 23 (82,1%) подростков, а в группе женщин эти показатели составили 9 (26,5%) и 25 (73,5%). Более высокие показатели тощаковой ГИ и ИР у подростков, вероятно, объясняются тем, что пубертатный период — это период физиологической ИР. С другой стороны, с возрастом происходит истощение в-клеток поджелудочной железы, что приводит к относительной недостаточности инсулина и постепенному развитию нарушения толерантности к глюкозе (НТГ) и сахарного диабета 2-го типа [3]. Так, в группе молодых женщин мы обнаружили, что доля пациенток с НТГ была значимо выше по сравнению с подростками, 12 (35,3%) и 3 (10,7%) соответственно (р=0,03).
Структура нарушений липидного спектра в обеих возрастных группах была практически идентична, и значимых отличий по его показателям выявлено не было. Однако в группе женщин гиперхолестеринемия (50%), гипоальфалипидемия (61,8%) и гипертриглицеридемия (26,5%) встречались несколько чаще, чем у подростков (42,9, 50 и 17,9% соответственно).
На основании критериев, предложенных Third Adult Treatment Panel III [17], метаболический синдром (МС) нами был диагностирован у 7 (25%) подростков и 20 (58,9%) взрослых женщин. В исследовании О.В. Бородиной [1] в группе подростков с ожирением у 29% из них отмечались различные сочетания клинико-лабораторных нарушений, характерных для МС. Среди взрослого населения, страдающего ожирением, частота МС составляет 49%, а в возрастной группе от 16 до 22 лет он наблюдается у 35% пациентов [2].
В гормональном профиле у пациенток разных возрастных групп наблюдалась сходная структура нарушений. Повышение уровня ЛГ и соотношения ЛГ/ФСГ выше 2,5 с формированием СПКЯ наблюдалось у 7 (25%) подростков и 8 (23,5%) женщин раннего репродуктивного возраста; изолированное повышение Т и/или А — у 10 (35,7%) подростков и 11 (32,4%) женщин; у 4 (14,3%) подростков и 7 (20,6%) женщин на фоне повышенных уровней яичниковых андрогенов отмечались признаки гиперкортицизма. У остальных пациенток нарушений в гормональном профиле выявлено не было, но за счет снижения уровня ПССГ отмечалось повышение уровня свободных андрогенов. У 100% обследованных пациенток была обнаружена гиперлептинемия. Кроме обратной корреляционной зависимости между уровнями лептина и ПССГ (r=-0,425; p=0,034), нами выявлена значимая корреляционная зависимость между лептином и Т (r=0,406; p=0,026), которую также наблюдала в своем исследовании Н.А. Крапивина [6].
На I этапе лечения проводилась терапия ожирения препаратом Ксеникал (орлистат) (табл. 1). Ксеникал был выбран благодаря его местному механизму действия, которое ограничено ЖКТ. Эффект препарата достигается подавлением активности желудочно-кишечных липаз, в результате чего всасывание жиров из пищи снижается примерно на 30%. На фоне лечения подростки снизили вес в среднем на 8,7±1,2%, женщины — на 13,6±4,2% от исходных значений. В обеих группах шло улучшение антропометрических показателей и нормализация липидного спектра крови, на что также указывают большинство исследователей, применявших орлистат, как у взрослых [6, 14, 20], так и у подростков [12, 16, 18].
Влияние орлистата на улучшение чувствительности к инсулину, не зависящее от снижения массы тела, было показано в рандомизированном исследовании эффектов монотерапии орлистата у больных сахарным диабетом 2 типа [15]. У наших пациенток обеих возрастных групп при приеме орлистата также отмечалась нормализация уровней тощакового и стимулированного инсулина, индекса HOMA—IR. Похожее влияние орлистата на углеводный обмен у пациенток репродуктивного возраста с нарушениями менструальной функции и СПКЯ было отмечено и другими авторами [6, 14].
При приеме орлистата в гормональном профиле происходило снижение выраженности гиперандрогении, как за счет значимого уменьшения уровней Т и А, так и благодаря значимому повышению ПССГ. У подростков статистически значимо снижалось соотношение ЛГ/ФСГ (р=0,011) и уровень Е2 (р=0,005), что привело к уменьшению ИСЭ (р=0,006), чего не наблюдалось у женщин. Работ по изучению влияния орлистата на гормональный профиль у подростков мы не встретили, но Th. Reinehr с соавт. [19] показали, что при потере веса у детей препубертатного и пубертатного возраста на фоне диетотерапии значимо снижаются уровни ДГЭА-С и тестостерона. Это позволяет говорить об опосредованном влиянии орлистата на гормональный профиль через снижение массы тела и, очевидно, большую зависимость эндокринного гомеостаза от количества жировой ткани у подростков по сравнению со взрослыми женщинами.
Кроме того, у всех пациенток по окончанию лечения значимо снизился уровень лептина. Уменьшение гиперлептинемии при монотерапии орлистатом у тучных пациенток репродуктивного возраста, как с нарушениями менструального цикла, так и с МС отмечали и ранее [4, 6].
При снижении массы тела на фоне проведения лечения орлистатом восстановление регулярной менструальной функции наблюдалось у 49 (79%) больных, у 16 (25,8%) пациенток зарегистрированы овуляторные циклы. В группе молодых женщин овуляция наблюдалась в 2 раза чаще, чем у подростков, что обусловлено как большим снижением массы тела, так и большей зрелостью их репродуктивной системы.
У 13 пациенток — 8 (28,6%) подростков и 5 (14,7%) молодых женщин — наблюдался неудовлетворительный результат. Пять подростков отказались от лечения на I этапе из-за развившихся у них побочных эффектов. Такую же реакцию у подростков наблюдали практически все исследователи, применявшие орлистат для лечения ожирения в этой возрастной группе [12, 16, 18], что объясняется сниженной мотивацией к проводимому лечению и отсутствием у детей подросткового возраста полного представления о ценности своего здоровья [5].
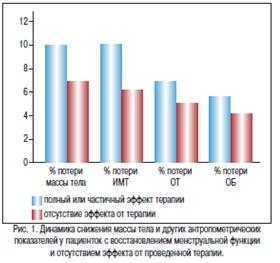
Проанализировав в сравнительном аспекте результаты I этапа лечения пациенток с отсутствием эффекта терапии и пациенток, у которых отмечалась нормализация менструальной функции, мы обнаружили, что восстановление менструального цикла сопровождалось потерей массы тела, в среднем, на 10,0% от исходного показателя, что было значимо выше, чем у пациенток с отсутствием эффекта, 7,3% (р=0,017) (рис. 1).
Кроме того, у пациенток с отсутствием эффекта терапии уровень лептина, несмотря на его значимое снижение, оказался в 2 раза выше (52,5±16,8 нг/мл), чем у пациенток с нормализацией менструального цикла.
Положительные сдвиги в гормональном профиле наблюдались у всех пациенток — уменьшалась выраженность гиперандрогении и гиперэстрогении. Но, по сравнению с пациентками, у которых менструальный цикл нормализовался, в группе с отсутствием эффекта от терапии оставались значимо высокими уровень ЛГ (9,15±4,05 мМЕ/мл, р=0,002) и ИСЭ (7,53±2,25, р=0,042), а уровень пролактина (242,4±58,8 мкМЕ/л) и кортизола (261,8±77,9 нмоль/л) оказался значимо ниже (р=0,037 и р=0,022, соответственно)
Полученные данные позволяют предположить, что у пациенток, не ответивших на терапию, направленную на коррекцию веса, в развитии нарушений менструального цикла помимо ожирения играют роль такие факторы, как дисфункция центральной нервной системы и генетически обусловленные дефекты стероидогенеза. Такого же мнения придерживаются и другие авторы [7].
После проведенного I этапа лечения, несмотря на высокий процент восстановления регулярной менструальной функции, ановуляция сохранялась у значительного числа пациенток. Из них (46 пациенток) на II этапе было сформировано две группы с учетом половой активности и желания реализации детородной функции. Пациенткам, планирующим детородную функцию или не живущим половой жизнью, к основному лечению добавлялся дидрогестерон, а женщинам, нуждающимся в контрацепции, — КОК с дроспиреноном.
Действие гормональных препаратов на метаболизм неоднозначно, что определяет осторожность в назначении этих препаратов пациентам с ожирением. Наиболее показательно в этой связи действие эстрогенов, которые непосредственно влияют на синтез липопротеидов в печени благодаря повышению синтеза ароА1, down-регуляции печеночных скэвенджер-рецепторов типа 1 класса В (SRB-1) и снижению активности печеночной липазы [22]. Результатом такого влияния синтетических препаратов, содержащих эстрадиол, становится повышение уровня ХС ЛПВП и триглицеридов [8], последнее обстоятельство нежелательно при ожирении.
Подобно эстрогенам, андрогены непосредственно влияют на обмен жиров через ферментативные системы печени. В отношении жирового обмена андрогены ведут себя как антагонисты эстрогенов, повышая активность печеночной липазы, экспрессию SRB-1, препятствуя эстрогензависимому синтезу апобелков липопротеидов в печени. Результатом этого влияния становится снижение ХС ЛПВП в плазме крови [13]. Из-за возможности такого эффекта прогестагены, обладающие остаточной андрогенной активностью, нежелательно назначать пациенткам, предрасположенным к нарушениям метаболизма. Это стало причиной выбора метаболически нейтрального прогестагена дидрогестерона и КОК, содержащего дроспиренон, не обладающий остаточной андрогенной активностью и имеющий благоприятный антиминералокортикоидный эффект.
На II этапе лечения в обеих группах продолжалась потеря веса, начавшаяся на I этапе, улучшились все антропометрические показатели, за исключением показателя ОТ/ОБ у пациенток, принимавших КОК.
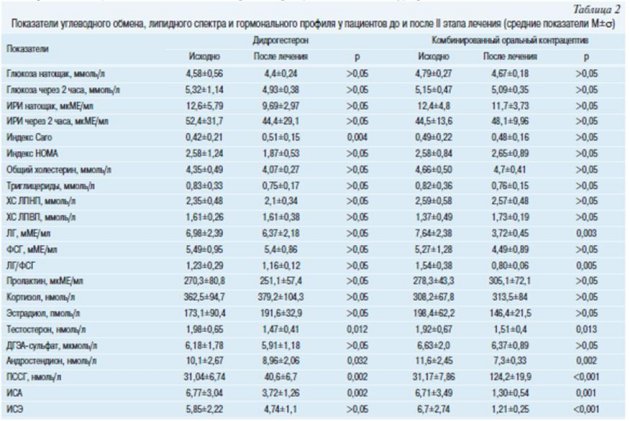
Одновременно с потерей массы тела у пациенток обеих возрастных групп как при приеме дидрогестерона, так и при приеме КОК сохранялась стабильность или положительная динамика показателей липидного и углеводного обмена, чего не наблюдается при монотерапии любыми видами КОК, в том числе и содержащими дроспиренон [8, 23] (табл. 2).
В гормональном профиле у всех пациенток продолжалось снижение уровней Т, А и повышение уровня ПССГ. Следует отметить, что в группе пациенток, принимавших КОК с дроспиреноном, повышение ПССГ было в 3 раза выше, чем в группе принимавших дидрогестерон, что связано с влиянием эстрогенного компонента КОК на печень. Кроме того, в группе пациенток, принимавших КОК, значимо снизились уровень ЛГ и соотношение ЛГ/ФСГ, чего не наблюдалось у больных, использовавших дидрогестерон, где лишь наметилась тенденция к снижению этих показателей. Изменения гормонального профиля привели к снижению ИСА и ИСЭ при приеме дидрогестерона и к нормализации их при приеме КОК.
При динамическом ультразвуковом исследовании в обеих группах, как у подростков, так и молодых женщин отмечалось уменьшение среднего объема яичников, а на фоне приема дидрогестерона у 40% пациенток восстановилась овуляторная функция.
Таким образом, одновременное использование терапии, направленной на снижение массы тела, коррекцию метаболизма и гормонотерапии, повышает приемлемость последней у пациенток с ожирением и менструальной дисфункцией, позволяя избежать ее негативных влияний.
Выводы
- У подростков и женщин раннего репродуктивного возраста с ожирением в структуре нарушений менструального цикла превалирует олигоменорея, с возрастом на фоне олигоменореи увеличивается частота метроррагий, отражающая формирование гиперпластических процессов эндометрия. В основе менструальной дисфункции в обеих возрастных группах лежит гиперандрогенная ановуляция, сформировавшаяся в условиях гиперинсулинемии и гиперлептинемии.
- У пациенток с нарушениями менструального цикла на фоне ожирения с возрастом увеличивается распространенность метаболического синдрома (25,6% у подростков; 57,7% у молодых женщин) и нарушений толерантности к глюкозе (9,3% до 34,6% соответственно), при этом частота СПКЯ остается стабильной как в пубертатном (25,6%), так и в раннем репродуктивном возрасте (23,0%).
- Назначение Ксеникала позволяет добиться восстановления менструальной функции у 78,9% больных, а у 26,3% — овуляторной функции. Клинически значимой потерей массы тела для репродуктивной системы является 10% и более от исходной, при которой возможно спонтанное восстановление овуляции; потеря веса в диапазоне от 5 до 10% сопровождается регуляцией ритма менструаций и улучшением показателей жирового и углеводного обмена.
- Сохранение ановуляторной дисфункции яичников при недостаточном снижении массы тела наблюдается у 73,7%, отражает формирование СПКЯ и/или наличие дисфункции гипоталамо-гипофизарной системы и является основанием для назначения гормональной терапии. Проведение гормональной терапии (Дюфастон®, Ярина®) у пациенток с ожирением должно сопровождаться назначением препарата Ксеникал®, что позволяет добиться дальнейшего снижения массы тела (на 13,95% от исходной) и улучшения (либо стабильности) показателей метаболизма.
Литература.
1.Бородина О.В. Ожирение у детей и подростков (факторы риска метаболического синдрома) // Автореф. дис. ... канд. мед. наук. М., 2005; 23 с.
2.Бутрова С.А., Дзгоева Ф.Х. Висцеральное ожирение - ключевое звено метаболического синдрома // Ожирение и метаболизм 2004; 1: 10-6.
3.Дедов И.И., Мельниченко Г.А. Ожирение: этиология, патогенез, клинические аспекты // М.: ООО «МИА», 2004; 456 с.
4.Ершова Е.В., Колесникова Г.С., Бутрова С.А. Клиническая, метаболическая и гормональная эффективность применения орлистата у пациентов с метаболическим синдромом // Ожирение и метаболизм 2004; 1: 34-7. 5.Кабаева В.М. Формирование осознанного отношения к собственному здоровью у подростков // Автореф. дис. ... канд. псих. наук. М., 2002; 31 с. 6.Крапивина Н. А. Оптимизация лечения ожирения у женщин репродуктивного возраста // Автореф. дис. ... канд. мед. наук. Кемерово, 2005; 24 с.7. Манухин И.Б., Геворкян М.А., Кушлинский Н.Е. Синдром поликистозных яичников // М.: ООО «МИА», 2004; 192 с. 8.Подзолкова Н.М., Глазкова О.Л., Сумятина Л.В. Метаболические эффекты низкодозированного контрацептива «Ярина» у пациенток с нормальной массой тела и умеренным ожирением // Гинекология 2005; 3 (7): 181-3. 9.Уварова Е.В. Детская и подростковая гинекология: руководство для врачей // М.: Литтерра, 2009; 238 с. 10.Шехтман М.М. Руководство по экстрагенитальной патологии у беременных//М.: Триада, 2003; 816 с. 11.Alberti K.G., Zimmet P., Shaw J. Metabolic syndrome - a new world-wide definition. A Consensus Statement from the International Diabetes Federation // Diabetic Medicine, 2006; 23: 469-80. 12.Chanoine J.-P., Hampl S., Jensen C. et al. Effect of Orlistat on weight and body composition in obese adolescents: a randomized controlled trial // JAMA 2005; 293(23): 2873-83. 13.Jansen H., Verhoeven A.J.M., Sijbrands J.G. Hepatic lipase: a pro- or antiatherogenic protein? // J Lipid Research 2002; 43: 1352-62. 14.Jayagopal V., Kilpatrick E.S., Holding S. et al. Orlistat is as beneficial as metformin in the treatment of polycystic ovarian syndrome // J Clin Endocrinol Metab 2005; 90(2): 729-33. 15.Kelley D. E., Kuller L. H., McKolanis Th. M. et al. Effects of moderate weight loss and orlistat on insulin resistance, regional adiposity, and fatty acids in type 2 diabetes // Diabetes Care 2004; 27(1): 33-40. 16.McDuffie J.R., Calis K.A., Uwaifo G.I. et al. Efficacy of orlistat as an adjunct to behavioral treatment in overweight African American and Caucasian adolescents with obesity-related co-morbid conditions // J Pediatr Endocrinol Metab, 2004; 17(3): 307-19. 17.National Institutes of Health. The third report of National Cholesterol Education Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adult (Adult Treatment Panel III) // NIH Publication 01 -3670. Bethesda, MD: National Institutes of Health, 2001. 18.Ozkan B., Bereket A., Turan S., Keskin S. Addition of orlistat to conventional treatment in adolescents with severe obesity // Eur J Pediatr, 2004; 163(12): 738-41. 19.Reinehr Th., de Sousa G., Roth Ch. L., Andler W. Androgens before and after weight loss in obese children // J Clin Endocrinol Metab, 2005; 90(10): 5588-95. 20.Sari R., Balci M.K., Coban E., Yazicioglu G. Comparition of effect of orlistat vs orlistat plus metformin on weight loss and insulin resistance in obese women // Int J Obes, 2004; 28(8): 1059-63. 21.Stepan H., Scheithauer S., Dornhbfer N. et al. Obesity as an obstetric risk factor: does it matter in a perinatal center? // Obesity, 2006; 14: 770-3. 22.Trigatti B.L., Krieger M., Rigotti A. Influence of the HDL receptor SRB-1 on lipoprotein metabolism and atherosclerosis // Arterioscler Tromb Vasc Biol 2003; 23: 1732-8. 23.Vrbicova J., Cibula D. Combined oral contraceptives in the treatment of polycystic ovary syndrome // Hum Reprod Update, 2005; 11(3): 277-91. 24.Zimmet P., Alberti K.G., Kaufman F.T. et al., IDF Consensus Group. The metabolic syndrome in children and adolescents - an IDF consensus report // Pediatr Diabetes 2007; 8(5): 299-306.
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


