
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
- Новини 26.10.2021 Аппаратура для УЗИ: применение, принципы работы, разновидности
- Новини 23.10.2021 Интимная пластика после родов: когда необходима операция
Инсулинотерапия сахарного диабета
Статья из монографии "Сахарный диабет: от ребёнка до взрослого".
Инсулинотерапия – основное и единственное средство лечения сахарного диабета 1-го типа.
В физиологических условиях секреция инсулина происходит в два этапа: поджелудочная железа секретирует инсулин постоянно (базальная инсулинемия), а в ответ на соответствующие стимулы (посталиментарная гипергликемия, или гипергликемия, вызванная действием контринсулярных гормонов) повышает секрецию инсулина. При этом нормогликемия в здоровом организме обеспечивается быстрой адекватной секрецией инсулина, а также коротким периодом полужизни (около 4 мин.) циркулирующего в крови инсулина.
Основная цель современной инсулинотерапии – поддержание состояния углеводного обмена, близкого к физиологическому (рис. 7.2).
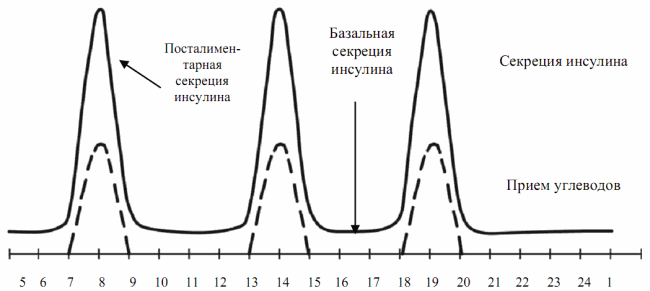
При экзогенном введении инсулин из подкожного депо медленно всасывается в общий кровоток, где концентрация его длительно остается нефизиологично высокой (рис. 7.3).
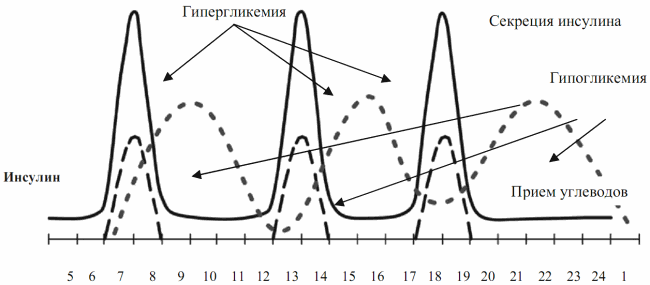
Рис. 7.3. Эффекты экзогенно вводимого инсулина в сравнении с физиологической секрецией
На рисунке видно, что кривые физиологической секреции инсулина и экзогенно введенного препарата не совпадают, причем не происходит своевременное обеспечение гормоном углеводов при питании. В результате – более высокая, чем у здоровых, посталиментарная гипергликемия и склонность к гипогликемии в более поздние часы.
При проведении инсулинотерапии возникают и другие проблемы:
- Из общего кровотока инсулин одновременно поступает в печень и другие органы-мишени. В результате гликоген депонируется в первую очередь в мышечной ткани, а запасы его в печени постепенно снижаются. Это является одной из причин развития гипогликемий, так как мышечный гликоген мало участвует в поддержании нормогликемии.
- Добиться физиологического соотношения концентрации гормона в портальной системе и на периферии при современных методах введения экзогенного инсулина невозможно, и это одна из наиболее сложных проблем заместительной инсулинотерапии.
Современные препараты инсулина в зависимости от происхождения разделяют на две группы – животные и человеческие (полусинтетический и биосинтетический инсулины). В последние годы к применению рекомендуются человеческие инсулины, обладающие низкой иммуногенностью (рис. 7.4).
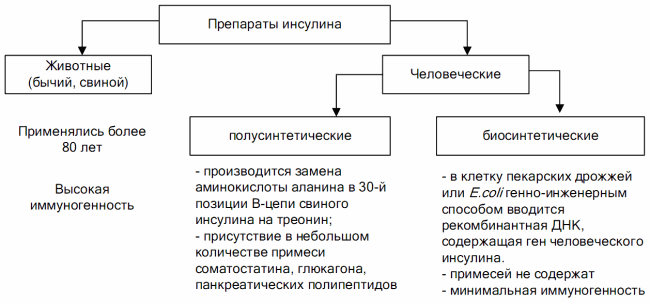
Рис. 7.4. Препараты инсулина
В табл. 7.3 приводим некоторые препараты инсулина с указанием начала и длительности их действия в соответствии с национальным стандартом оказания помощи детям, больным сахарным диабетом.
|
Препарат инсулина |
Начало действия |
Пик действия |
Максимальная длительность действия |
|
Короткого действия: |
30 мин. |
1-3 часа |
6-8 часов |
|
Аналоги инсулина быстрого действия (ультракороткого): |
5-15 мин. |
1-2 часа |
3-5 часов |
|
Длительного действия: |
1-2 часа |
4-12 часов |
18-24 часа |
|
Смешанный 50/50: |
30 мин. |
2-8 часов |
24 часа |
|
Смешанный 40/60: |
30 мин. |
2-8 часов |
24 часа |
|
Смешанный 30/70: |
30 мин. |
2-8 часов |
24 часа |
|
Смешанный аналог инсулина: |
10-20 мин. |
1-3 часа |
18-24 часа |
|
Аналоги инсулина длительного действия: |
1-2 часа |
без пиков |
24 часа |
При проведении лечения детей и подростков рекомендованы к использованию только человеческие генно-инженерные инсулины или инсулиновые аналоги. При этом используют препараты ультракороткого, короткого действия, средней продолжительности. Смеси инсулинов разной длительности действия в детской практике практически не используют в связи с тем, что рекомендованное соотношение препаратов составляет 50:50, тогда как большинство микст-форм имеют соотношение 30 : 70.
Следует отметить, что в ряде странах мира производятся препараты инсулинов животного происхождения довольно высокого качества, сравнимые с аналоговыми (уровень доказательности А).
В табл. 7.4 представлены инсулины отечественного производства, назначаемые взрослым пациентам.
|
Инсулины по длительности действия |
Препараты, производитель |
Время начала действия |
Время пика действия, ч |
Длительность действия, ч |
|
Короткого действия |
Фармасулин Н, «Фармак» |
30 мин |
1-3 |
5-7 |
|
Хумодар Р 100, «Индар» |
30 мин |
1-2 |
5-8 |
|
|
Хумодар Р 100 Р, «Индар» |
30 мин |
1-2 |
5-7 |
|
|
Монодар, «Индар» |
30 мин |
1-2 |
5-6 |
|
|
Средней продолжительности |
Фармасулин HNP, «Фармак» |
1 час |
2-8 |
18-20 |
|
Хумодар Б 100, «Индар» |
1 час |
4-6 |
12-20 |
|
|
Хумодар Б 100 Р, «Индар» |
1 час |
4-6 |
12-20 |
|
|
Готовые смеси-комбинации инсулинов короткой и средней продолжи тельности действия |
Фармасулин Н 30/70, «Фармак» |
30 мин |
1-8,5 |
14-15 |
|
Хумодар К 25 100, «Индар» |
30-45 мин |
1,5-3 |
12-18 |
|
|
Хумодар К 25 100 Р, «Индар» |
30-45 мин |
1,5-3 |
12-18 |
На современном этапе наибольшее предпочтение отдается препаратам ультракороткого действия и аналогам инсулинов длительного действия. К преимуществам ультракоротких инсулинов (рис. 7.5) относят:
- быстрое начало и пик действия, параллельные уровню посталиментарной гипергликемии, в связи с чем могут использоваться непосредственно перед приемом пищи;
- меньшую продолжительность действия, что дает возможность избегать частых «перекусов»;
- возможность использования сразу после еды (что полезно для детей раннего возраста при вариабельности употребления пищи);
- более быстрый эффект в случае гипергликемии, протекаюшей с кетозом и без него;
- эффективность использования при помповом введении препарата.
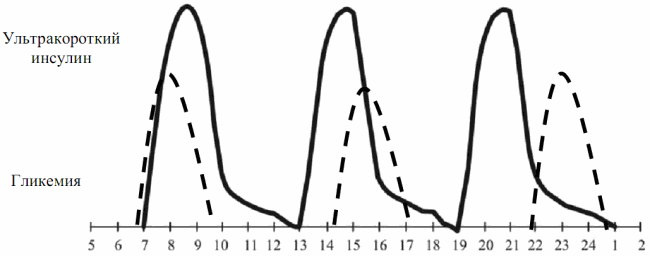
Рис. 7.5. Обеспечение контроля гликемии препаратами ультракороткого инсулина
Внутривенное введение инсулина применяют в случае выведения из диабетического кетоацидоза и при проведении хирургических вмешательств.
Беспиковые аналоговые инсулины длительного действия (рис. 7.6) характеризуются:
- отсутствием необходимости дополнительных инъекций короткого инсулина в ранние утренние часы у большинства пациентов с феноменом «утренней зари»;
- достоверным снижением утренней гликемии;
- уменьшением лабильности углеводного обмена;
- более высокой стоимостью, ограничивающей их использование.
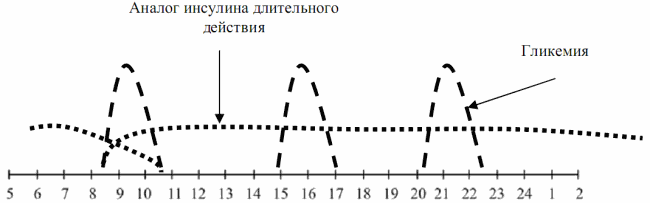
Рис. 7.6. Обеспечение контроля гликемии препаратами аналогов длительного действия
Смешанные инсулины достаточно популярны в некоторых странах мира у подростков и взрослых, поскольку позволяют осуществлять лечение по схеме «две инъекции в день» в случаях проблем с организацией инъекционного процесса в течение дня. Однако у детей они используются редко в связи со склонностью к лабильному течению заболевания и отсутствием доказательств безопасности и эффективности их применения.
Проведенные испытания в отношении эффективности ингаляционного пути введения инсулина у лиц старше 12 лет (Skyler J. S, Weinstock R. S, Raskin P., 2005) ожидаемых результатов не показали в связи с возможностью использования препарата только в болюсном режиме, громоздкостью установок и неизвестными долговременными эффектами на легочную ткань.
Выбор режима инсулинотерапии зависит от многих факторов, таких как:
- тип и длительность сахарного диабета;
- возраст, масса тела;
- особенности образа жизни и питания;
- состояние метаболического контроля;
- возможности проведения индивидуального мониторинга и проведения инъекций;
- наличие или отсутствие интеркуррентных заболеваний;
- индивидуальные предпочтения.
Имеющиеся общие рекомендации по режиму инсулинотерапии являются только основой для разработки индивидуального режима, который должен учитывать физиологические потребности и сложившийся образ жизни каждого пациента.
Тем не менее, выбор схемы инсулинотерапии определяется не столько желанием врача или семьи больного, сколько оптимальным профилем введения инсулина, который обеспечивает компенсацию углеводного обмена в данном конкретном случае.
Наиболее часто используемые схемы инсулинотерапии:
- две инъекции в день смешанного (короткого и пролонгированного инсулина) препарата;
- три инъекции в день с использованием смеси инсулинов перед завтраком и ужином и коротких перед обедом;
- базисно-болюсный режим.
Помимо этого могут применяться нестандартные режимы инсулинотерапии, часто используемые у пациентов с индивидуальными особенностями при частично сохраненной импульсной активности β-клеток.
При разработке режимов инсулинотерапии необходимо соблюдать следующие правила:
- Комбинировать препараты пролонгированного действия с короткодействующими, что позволяет моделировать базальную инсулинемию и посталиментарную гиперинсулинемию (роль базальной инсулинемии играют пролонгированные препараты инсулина; короткодействующие препараты инсулина, введенные за 30-60 мин. до очередного приема пищи, имитируют посталиментарную гиперинсулинемию).
- Вводить суточную дозу инсулина в несколько приемов.
- Определить минимальную суточную дозу инсулина, которая позволяет максимально снизить уровень гликемии у данного больного.
Так, наиболее распространенная в использовании интенсифицированная (базисно-болюсная) схема представляет собой применение короткого инсулина перед каждым основным приемом пищи и пролонгированного инсулина от одного до трех раз в сутки (рис. 7.7).
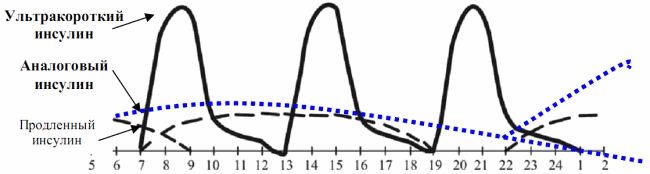
Рис. 7.7.
Базисно-болюсная схема инсулинотерапии
В связи с полным прекращением действия β-клеток через 5 лет от начала заболевания потребность в инсулине обычно повышается до 1 ЕД/кг массы. В период полового созревания в связи с особенностями гормонального фона она вырастает еще больше, достигая у многих подростков 1,5 ЕД/кг, иногда 2 ЕД/кг. В последующем у взрослых доза инсулина снижается в среднем до 1 ЕД/кг. Длительная декомпенсация заболевания также ведет к повышению потребности в инсулине, которая может достигать 2-3 ЕД/кг с последующим снижением дозы вплоть до исходной.
Ориентировочная суточная потребность в инсулине:
- на первом году заболевания – 0,25-0,50 ЕД/кг в сутки;
- на втором году болезни – 0,6-0,8 ЕД/кг в сутки;
- в период препубертата – 0,6-1,0 ЕД/кг в сутки;
- в период пубертата – 1,0-2,0 ЕД/кг в сутки.
В детском возрасте потребность в инсулине, рассчитанная на 1 кг массы тела, нередко выше, чем у взрослых, что обусловлено:
- большей скоростью аутоиммунных процессов;
- активным ростом ребенка;
- высоким уровнем контринсулярных гормонов в период полового созревания.
Соотношение пролонгированного и короткого инсулина сдвигается: от преобладания пролонгированного инсулина у детей первых лет жизни к преобладанию короткого инсулина у подростков и взрослых.
Как и у взрослых, у детей на одну хлебную единицу (ХЕ) в утренние часы требуется несколько больше инсулина, чем в обед и в ужин.
Критерии эффективности инсулинотерапии по ISPAD:
- уровень глюкозы в крови натощак или перед едой – 4,0-7,0 ммоль/л;
- уровень глюкозы после приема пищи – 5,0-11,0 ммоль/л;
- отсутствие тяжелых гипогликемий, допускается наличие отдельных легких гипогликемий;
- содержание HbA1c менее 7,6%.
Инсулинотерапия у пациентов с сахарным диабетом 2-го типа (СД 2) может использоваться:
- транзиторно в специальных ситуациях;
- при неадекватном гликемическом контроле с использованием пероральных сахароснижающих средств;
- при длительном сочетании СД 2 с полным снижением функции β-клеток.
К специальным ситуациям относят дебют сахарного диабета 2-го типа, хирургические вмешательства и интеркуррентные заболевания, когда уровень глюкозы крови значительно превышает норму.
В настоящее время FINFAT разработаны следующие подходы к проведению инсулинотерапии:
- назначение малых доз инсулина средней продолжительности действия перед сном (2-4 ЕД или 10 %) с последующим контролем уровня гликемии;
- интервал для наблюдения за действием препарата составляет 2-3 дня;
- повторная инъекция назначается в том случае, когда уровень глюкозы в крови в дневное время сохраняется выше целевых значений;
- пациент должен быть обучен распознаванию гипогликемических состояний и их коррекции, также как и пациент при сахарном диабете 1-го типа;
- коррекция дозы инсулина проводится обычно 1-2 раза в неделю;
- режим инсулинотерапии обычно более гибкий, чем при сахарном диабете 1-го типа.
Время введения инсулина
Введение инсулина обычно соответствует основным приемам пищи. С учетом типа инсулина и начала его действия необходимо учитывать следующие рекомендации:
- Растворимый инсулин (короткого действия, fast) всасывается быстро, но прием пищи возможен лишь через 30 минут после введения препарата. Аналоги инсулина ультракороткого действия могут вводиться за 15 минут до еды или сразу перед едой.
- В некоторых случаях, когда нет уверенности в количестве пищи, которая будет принята (например, у маленьких детей), препарат может быть введен сразу после еды.
- Инсулины средней продолжительности действия и длительные могут назначаться в любое время вне связи с приемом пищи.
Требования к технике введения инсулина:
- инсулин должен вводиться в подкожно-жировую клетчатку;
- у очень худых лиц применяют дополнительный «захват тканей» или иглы более короткой длины;
- направление иглы у очень худых пациентов – 45°, при ожирении – 90°;
- использование инсулина комнатной температуры уменьшает болезненность при проведении инъекции;
- протирание места инъекции спиртом не является обязательным.
Как правильно проводить инъекции инсулина
Медицинские работники и некоторые больные диабетом в полной мере осознают важность правильной методики инъекции для эффективного действия инсулина. Но в большинстве своем врачи и многие больные сахарным диабетом не осознают всей важности правильной техники инъекций инсулина.
За последние годы основное внимание при лечении диабета уделяют подбору адекватных доз инсулина, кратности их введения и периодическому измерению концентрации глюкозы в крови. Не меньшую роль для максимально полной компенсации диабета играет правильная техника инъекции. Неправильный выбор участка кожи для укола и неверная техника инъекции могут привести к изменению скорости всасывания инсулина в кровоток из места его введения и стать, таким образом, причиной разобщения по времени между максимальной концентрацией глюкозы и максимальным эффектом инсулина. Подобный дисбаланс может сопровождаться как гипергликемией, так и гипогликемией.
Для обеспечения полного всасывания инсулина инъекции должны быть сделаны в подкожно-жировую клетчатку, а не в кожу или мышцу.
Во время внутримышечного введения ускоряется всасывание инсулина, что провоцирует развитие гипогликемии, внутрикожное попадание приводит к вытеканию инсулина и/или к боли.
С этой точки зрения, именно укол с предварительным формированием кожной складки рекомендован специалистами в области диабета. С помощью КТ и УЗИ было доказано, что формирование кожной складки перед уколом достоверно увеличивает вероятность п/к введения инсулина.
Кожную складку необходимо формировать двумя пальцами (большим и указательным). Складка должна сохраняться в течение того времени, пока вводится инсулин. Перед тем, как вынимать иглу, складка должна сохраняться еще в течение 5-10 сек. с момента окончания введения инсулина.
Всегда необходимо учитывать ключевые факторы, определяющие скорость всасывания инсулина:
- места инъекций и их соответствие времени введения инсулина;
- толщина подкожно-жировой клетчатки в месте инъекции;
- техника инъекции;
- длина иглы;
- наличие липодистрофий;
- режим физической нагрузки;
- температура тела.
Основные места для проведения инъекций:
- живот (самая высокая скорость всасывания) рекомендуют для инъекций инсулинов короткого или смешанного действия;
- ягодицы (скорость всасывания достаточно низкая) подходят для введения инсулинов среднего и продолжительного действия;
- бедра (скорость всасывания низкая и предсказуемая) рекомендуют для введения инсулинов среднего и продолжительного действия;
- руки (средняя скорость всасывания) используют как дополнительное место для инъекций при ротации.
Для достоверного прогнозирования воздействия дозы инсулина необходимо проводить инъекции в одну и ту же зону и в одно и то же время (рис. 7.8). Следует обращать внимание пациентов на то, что во время физической нагрузки мышц той зоны, куда только что был введен инсулин, скорость всасывания увеличивается в 7 раз.
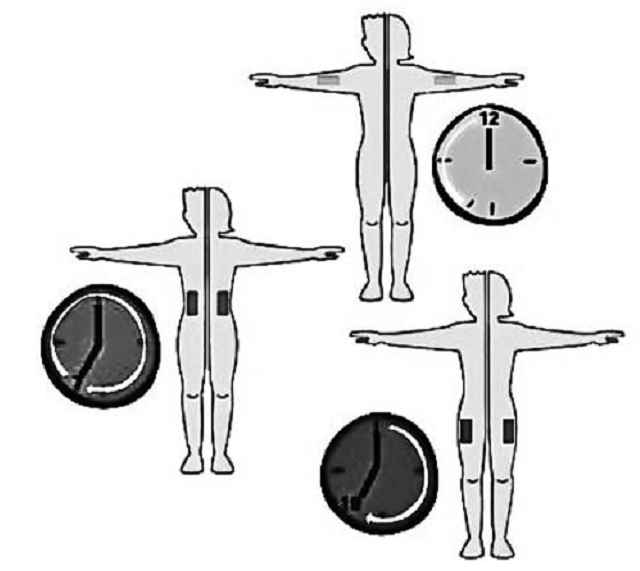
Рис. 7.8. Пример распорядка введения инсулина
Толщина подкожно-жировой ткани
Компьютерная томография выявила существенные различия толщины подкожно-жирового слоя в областях проведения инъекций в зависимости от пола, в популяции и у одного человека.
Было подтверждено, что толщина подкожно-жировой ткани является основным фактором риска внутримышечного введения инсулина в местах, где она тонкая. При использовании взрослыми иглы длиной 12,7 мм возможно ее проникновение через подкожно-жировой слой в мышцу. Риск повышается в местах со слаборазвитым слоем подкожно-жировой клетчатки, особенно если инъекция выполняется перпендикулярно коже без формирования кожной складки. У детей и худых взрослых даже игла длиной 8 мм может проникнуть очень глубоко при введении без формирования кожной складки.
Правильное формирование кожной складки
Для правильного формирования кожной складки используют большой и указательный/средний пальцы. При этом поднимаются кожа и подкожно-жировой слой, оставляя мышцу нетронутой (рис. 7.9).
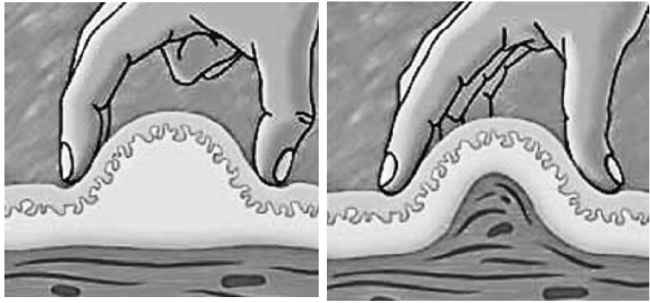
Рис. 7.9. Правильное формирование кожной складки
Складку следует удерживать в течение всего времени введения до тех пор, пока игла не будет извлечена. Если отпустить складку раньше, игла может пройти в мышечный слой.
Введение иглы под углом к коже также уменьшает риск попадания инсулина в мышцу. В ряде случаев, когда риск внутримышечного введения чрезвычайно высок, рекомендуется техника введения инсулина в кожную складку под углом в 45° (рис. 7.10).
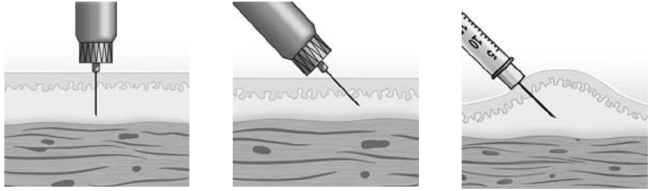
Рис. 7.10. Техника введения инсулина в кожную складку под углом в 45°
Средства введения инсулина
Инсулин вводят с использованием приспособлений, специально для этого адаптированных, таких как инсулиновые шприцы, шприц-ручки, постоянные катетеры, безигольные инжекторы, инсулиновые помпы.
В настоящее время рекомендуется использование растворов, содержащих единую концентрацию инсулина – 100 МЕ/мл, что способствует универсализации дозирования препарата и использования единых приспособлений для его введения.
|
Модификация шприца |
Клиническое применение |
|
Инсулиновый шприц 1 мл U-100, с иглой 29 G (0,33 х 12,7 мм) |
Использовать для введения инсулина концентрации U 100, для доз до 100 ЕД за одно введение. Рекомендован для взрослых с избыточной и нормальной массой тела для инъекций в кожную складку под углом 45°. Шаг – 2 ЕД. |
|
Инсулиновый шприц 1 мл U-100, с иглой 30 G (0,3 х 8 мм) |
Использовать для введения инсулина концентрации U 100. Рекомендован для взрослых и детей с нормальной массой тела, делающих инъекцию в кожную складку. Шаг – 2 ЕД. |
|
Инсулиновый шприц 0,5 мл U-100, с иглой 29 G (0,33 х 12,7 мм) |
Использовать для введения инсулина концентрации U 100, для доз до 50 ЕД за одно введение. Рекомендован для взрослых с избыточной и нормальной массой тела, делающих инъекцию в кожную складку под углом 45°. Шаг – 1 ЕД. |
|
Инсулиновый шприц 0,5 мл U-100, с иглой 30 G (0,3 х 8 мм) |
Использовать для введения инсулина концентрации U 100, для доз до 50 ЕД за одно введение. Рекомендован для взрослых и детей с нормальной массой тела, делающих инъекцию в кожную складку. Шаг – 1 ЕД. |
|
Инсулиновый шприц 0,3 мл U-100, с иглой 30 G (0,3 х 8 мм) |
Использовать для введения инсулина концентрации U 100. Рекомендован для детей и взрослых, получающих инсулин в дозировках кратных 0,5 ЕД (маленькие дети, вновь выявленные больные, больные сахарным диабетом с хронической почечной недостаточностью, беременные). Шаг – 0,5 ЕД. |
В последние годы заслуженной популярностью у пациентов всех возрастных групп стали пользоваться шприц-ручки (рис. 7.11, 7.12).

Рис. 7.11. Варианты шприц-ручек для введения инсулина

Рис. 7.12. Совместимость одноразовых игл BD Mикро-Файн™ Плюс с известными шприц-ручками
К преимуществам шприц-ручек относят:
- простоту в обращении;
- возможность точного набора дозы препарата (даже минимальных доз);
- возможность контроля введения (по щелчку);
- психологический комфорт пациентов, особенно детского и подросткового возраста, что положительно отражается на качестве их жизни.
Автоматические инжекторы эффективны для использования у детей со «страхом иглы», поскольку игла в этих устройствах скрыта и прокол осуществляется стремительно.
Джет-инжекторы с п/к введением инсулина под высоким давлением используются в случаях иглофобии, а эффективность их использования в отношении метаболического контроля за сахарным диабетом сравнима с другими устройствами. Тем не менее, существует проблема неконтролируемой вариабельной глубины инъекций с возможным возникновением синяков и болезненности.
|
Пациент, возраст |
Телосложение |
Толщина иглы, мм |
|
Дети (5-12 лет) |
Все |
5 |
|
Подростки (12-18 лет) |
Худые |
5 |
|
Нормальные |
8 |
|
|
С ожирением |
12 |
|
|
Мужчины взрослые |
Худые |
5 |
|
Нормальные |
8 |
|
|
С ожирением |
12,7 |
|
|
Женщины взрослые |
Худые |
5 |
|
Нормальные |
8 |
|
|
С ожирением |
12,7 |
Риск повторного использования одноразовых игл
Специальные иглы, применяемые в тандеме со шприц-ручками, проходят современную систему заточки и обрабатывание силиконовой смазкой с использованием современных технологий. Однако использовать одну и ту же иглу для многократного введения инсулина нельзя. Со временем иглы тупятся и приобретают форму крючка (рис. 7.13), из-за чего при вынимании иглы образуются микротравмы и микрокровоизлияния. Все это может привести к изменениям подкожно-жировой клетчатки и развитию липодистрофии. Поэтому иглу необходимо менять после каждой инъекции.

Рис. 7.13. Изменения инсулиновых игл в зависимости от кратности инъекций
В последние годы получили распространение инсулиновые помпы (рис. 7.14).

Рис. 7.14. Инсулиновая помпа Paradigm REAL-Time
Терапия с помощью инсулиновой помпы наиболее эффективна в настоящее время, так как способствует нормализации глюкозы крови, самочувствия, здоровья и отсрочке осложнений, связанных с диабетом.
Инсулиновая помпа – это современный надежный прибор размером с пейджер. Помпа обеспечивает введение инсулина в течение дня с минимальной базальной скоростью по 0,05/0,1 ЕД/ч. Самые последние модели инсулиновых помп – Paradigm и Paradigm REAL-Time – имеют самые совершенные функции: калькулятор болюса и измерение уровня гликемии в реальном времени. Калькулятор болюса рассчитывает необходимую болюсную дозу в данный момент с учетом активного, или «остаточного», инсулина, с учетом фактора чувствительности к инсулину и коэффициента чувствительности на еду.
Инсулиновая помпа Paradigm REAL-Time дополнена сенсором, который показывает уровень глюкозы в реальном времени, что позволяет предупредить критичные повышения или понижения уровня гликемии, а также отображает тенденцию и скорость движения уровня глюкозы. Также инсулиновая помпа Paradigm REAL-Time способна самостоятельно предупреждать состояния гипогликемии у пациентов, что достигается автоматическим отключением введения инсулина на два часа при достижении уровня глюкозы 5 ммоль и ниже (задается индивидуально).
Показания к помповой терапии:
- частые гипогликемические состояния;
- скрытые гипогликемии;
- симптом «утренней зари»;
- беременность;
- неконтролируемый диабет;
- высокая чувствительность к инсулину;
- плохой гликемический контроль (HbA1c > 7%);
- желание пациента.
К преимуществам помп относятся малые размеры и вес, программируемый тип действия, доказанная рандомизируемыми исследованиями (А) эффективность в отношении оптимизации гликемического контроля как у взрослых пациентов, так и у детей. Кроме того, помпы весьма эффективны как для пациентов с оптимальным и неоптимальным метаболическим контролем, так и в случаях диабетического кетоциадоза.
Новая генерация инсулиновых помп – smart pumps – позволяет автоматически производить подсчет еды, необходимую корректирующую дозу препарата, инсулин/углеводное соотношение, учитывать влияние дополнительных факторов. Использование помпы может быть опасным в случаях малых депо подкожного инсулина и внезапного повышения концентрации кетонов при прекращении введения инсулина. Однако большинство устройств снабжены автоматическим определителем концентрации кетонов (по β-гидроксибутирату) и автоматически останавливаются, когда их концентрация превышает 1,5 ммоль/л, но не в случаях диабетического кетоциадоза. Аналогичная ситуация имеет место у взрослых.
Акцентируем внимание на том, что использование всех технических приспособлений для проведения инсулинотерапии требует специального обучения пациентов и их родителей в условиях стационара.
Осложнения инсулинотерапии
При проведении лечения препаратами инсулина, как, впрочем, и при использовании любых других методов лечения, может возникать ряд осложнений. К ним относят:
- передозировку препаратами инсулина (в том числе и преднамеренную);
- локальную гиперчувствительность, требующую замены препарата инсулина; если действительно имеет место аллергическая реакция к инсулину, необходимо проведение десенсибилизирующей терапии по соответствующим протоколам с добавлением малых доз кортикостероидов;
- болезненные инъекции, являющиеся частой проблемой в детском возрасте; при этом требуется проверить остроту иглы, угол и глубину введения препарата во избежание его внутримышечного использования;
- синяки и кровотечения в местах инъекций, которые возникают в случае внутримышечного введения препарата;
- инсулиновые отеки, возникающие у пациентов с выраженной декомпенсацией заболевания на фоне резкого снижения гликемии, что связано с задержкой натрия и воды вследствие компенсаторного повышения уровня антидиуретических гормонов (АДГ) в ответ на длительный осмотический диурез;
- липодистрофии − изменения кожи и подкожно-жировой клетчатки в виде участков атрофии или гипертрофии в местах введения инсулина (рис. 7.15).
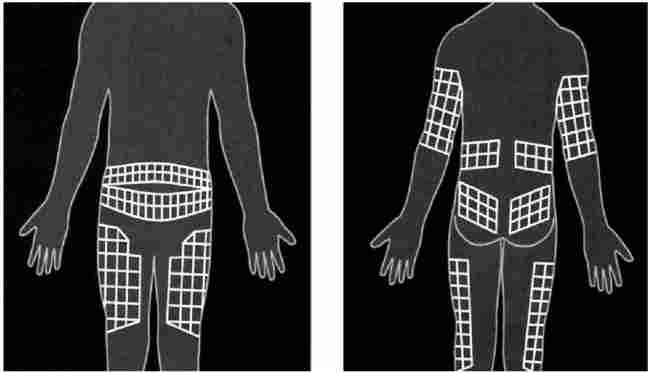
Рис. 7.15. Наиболее вероятные места локализации липодистрофий
В детском возрасте чаще встречаются гипертрофические липодистрофии (липогипертрофии), которые наблюдаются почти у четверти больных сахарным диабетом 1-го типа.
Считается, что к развитию липодистрофий приводят такие факторы как кислый рН инсулиновых препаратов, нарушение техники инъекций, а также иммунопатологические местные реакции, особенно у больных, получающих малоочищенные инсулины.
Гипертрофические липодистрофии (рис. 7.16) характеризуются припухлостью и твердостью мягких тканей, безболезненных при пальпации. Полагают, что возникновение липогипертрофий является результатом липогенеза подкожно-жировой клетчатки вследствие прямого действия инсулина. Липогипертрофии приводят к нарушению всасывания инсулина.
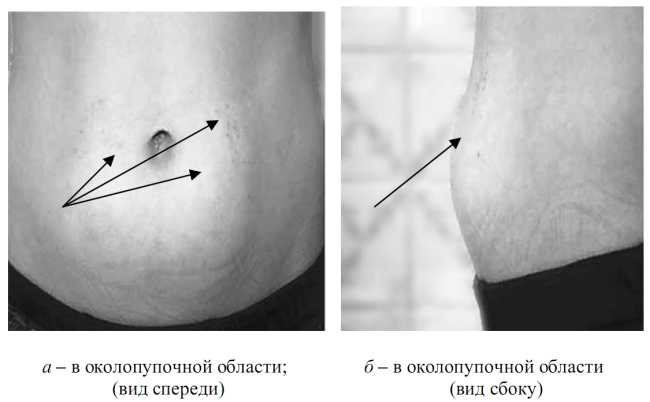
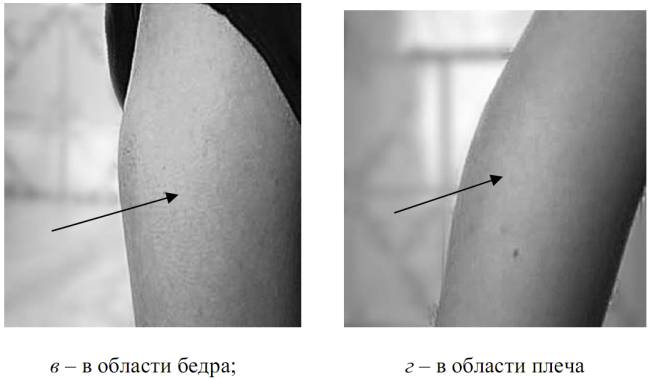
Рис. 7.16. Гипертрофические липодистрофии (липогипертрофии)
Липоатрофии (рис. 7.17) характеризуются полным отсутствием жира в подкожно-жировом слое около мест инъекций, со временем углубления постепенно увеличиваются. С момента широкого использования в клинической практике высокоочищенных инсулинов липоатрофии являются малораспространенными. Однако в последние годы в связи с разработкой и внедрением современных аналоговых препаратов липоатрофии вновь стали чаще регистрироваться.
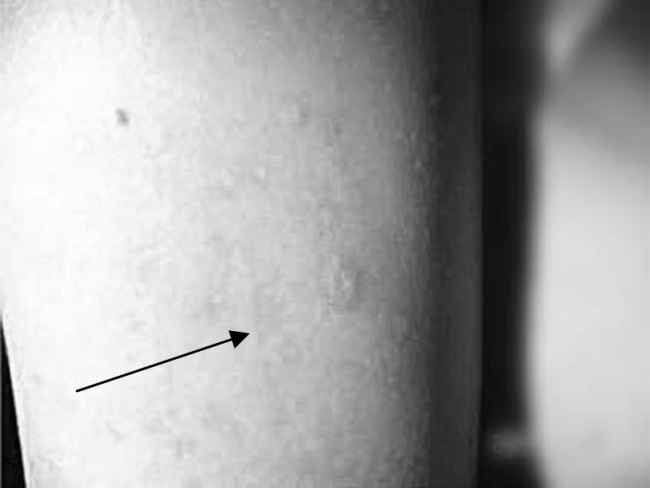
Рис. 7.17. Липоатрофии в области плеча
И гипертрофические и атрофические липодистрофии плохо васкуляризируются, поэтому препятствуют полноценному всасыванию инсулинов.
Потеря чувствительности в местах липодистрофий делает безболезненным введение инсулина, что, с одной стороны, нравится детям, но, с другой стороны, нарушение всасывания гормона приводит к декомпенсации заболевания и утрате контроля над ним.
Лечение липодистрофий заключается в чередовании мест инъекций инсулина и физиотерапевтическом лечении (лазеротерапия на места липодистрофий, парафиновые аппликации на места липодистрофий; ультразвуковая терапия, ультразвуковая терапия поочередно с лазеротерапией; гипербарическая оксигенация).
Из монографии «Сахарный диабет: от ребенка до взрослого»
Сенаторова А.С., Караченцев Ю.И., Кравчун Н.А., Казаков А.В., Рига Е.А., Макеева Н.И., Чайченко Т.В.
ГУ «Институт проблем эндокринной патологии им. В.Я. Данилевского АМН Украины»
Харьковский национальный медицинский университет
Харьковская медицинская академия последипломного образования МЗ Украины
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


