
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
- Новини 26.10.2021 Аппаратура для УЗИ: применение, принципы работы, разновидности
- Новини 23.10.2021 Интимная пластика после родов: когда необходима операция
Медикаментозное лечение ожирения больных с метаболическим синдромом
Чрезвычайно высокая распространенность ожирения и метаболического синдрома (МС) общеизвестна. Необходимость раннего начала терапии и более тщательного подбора медикаментозного лечения МС отмечена в большом количестве публикаций. В качестве патогенетической терапии было предложено множество средств для снижения массы тела (МТ), т.к. общеизвестен факт превалирующей роли ожирения в патогенезе МС.
По тем или иным причинам многие препараты не нашли широкого применения в практике. В статье приведены данные многолетнего опыта применения одного из эффективных препаратов для снижения МТ — орлистата (Ксеникала®). На собственном материале было показано позитивное влияние снижения МТ при использовании орлистата на углеводный и липидный обмены, суточный профиль АД и перфузию головного мозга. Доказана целесообразность использования орлистата для лечения пациентов с МС, для снижения риска развития сердечно-сосудистых осложнений у этой категории пациентов.
Частота сердечно-сосудистых заболеваний (ССЗ) возрастает в зависимости от избытка массы тела (МТ) у мужчин и женщин [1]. Риск сердечнососудистых осложнений (ССО) начинает повышаться уже при МТ на уровне верхней границы нормы и прогрессивно растет по мере ее увеличения. Более того, сам по себе процесс увеличения МТ в возрасте также является фактором сердечнососудистого риска. Результаты Фремингемского исследования показали, что степень увеличения МТ после 25 лет прямо коррелировала с риском ССО. Снижение индекса МТ (ИМТ) уменьшало степень этого риска. Гипокалорийная диета и повышение физической активности являются основой лечения ожирения, однако часто только при их применении трудно достичь желаемого результата. Еще труднее, снизив вес, удерживать его на достигнутом уровне. Поэтому в ряде случаев необходимо к немедикаментозным методам лечения ожирения добавлять лекарственные препараты, снижающие вес.
Показаниями к их применению являются:
- ИМТ > 30 кг/м2 или
- ИМТ > 27 кг/м2, в сочетании с абдоминальным ожирением, наследственной предрасположенностью к СД 2 типа (СД-2) и наличием факторов риска (ФР) ССО — дислипидемии (ДЛП), артериальной гипертонии (АГ) и СД-2.
Лекарственные средства для снижения веса подразделяются на группы препаратов центрального, периферического и различного действия (гормон роста, андрогены).
Большинство препаратов центрального действия, снижающих аппетит, было снято с производства из-за побочных эффектов, нередко приводящих к гибели больных, наиболее грозным из которых являлось развитие тяжелой легочной гипертонии (ЛГ). Эти эффекты возникали, как правило, вследствие системного действия данных лекарственных средств.
История создания и внедрения в лечебную практику «аноректиков» — препаратов для уменьшения аппетита, драматична [2]. Первым препаратом, предложенным в 1938 г для снижения веса, был хорошо известный всем амфетамин. Но вскоре появились сообщения о неблагоприятных побочных эффектах при его назначении — выраженное стимулирующее действие на центральную нервную систему (ЦНС), а также «синдром отмены», развивающийся при прекращении приема. В настоящее время амфетамин для лечения ожирения не используется.
Следующая черная полоса в истории применения аноректиков связана с эпидемией первичной ЛГ (ПЛГ), разразившейся в середине 60-х годов в Швейцарии, Германии и Австрии. Она возникла после распространения аминорекса фумората. ПЛГ относится к наиболее тяжелым ССЗ. Средняя продолжительность жизни при этой патологии составляет 5-7 лет. В основе болезни лежат тяжелые необратимые поражения сосудов легких, к которым относятся выраженный фиброз интимы, плексиформные изменения, тромботические поражения мелких легочных артерий. К счастью, эта патология встречается крайне редко — в среднем в 1-2 случаях на 1 млн. населения, но при назначении некоторых аноректиков частота ее увеличивается многократно. В работах группы американских пульмонологов было показано, что частота развития ПЛГ при применении аминорекса возрастает в ~ 30 раз.
В 80-90гг. препаратами выбора для лечения ожирения служили фенфлюрамины, влияющие на обмен серотонина, а также фентермин, обладающий стимулирующим действием на симпатическую нервную систему (СНС) [3]. Популярностью также пользовалась комбинация фентермина и фенфлюрамина — так называемый препарат «фен-фен». Эти лекарственные средства привлекали своей высокой эффективностью и хорошей, по сравнению с предшественниками, переносимостью. Но, к сожалению, стимулирующее влияние на СНС, а также «токсический» эффект высоких концентраций серотонина приводили к дисфункции и повреждению сосудистого эндотелия, в первую очередь в легких, что сопровождалось повышением сосудистого тонуса и развитием ЛГ. Фенфлюрамины в ряде случаев способствовали возникновению патологии клапанного аппарата сердца [4]. В некоторых исследованиях было показано, что фенфлюрамины могут повышать системное давление и увеличивать частоту сердечных сокращений (ЧСС), что неблагоприятно для пациентов с АГ [5]. Частота развития Л Г при назначении фенфлюраминов была значительно ниже, чем при использовании аминорекса и, как правило, побочные эффекты развивались после 6 месяцев постоянного применения. Однако обеспокоенная медицинская общественность обратилась к контролирующим органам с просьбой запретить продажу этих лекарств; с 1997г в ряде стран их распространение прекращено, а в других срок применения ограничен 3-6 месяцами.
В последние годы на фармацевтическом рынке появился новый препарат центрального действия для лечения ожирения — сибутрамин. Он отличается от своих предшественников фенфлюраминов тем, что в меньшей степени влияет на дофаминовый обмен и не действует на холинергические процессы [6]. Прием сибутрамина приводит к быстрому появлению чувства насыщения и снижению аппетита. В результате лечения сибутрамином снижается МТ и масса висцерального жира, о чем свидетельствуют исследования с применением компьютерной томографии. Снижение веса улучшенает показатели углеводного и липидного обменов. Однако назначение сибутрамина лицам, не страдающим АГ, может сопровождаться повышением артериального давления (АД) на 3-4 мм рт.ст. и ЧСС. Это его свойство увеличивать АД и ЧСС ограничивает использование сибутрамина у пациентов с АГ, метаболическим синдромом (МС) и повышенным риском ССЗ.
Предыдущие неудачи и желание иметь как можно более безопасный и эффективный препарат заставили ученых выбрать другой путь — создать препарат не центрального, а местного действия. Усилия фармацевтов были направлены на получение лекарства, действие которого носило бы локальный характер. Таким препаратом является орлистат (Ксеникал®, Ф.Хоффманн-Ля Рош Лтд., Швейцария) — лекарственное средство для лечения ожирения с несистемным эффектом [7]. Он тормозит всасывание жиров пищи в желудочно-кишечном тракте (ЖКТ) вследствие ингибирования желудочно-кишечных липаз — ключевых ферментов, участвующих в гидролизе триглицеридов (ТГ) пищи, высвобождении жирных кислот (ЖК) и моноглицеридов. Это приводит к тому, что ~ 30% ТГ пищи не переваривается и не всасывается, что позволяет создать дополнительный дефицит калорий по сравнению с применением только гипокалорийной диеты [8]. После отмены орлистата (Ксеникала®) активность липаз быстро восстанавливается. Орлистат не действует на другие ферменты ЖКТ, даже когда дозы препарата превышают в 100 раз среднетерапевтические [9]. Орлистат не влияет на всасывание углеводов, белков и фосфолипидов. Препарат оказывает собственный дополнительный гиполипидемический эффект, поскольку, подавляя липазы ЖКТ, он снижает количество свободных ЖК (СЖК) в кишечнике и тем самым уменьшает растворимость и всасывание холестерина (ХС). Орлистат уменьшает уровень ХС в большей степени, чем этого можно было ожидать только из-за уменьшения МТ на фоне его применения.
Эффективность и безопасность орлистата были изучены более чем в 100 крупных, длительных, двойных слепых, плацебоконтролируемых, клинических исследованиях. В общей сложности в них участвовали ~ 30 тыс. больных с ожирением. Длительность терапии в исследованиях составила от 6 месяцев до 4 лет. Во всех исследованиях имело место уменьшение МТ в ответ на назначение орлистата, при этом первые 3 месяца вес снижался в среднем на 5%, а к концу года на 14,2%. В 4 исследованиях, длительностью 2 года, изучалось действие орлистата (Ксеникала®) при длительном применении. У пациентов, принимавших орлистат, снижение МТ было более выраженным, чем в группе контроля. Эффективность орлистата сохранялась на протяжении 2 лет. У больных с исходно повышенным уровнем ХС липопротеинов низкой плотности (ЛНП), лечившихся орлистатом, концентрация его уменьшалась на 10,9%, в то время как у получавших плацебо только на 2,4%. Нормализация этого показателя в группе активного лечения наблюдалась в 2 раза чаще, чем в группе плацебо. К концу исследования концентрация ХС ЛНП в группе плацебо вернулась к исходной, а в группе Ксеникала® его уровень оставался ниже начальных значений [10].
Уменьшению МТ при лечении орлистатом сопутствовало снижение систолического (САД) и диастолического АД (ДАД). У больных с ожирением с исходным ДАД > 90 мм рт.ст. на фоне приема орлистата оно снизилось на 7,9 мм рт.ст. к концу первого года, в то время как на плацебо снижение ДАД составило < 5,5 мм рт.ст. При назначении орлистата САД снижалось на 10,9 мм рт.ст., при приеме плацебо только на 5,1 мм рт.ст.
Терапия орлистатом согласно результатам длительных исследований способствовала уменьшению содержания инсулина в крови. К концу первого года лечения разница с группой плацебо составляла — 19,7 пмоль/л; концу второго года была еще более выраженной — 30 пмоль/л.
В США исследовали влияние орлистата на МТ и состояние углеводного обмена у больных СД-2, принимавших препараты сульфанилмочевины. Результаты этого исследования показали, что орлистат достоверно снижает МТ у больных СД и ожирением [11]. На фоне терапии орлистатом заметно падал уровень гликемии натощак и уменьшалась концентрация гликированного гемоглобина. Одним из наиболее важных результатов исследования явилось то, что у больных, принимавших орлистат, снижалась потребность в препаратах сульфанилмочевины для компенсации СД. Анализ данных этого исследования показал, что среди пациентов с нормальной толерантностью к глюкозе на фоне приема орлистата в течение 2 лет не было отмечено ни одного нового случая СД-2, в то время как в группе плацебо СД-2 развился в 1,5% случаев [12]. Нарушение толерантности к глюкозе определялось с течением времени в группе плацебо в 2 раза чаще, чем в группе орлистата.
Результаты проспективного, рандомизированного, плацебоконтролируемого исследования XEN-DOS (XENical in prevention of Diabetes in Obese Subjects) подтвердили эффективность и безопасность длительной терапии орлистатом у больных с ожирением. К концу четвертого года терапии содержание ХС ЛНП уменьшилось на 12,8%, а в группе плацебо на 5,1%. САД у пациентов, принимавших орлистат (Ксеникал®), снизилось в среднем на 4,9 мм рт.ст., ДАД — на 2,6 мм рт.ст., что было достоверно выше по сравнению с пациентами, использовавшими плацебо — 3,4 мм рт.ст. и 1,9 мм рт.ст. соответственно. Риск развития СД-2 сократился на 37% в группе орлистата по сравнению с группой плацебо [13].
В масштабном исследовании XXL (Xenical еХtraLarge study) — Primary Health Care Trial — оценивалась эффективность орлистата (Ксеникала®) у тучных пациентов с сопутствующими заболеваниями в рутинной амбулаторной практике. Впервые изучен опыт применения орлистата более чем у 15 тыс. пациентов. В состав участников были включены 11131 женщин и 4418 мужчин, проживающих в Германии (средний возраст 48 лет, средний индекс ИМТ — 34,7 кг/м2); 98% из них находились под наблюдением терапевта. Большинство пациентов имели ожирение в течение длительного времени (в среднем в течение 13,7 лет), в 80% случаев отмечены сопутствующие заболевания, связанные с ожирением. Длительность терапии Ксеникалом® составила в среднем 7,1 месяцев; МТ у мужчин и женщин в среднем уменьшилась на 10,8 кг или 10,7% от исходных показателей.
- 87% пациентов потеряли >5% МТ
- 51% пациентов потеряли >10% МТ
У пациентов, применявших орлистат в сочетании с увеличенной физической нагрузкой, отмечалось наибольшее снижение МТ (12,0% от исходных показателей). Ксеникал® оказывал положительное влияние на уровни липидов и глюкозы крови, а также на параметры АД.
Снижение содержания ХС ЛНП и повышение ХС липопротеидов высокой плотности (ЛВП) приводили к сокращению соотношения ЛНП/ЛВП в среднем на 15,4%. САД/ДАД снизилось в среднем на 8,7/5,1 мм рт.ст. соответственно. В целом наблюдалось уменьшение уровня глюкозы крови на 7,5%. У больных снижалось содержание общего ХС (ОХС) (14%), ХС ЛНП (14%) и ТГ (18%), при этом ХС ЛВП возрастал на 13%. Некоторые пациенты прекратили или сократили прием препаратов для лечения сопутствующих заболеваний: 31% пациентов при наличии ДЛП прекратили прием лекарств, понижающих уровень липидов, еще 15% сумели снизить дозу препаратов; 18% больных АГ перестали принимать антигипертензивные средств, а 8% снизили дозу; среди больных СД-2 16% прекратили прием препаратов и 18% сократили дозу. Результаты, полученные в ходе этого постмаркетингового исследования, где лечение осуществлялось в «домашних/амбулаторных» условиях, были сопоставимы с данными рандомизированных, плацебоконтролируемых исследований, которые проводились главным образом в клинических центрах. [13].
В различных исследованиях, проводимых в Австралии и Новой Зеландии (Ксеникал® и риск развития ССЗ у тучных пациентов, n=339) [14], Греции (ORLICARDIA — орлистат и уровень сердечно-сосудистого риска у пациентов с МС и СД-2, n=134) [15], Франции (орлистат и заболевания, сопутствующие ожирению, n=1004) [16, 17], значительно уменьшались многие индивидуальные ФР развития ССЗ: ОХС, ЛНП, глюкоза крови, гликированный гемоглобин, инсулин. Орлистат достоверно уменьшал потребность в сахароснижающих и антигипертензивных препаратах. В исследовании ORLICARDIA получены результаты, показывающие, что при приеме орлистата относительный риск возникновения сосудистых событий в течение 10 лет уменьшается в 2 раза.
Поскольку орлистат (Ксеникал®) ингибирует гидролиз и всасывание жиров в кишечнике, возможны их задержка и накопление в ЖКТ. Известна также роль чрезмерного количества жира в развитии рака прямой кишки. В связи с этим изучалось действие орлистата на пролиферацию клеток прямой кишки. Как показали результаты этого исследования, применение орлистата в терапевтической дозе 360 мг в сутки не влияло на пролиферацию клеток в биоптатах толстой кишки [18].
Способность орлистата частично блокировать всасывание жиров пищи послужила основанием для исследования влияния его длительного применения на концентрацию жирорастворимых витаминов. Результаты работы показали, что прием препарата в течение 2 лет сопровождался незначительным изменением концентрации жирорастворимых витаминов (A, D, E, K), и в среднем, их уровни сохранились в пределах нормальных значений. Было установлено, что снижение концентрации витаминов наблюдалось лишь в первый месяц лечения, в дальнейшем она сохранялась неизменной до конца исследования. У всех пациентов в исследовании отсутствовали симптомы гиповитаминоза [19].
Лабораторных и клинических признаков нарушений кальциевого обмена на фоне длительного применения орлистата также не наблюдалось, но было показано и в других клинических исследованиях. В нескольких работах отмечено, что усиление остеокласт-остеобластной активности или снижение костной массы при длительном назначении орлистата не происходило. На основании этих наблюдений был сделан вывод, что орлистат не оказывает влияния на обменные процессы в костной ткани.
Терапия орлистатом, как показал ряд исследований, не увеличивает риск образования камней в желчевыводящих путях. Эти нежелательные явления имели место лишь в 1% случаев как в группе орлистата, так и в группе плацебо. В ряде других исследований было установлено, что препарат не вызывал клинически значимых нарушений физиологических процессов в ЖКТ. Таким образом, орлистат является в настоящее время наиболее эффективным и безопасным средством медикаментозного лечения ожирения.
Клинические исследования орлистата выполнены на большом контингенте больных с участием > 30 тыс. человек, среди них были пациенты с СД-2, с нарушенной толерантностью к глюкозе и другими множественными факторами сердечно-сосудистого риска. В связи с этим можно с уверенностью говорить, что данное лекарственное средство является наиболее широко и тщательно изученным препаратом для лечения ожирения в настоящее время.
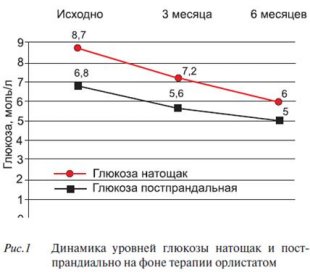
Опыт применения орлистата в Отделе системных гипертензий НИИ кардиологии имени А.Л. Мясникова РК НПК у больных с МС еще раз убеждает в его не только высокой эффективности, но и безопасности для лечения пациентов с высоким сердечно-сосудистым риском [20]. В результате приема орлистата на протяжении 24 недель МТ уменьшилась в среднем на 16 кг или более чем на 14%. Снижение МТ на фоне терапии орлистатом достоверно повышало чувствительность тканей к инсулину, улучшало показатели углеводного и липидного обменов. Уровень глюкозы плазмы натощак достоверно снизился на 26%, а постпрандиальная концентрация на 29% (рисунок 1). Уменьшилась гиперинсулинемия. Исходно повышенные базальные уровни инсулина и С-пептида снизились на 54% и 32% соответственно, а постпрандиальные на 38% и 7% соответственно.
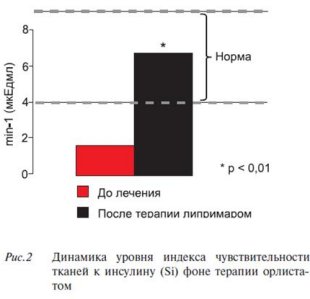
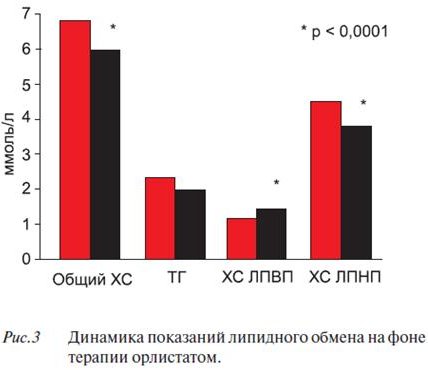
Результаты инсулинмодифицированного теста толерантности к глюкозе (Минимальная модель Bergman N) продемонстрировали достоверное повышение чувствительности тканей к инсулину на фоне приема орлистата (рисунок 2). Снижению МТ сопутствовало улучшение липидного профиля. Достоверно снизилось содержание ОХС на 12%, ХС ЛНП на 17,6%, повысился уровень ЛВП на 22%, и отмечалась тенденция к снижению ТГ (рисунок 3).
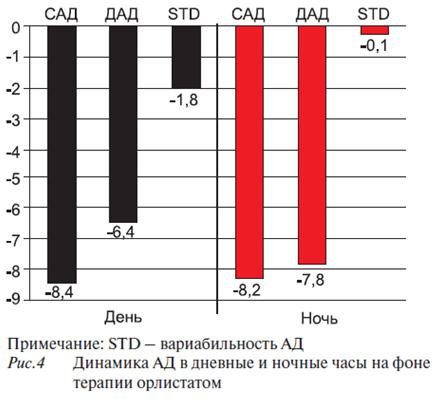
На фоне уменьшения МТ, повышения чувствительности тканей к инсулину и улучшения показателей углеводного и липидного обменов достоверно понизилось АД в дневное и в ночное время суток, и улучшился суточный профиль АД (рисунок 4). Снижение АД в результате уменьшения МТ может быть опосредовано нормализацией повышенной активации СНС и снижением функции ренин-ангиотензин-альдостероновой системы. Эти эффекты, вероятно, обусловлены уменьшением количества СЖК, повышением чувствительности тканей к инсулину на фоне падения МТ.
Через 24 недели лечения орлистатом пациентов с МС и признаками гипертрофии миокарда левого желудочка (ГМЛЖ) последняя достоверно уменьшилась на фоне снижения МТ, АД и благоприятных метаболических эффектов. Уменьшение ГМЛЖ на фоне приема орлистата вероятно связано со снижением МТ, улучшением чувствительности периферических тканей к инсулину, следствием чего является снижение гиперинсулинемии, которая возможно играет значительную роль в формировании ГМЛЖ. Снижение АД могло также оказать благотворное влияние на функционально-структурное состояние миокарда.
Исходно пониженная перфузия головного мозга у пациентов с МС достоверно улучшилась на фоне уменьшения МТ, АД, инсулинорезистентности (ИР) и улучшения показателей углеводного и липидного обменов. Такой выраженный позитивный эффект на состояние перфузии головного мозга можно связать с ростом чувствительности тканей к инсулину, улучшением углеводного и липидного обменов. Все это способствует восстановлению гемостаза, реологии крови и улучшению кровообращения не только в крупных, но и в сосудах микроциркуляторного русла. Снижение ИР, возможно, положительно влияет на эндотелиальную функцию и эндотелийзависимую вазодилатацию.
Из нежелательных побочных эффектов у пациентов наблюдалась только стеаторея, которая, как известно, возникает лишь при повышенном приеме жиров с пищей (>30%). Стеаторея, являясь своеобразным «индикатором» излишнего потребления жиров, помогала пациентам самостоятельно корректировать диету.
Высокая периферическая селективность орлистата, отсутствие системного действия и серьезных побочных эффектов, достаточное уменьшение МТ, которое сопровождается снижением АД и значительным улучшением липидного и углеводного обменов, являющимися серьезными факторами сердечно-сосудистого риска, дает основание рекомендовать орлистат для применения в кардиологической практике. Орлистат (Ксеникал®) можно также успешно применять для профилактики развития МС у здоровых лиц с избыточной МТ.
Литература
- Hubert HB, Feinleib M, McNamara PM, et al. Obesity as an independent risk factor for cardiovascular disease: a 26-year follow-up of participants in the Framingham heart study. Circulation 1983; 67:968-77.
- Silverstone T. Appetite suppressants. Drugs 1992; 43(6): 820-36.
- McCann U, Seiden L, Rubin L, Ricaurte G. Brain Serotonin Neurotoxicity and Primary Pulmonary Hypertension From Fenfluramine and Dexfenfluramine. JAMA 1997; 278: 666-72.
- Weissman N, Tighe J, Gottdiener J, et al. Prevalence of valvular-regurgitation associated with dexfenfluramine three to fine months after discontinuation of treatment. JACC 1999; 34(7): 2088-95.
- Guy-Grand B. The clinical uses of dexfenfluramine in the management of obe-sity. Rev Contemp Pharmacother 1991; 2(2): 115-28.
- Hansen D, Toubro S, Stock M, et al. The effect of sibu-tramine on energy expenditure and appetite during chronic treatment without dietary restriction. Int J Obes Relat Metab Disord 1999; 23(10): 1016-24.
- Ackroff K, Sclafani A. Effects of the lipase inhibitor orlistat on intake and preference for dietary fat in rats. Am J Physiol 1996; 271(1 Pt 2): 48-54.
- Despres JP. The impact of orlistat on the multifactorial risk profile of abdominally obese patients. Diabetes 1998; 48: 1-307.
- Drent M, Larsson I, William-Olsson T, et al. Orlistat (Ro 180647), a lipase inhibitor, in the treatment of human obesity: a multiple dose study. Int J Obes Relat Metab Disord 1995; 19(4): 221-6.
- Zavoral JH. Treatment with orlistat reduces cardiovascular risk in obese patients. J Hypertens 1998; 16: 2013-7.
- Hollander P, Elbein S, Hirsch I, et al. Role of orlistat in the treatment of obese patients with type 2 diabetes. Diabetes Care 1998; 21: 1288-94.
- Kelley D, Bray G, Xavier F, et al. Clinical efficacy of orlistat therapy in overweigh and obese patients with insulin-treated type 2 diabetes. Diabetes Care 2002; 25: 1033-41.
- Torgerson JS, Hauptman J, Boldrin MN, Sjostrom L. XENical in the prevention of diabetes in obese subjects (XENDOS) study: a randomized study of orlistat as an adjunct to lifestyle changes for the prevention of type 2 diabetes in obese patients. Diabetes Care 2004; 27(1): 155-61. Erratum in: Diabetes Care 2004; 27 (3):856.
- Wirth A. Reduction of body weight and comorbidities by orlistat: The XXL - Primary Health Care Trial. .Diabetes Obes Metab 2005; 7(1): 21-7.
- Swinburn BA, Carey D, Hills AP, et al. Effect of orlistat on cardiovascular diseases risk in obese adults. Diabetes Obes Metab 2005; 7(3): 254-62.
- Didangelos TP, Thanopoulou AK, Bouaboulas SH, et al. The Orlistat and Cardiovascular risk in patients with metabolic syndrome and tyre 2 Diabetes (ORLICARDIA) Study. Curr Med Res Opin 2004; 20(09): 1393-401.
- Guy-Grand B, Drouin P, Eschwege E, et al. Effects of orlistat on obesity-related diseases — a six-month randomized trial. Diabetes Obes Metab 2004; 6(5): 375-83.
- Zhi J, Melia A, Guerciolini R, et al. Retrospective population-based analysis of the dose-response (fecal fat excretion) relationship of orlistat in normal and obese volunteers. Clin Pharmacol Ther 1994; 56: 82-5.
- Hauptman J. Orlistat is a well tolerated, long-term treatment for obesity. Int J Obes Relat Metab Disord 1998; 22 (Suppl. 3): P678.
- Мычка В.Б., Творогова М.Г., Яськова К.Н., Чазова И.Е. Терапия ксеникалом больных артериальной гипертонией и метаболическим синдромом. Артер гиперт 2002; 8(1): 16-9.
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


