
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
- Новини 26.10.2021 Аппаратура для УЗИ: применение, принципы работы, разновидности
- Новини 23.10.2021 Интимная пластика после родов: когда необходима операция
Влияние длительной терапии орлистатом на композиционный состав тела, костный метаболизм и минеральную плотность костной ткани у женщин с ожирением в постменопаузе
В постменопаузе у 50% женщин впервые развивается ожирение, либо отмечается его прогрессирование [14,15,16]. Возрастная инволюция репродуктивной системы сопровождается изменением композиционного состава тела с преимущественным отложением жира в абдоминально-висцеральной области и способствует формированию постменопаузального метаболического синдрома. В этот период у женщин в значительной степени возрастает риск развития сахарного диабета 2 типа, артериальной гипертензии, ИБС и др.
Наступление постменопаузы может оказывать негативное влияние на состояние костного метаболизма, провоцируя снижение минеральной плотности костной ткани (МПКТ). Как следствие этого, у 25—40% женщин развивается постменопаузальный остеопороз. Ожирение, как показали исследования, оказывает про-тективный эффект в отношении снижения МПКТ [4,20,21]. В частности Л.Я. Рожинская отметила положительную зависимость между МПКТ и индексом массы тела у женщин в постменопаузе [3]. В проведенном нами исследовании было также показано, что при ожирении у женщин в постменопаузе, остеопенический синдром встречается реже, чем у женщин, имеющих нормальную массу тела. Причем снижение МПКТ у женщин с ожирением сочеталось с низким темпом костного метаболизма, тогда как у женщин без ожирения отмечалось повышение костного обмена [1].
Снижение массы тела у женщин в постменопаузе имеет большое значение для профилактики и лечения заболеваний, связанных с избыточным весом. Терапия ожирения направлена, прежде всего, на снижение массы жировой ткани и, в дальнейшем, на стабилизацию полученных результатов. Однако на практике большинство пациенток не в состоянии эффективно снижать вес или длительно поддерживать достигнутый ранее результат. В связи с этим возникает потребность в более эффективных методах лечения ожирения, в том числе медикаментозной поддержке. В сложившейся ситуации большой интерес представляет Орлистат (Ксеникал®) — препарат периферического действия, оказывающий терапевтическое воздействие в пределах ЖКТ и не обладающий системными эффектами.
Происходящие в процессе длительного лечения ожирения снижение массы жировой ткани, изменение композиционного состава тела, а также определенные ограничения в питании потенциально могут оказать влияние на костный обмен и минеральную плотность костной ткани.
Целью нашего исследования явилась оценка влияния длительного комплексного лечения ожирения (орлистат+диетотерапия) на композиционный состав тела, костный метаболизм и минеральную плотность костной ткани у женщин в постменопаузе.
Материалы и методы
Открытое сравнительное рандомизированное исследование длительностью 12 мес. проводилось в Эндокринологическом научном центре РАМН.
Критерии включения: постменопауза >5лет <10 лет, индекс массы тела (ИМТ) >30, либо >27 кг/м2 с сопутствующими факторами риска.
Критерии исключения: остеопороз, функциональные нарушения щитовидной железы, булимия, синдром мальабсорбции, тяжелые соматические и психические заболевания.
В исследование включено: 60 женщин в возрасте от 45 до 65 лет, средний возраст 55 (51,5;59) лет, ИМТ 36,4 (33,5; 39,1) кг/м2, возраст наступления постменопаузы 51(46; 52,5) лет, длительность постменопаузы 7,2 (6,3; 8,4) лет. Всем пациенткам проводилась оценка антропометрических показателей: масса тела (кг), рост (см), ИМТ (кг/м2), окружность талии (ОТ), окружность бедер (ОБ), соотношение ОТ/ОБ. Методом двухэнерге-тической рентгеновской абсорбциометрии (ДРА) определялся композиционный состав тела по программе «total body» с оценкой количества и процентного соотношения массы жировой и тощей тканей, а также процентного содержания жира в организме.
С целью ранней диагностики снижения МПКТ, методом ДРА проводилась денситометрия поясничного отдела позвоночника (L2-L4) и проксимального отдела бедренной кости с избирательной оценкой костной плотности в отдельных зонах (шейка бедренной кости, большой вертел, область Варда). Исследование проводилось при помощи пакета программ на аппарате Expert XL фирмы LUNAR (США).
Для статических расчетов использовались абсолютные значения МПКТ в г/см2, изменения МПКТ оценивались по Т критерию (величина стандартных отклонений — SD от средних значений «пиковой костной массы») и Z критерию (МПКТ исследуемого субъекта в % от среднепопуляционных возрастных нормативных значений). Диагностика остеопороза осуществлялась согласно критериям ВОЗ (1994 год). Снижение МПКТ до - 1 SD расценивалось как норма, от — 1 до -2,5 — остеопения, более -2,5 — остеопороз.
Определение ионизированного кальция (Са ++) и неорганического фосфата (Р) в плазме крови, Са, Р в утренней моче по отношению к креатинину и Са, Р в суточной моче проводилось на биохимическом анализаторе Hitachi 912 (Roche). Исследовались в сыворотке крови маркеры костеобразования: остеокальцин (ОК) (электрохемилюминесцентный иммуноанализ Elecsys) и общая щелочная фосфатаза (ОЩФ) (биохимический анализатор). Резорбтивная активность костной ткани оценивалась при помощи количественного определения С — терминальных телопептидов, образующихся при деградации коллагена первого типа (бета- Cross Laps) с помощью тест-системы «serum Cross Laps One Step Elisa». Изучалось содержание дез-оксипиридинолина (ДПИД) в утренней моче по отношению к креатинину (Immulite Pyrilinks-D) твердофазный, хемилюминесцентный иммуноанализ.
Ежемесячно осуществлялся мониторинг антропометрических показателей, оценивалась комплаент-ность, а на 6 и 12-м месяцах лечения проводилось полное лабораторно-инструментальное обследование.
Включение пациенток в группы осуществлялось методом простой рандомизации. В основной группе (n=31) пациентки получали орлистат (Ксеникал®) в дозе 120 мг (1 капсула) 3 раза в сутки во время еды, в сочетании с изменением образа жизни и питания. В контрольной группе (n=29) назначалась диетотерапия с ограничением потребления жира не более 30% калорийности суточного рациона.
Статистический анализ проводился при помощи пакета STATISTICA 6.0 (Stat-Soft, 2001) и программы BIO-STATISTICA 4.03 (S.A. Glantz, Mc Graw Hill, перевод на русский язык — «Практика», 1998). Использовались критерий Манна-Уитни (показатель T) для сравнения независимых выборок, тест Уилкоксона (показатель W) для сравнения связанных выборок. При сравнении более двух зависимых выборок использовались ранговый дисперсионный анализ Фридмана (показатель S), множественные сравнения с контрольной группой в этом случае проводились с использованием критерия Ньюме-на-Кейлса (критерий q). Сравнения относительных показателей производилась по критерию %2 (хи-квадрат). Так как по большинству показателей полученные выборки имели неправильное распределение, для их описания использовались медианы с квартилями Me (25; 75) (Me — медиана; 25 и 75 — 1-ый и 3-ий квартили), А Ме. Критический уровень значимости при проверке статистических гипотез принимался равным 0,05.
Результаты исследования
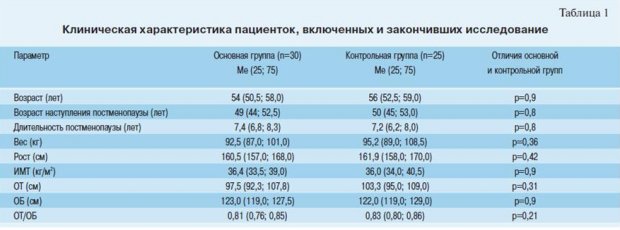
Из 60 пациенток включенных в исследование, лечение закончили 55 человек, 30 в основной группе и 25 в группе контроля. Подробная клиническая характеристика пациенток представлена в таблице 1.
В основной группе на фоне приема орлистата (Ксени-кала®) за 12 месяцев лечения масса тела снизилась на 10,3 кг, в контрольной на 7,2 кг, ИМТ уменьшился в основной группе на 3 кг/м2 и в группе контроля на 2 кг/м2. Клинически значимого снижения массы тела на >5% от исходной за период лечения в основной группе достигли 86,7% (n=26), на > 10% 43,3% женщин (n=13), тогда как в контрольной группе - 72,4% (n=18) и 32% (n=8) пациенток соответственно.
Медиана темпа снижения массы тела в основной группе составила -9,24%, динамики ИМТ -9,18% (р<0,001), в группе контроля -6,23% и -5,23% (р<0,001) соответственно. В группе орлистата медиана динамики окружности талии составила -4,04% (р<0,001) в контрольной -3,85% (р<0,001). Сравнительный анализ по периодам лечения показал, что на фоне приема ор-листата (Ксеникала®) снижение антропометрических показателей было значимо, как в первом, так и втором полугодии лечения, а в группе контроля только в течение первых 6 месяцев. То есть, на фоне приема орлис-тата пациентки на этапе поддержания массы тела, не только сумели удержать достигнутый ранее результат, но и продолжали снижать вес (табл. 2).
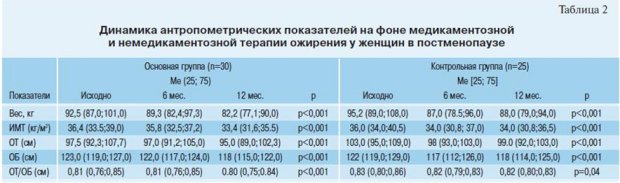
В контрольной группе 32% (n=8) женщин не смогли удержать достигнутую в процессе снижения массу тела.
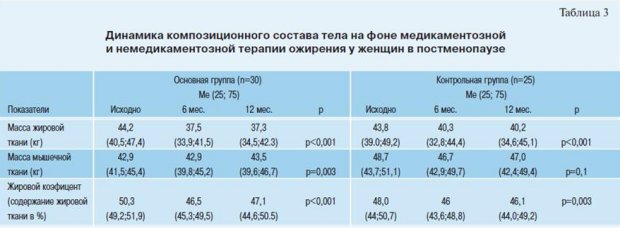
Снижение массы тела у всех пациенток сопровождалось изменением композиционного состава тела. У женщин получавших орлистат масса жировой ткани уменьшилась на 7 кг, тогда как контрольной группе на 3,6 кг, что в два раза меньше, чем в основной группе. Более того, на фоне приема орлистата потеря массы жировой ткани была статистически значимо выше, чем в контрольной группе (р=0,027), и это снижение сопровождалось увеличением массы мышечной ткани на 0,6 кг (р=0,003). В контрольной группе потеря массы жировой ткани, напротив, сопровождалась снижением массы мышечной ткани (на 1,7 кг) (р=0,1). Медиана динамики потери жировой массы за 12 мес. наблюдения в основной группе составила -14,4%, в группе контроля -9,1% (табл. 3).
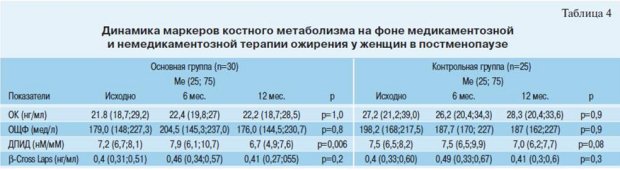
У всех женщин с ожирением исходно был низкий темп костного метаболизма, в процессе лечения динамических изменений маркеров, отражающих состояние костного обмена не выявлено, за исключением снижения уровня ДПИДа (маркера костной резорбции) с 7,2 до 6,7 нМ/мМ (р=0,006) в основной группе (табл 4).
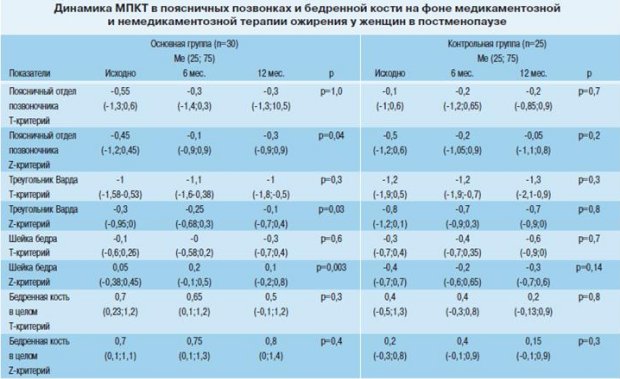
При первичном обследовании остеопения (Т-крите-рий от -1 до -2,5 SD) в поясничных позвонках выявлена у 36% женщин основной и 38 % контрольной групп; в треугольнике Варда у 46% женщин основной группы и 34% контрольной, в шейке бедра у 10% и 7% обследованных соответственно. В целом в бедренной кости остеопения обнаружена у 3% пациенток основной группы и 10% контрольной. В наблюдаемых группах через 12 мес. лечения частота остеопении не изменилась, и не отмечалось статистически значимого снижения МПКТ в исследуемых зонах. Результаты денситометрии поясничных позвонков и бедренной кости представлены в таблице 5.
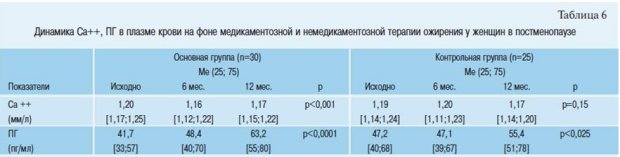
Исходно у всех женщин с ожирением не было отмечено нарушений кальций-фосфорного обмена, однако за время наблюдения прослеживалась тенденция к снижению уровня ионизированного кальция, как в контрольной, так и в основной группах. Содержание Са ++ снизилось с 1,20 до 1,17 ммоль/л в основной, с 1,19 до 1,17 ммоль/л в контрольной группе. Однако все показатели не превышали границы референсных значений. Динамических изменений со стороны экскреции кальция, фосфора в утренней и суточной моче в обследуемых группах отмечено не было (табл. 6).
Обсуждение
Результаты проведенного исследования показали, что терапия орлистатом (Ксеникалом®) не только способствует эффективному снижению массы тела у женщин в постменопаузе, но и позволяет стабилизировать полученные результаты в течение длительного времени, что отвечает современным требованиям лечения ожирения. Применение орлистата способствует также улучшению композиционного состава тела: на фоне длительного приема препарата снижение массы тела происходило преимущественно за счет потери массы жировой ткани и сопровождалось увеличением массы мышечной ткани.
В зарубежной литературе опубликовано большое число работ по изучению эффективности и безопасности применения орлистата у пациентов с ожирением различных возрастных групп. Hutton B. и Fergusson D. (2004) провели мета-анализ 28 рандомизированных плацебо контролируемых исследований с участием более десяти тысяч пациентов и показали, что применение ор-листата в сочетании с гипокалорийной диетой в течение 6—12 мес более эффективно, чем только диетотерапия. Более 85% пациентов, получавших орлистат, достигли снижения массы тела более чем на 5% от исходной. Кроме того, орлистат существенно повышает эффективность диетотерапии у больных с нарушениями углеводного, липидного обмена, сердечно-сосудистыми заболеваниями, как в отношении снижения массы тела, так и улучшения метаболических показателей [13].
В исследованиях по изучению факторов риска остео-пороза было показано, что потеря веса может рассматриваться как независимый фактор риска развития остеопо-роза [10,11,18], особенно у женщин в постменопаузе [17].
В проведенном нами исследовании не отмечено изменений МПКТ и маркеров костного метаболизма на фоне длительного лечения ожирения у женщин в постменопаузе. Полученные результаты согласуются с данными Г.А. Хорошевой, Г.А. Мельниченко с соавт, продемонстрировавших, что длительное лечение женщин в постменопаузе не оказывает отрицательного влияния на МПКТ[2].
Holecki М. (2005) также не обнаружил снижения МПКТ на фоне трехмесячного приема орлистата [12].
В зарубежной литературе цитируются неоднозначные результаты исследований, оценивающих влияние снижения массы тела на маркеры костного метаболизма. Так Pace D. с соав. (2001), изучая маркеры: костеоб-разования (ОК, КЩФ) и костной резорбции (пириди-нолин (ПИД), (ДПИД), Р-кросслап, оксипролин) на фоне трехнедельного приема орлистата, не отметили статистически значимых изменений изучаемых показателей, как в основной, так и в контрольной группе [19].
Gotfredsen A. с соавт. отметили увеличение содержания маркеров костной резорбции (отношение экскреции оксипролина к клиренсу креатинина) как в контрольной группе, так и у пациентов, получавших орлистат [9]. Следует подчеркнуть, что, оценивая маркеры костного метаболизма, необходимо учитывать, что их уровень подвергается значительным колебаниям в зависимости от пола, возраста (особенно у женщин), приема пищи, физической активности, функционального состояния печени и почек, приема фармпрепаратов, и, кроме того, различная чувствительность лабораторных наборов может также влиять на результаты измерения [5,8,10].
В ряде экспериментальных и клинических исследований зарубежных авторов, изучавших состояние кальций-фосфорного обмена на фоне снижения массы тела, получены неоднозначные данные. Так Cifuentes M. с соавт. (2002) в эксперименте показали, что потеря массы тела у животных сопровождалась снижением абсорбции кальция в желудочно-кишечном тракте [7]. В последующих работах, авторы получили аналогичные результаты у женщин с ожирением в постменопаузе при соблюдении гипокалорийной диеты с физиологической нормой содержания кальция (1 г/сутки), тогда как в группе женщин с высоким потреблением кальция(1,8 г/сутки) его абсорбция не изменялась [6]. В то же время Holecki М. с соавт. (2005) не выявили изменений в содержании общего кальция и фосфора в крови на фоне комбинированного лечения женщин с ожирением в постменопаузе [12]. В нашем исследовании была отмечена тенденция к снижению уровня ионизированного кальция, но при этом все полученные показатели не выходили за диапазон нормативных значений.
В заключение хотелось бы отметить, что длительное применение орлистата (Ксеникала®) в комплексной терапии ожирения у женщин в постменопаузе не оказывает влияния на костный метаболизм и минеральную плотность костной ткани, и может эффективно использоваться у пациенток данной возрастной группы.
Выводы
- Применение орлистата (Ксеникала®) в комплексной терапии ожирения у женщин в постменопаузе способствует наиболее эффективному и устойчивому снижению массы тела и сопровождается улучшением композиционного состава тела.
- Длительное, комплексное лечение ожирения не оказывает отрицательного воздействия на костный метаболизм и МПКТ у женщин в постменопаузе.
Литература
- Мельниченко Г.А., Бутрова С.А., Чигарькова О.В., Ильин А.В. Состояние костной ткани у женщин с ожирением в постменопаузе // Врач - 2004. - №9 - С 32-34.
- Хорошева Г.А., Мельниченко Г.А, Романцова Т.И., Изможерова Н.В., Попов А.А. Открытое исследование эффективности и безопасности терапии орлистатом (Ксеникалом) у женщин с метаболическим синдромом в постменопаузе // Ожирение и метаболизм – 2005. - № 1 - С 8 - 12, № 2 - С 26 - 29.
- Рожинская Л.Я. Остеопенический синдром при заболеваниях эндокринной системы и постменопаузальный остеопороз. // Диссертация на соискание ученой степени д.м.н. // 2001 – Москва. С-275.
- Dawson-Hughes B., Shipp C., Sadowski L., Dallal G. Bone density of the radius, spine and hip in relation to percent of ideal body weight in postmenopausal women. // Calcif Tissue Int. 1987; 40:310 - 314.
- Christgau S. - Circadian variation in serum Crosslaps concentration is reduced in fasting individuals. // Clin Chem. – 2000 - 46:431.
- Cifuentes M., Riedt C.S., Field M.P., Sherrell R.M., Brolin R.E., Shapses S.A. Weight loss and calcium intake influence calcium absorption in overweight postmenopausal women. // Am J Clin Nutr - 2004 - 80:123-130.
- Cifuentes, M., Morano A. B., Chowdhury H. A. & Shapses S. A. Energy restriction reduces fractional calcium absorption in mature obese and lean rats. // J. Nutr – 2002. - 132:2660-26667.
- Delmas P.D, Eastell R., Garnero P., Seibel M.J, Stepan J. Committee of Scientific Advisors of the International Osteoporosis Foundation The use of biochemical markers of bone turnover in osteoporosis. Committee of Scientific Advisors of the International Osteoporosis Foundation. // Osteoporos Int. 2000. - 11 Suppl 6: S2 - 17.
- Gotfredsen A., Westergren Hendel H., Andersen T. Influence of orlistat on bone turnover and body composition. // Int J Obes Relat Metab Disord. 2001 Aug; 25(8):1154-60.
- Hannon R., Eastell R. Preanalytical variability of biochemical markers of bone turnover. // Osteoporos Int – 2000 – 11 (Suppl 6): S 30 – S 44.
- Holbrook T.L., Barrett-Connor E. The association of lifetime weight and weight control patterns with bone mineral density in an adult community. // Bone Miner – 1993 - ; 20:141–9.
- Holecki M., Zahorska-Markiewicz B., Nieszporek T., Olszanecka-Glinianowicz M., Mizia-Stec K., Zak-Golab A., Kocelak P., Fryzlewicz-Moska A., Wiecek A. Impact of the mass-reductive therapy with orlistat on 25-(OH)-D3 and PTH concentration in sera of obese, menopausal women. // Endokrynol Pol. – 2005 - May-Jun; 56(3):240-5.
- Hutton B., Fergusson D. Changes in body weight and serum lipid profile in obese patients treated with orlistat in addition to a hypocaloric diet: a systematic review of randomized clinical trials. // Am J Clin Nutr. -2004- Dec; 80 (6):1461-8.
- Lovejoy J.C. The influence of sex hormones on obesity across the female life span. // J Wom Health 1998; 7: 1247 - 1256.
- Manson J.C. Willet W.C. Stampfer M.J. et al. Body weight and mortality among women. // N Engl J. Med 1995; 333: 677-685.
- Milewicz A. Bidzinska B., Sidorowicz A. Perimenopausal obesity. // Glinecol Endocrinol 1996; 10: 285-291.
- Nelson H.D, Morris C.D, Kraemer D.F, et al. Osteoporosis in postmenopausal women: diagnosis and monitoring. Evidence Report/Technology Assessment No. 28 (Prepared by the Oregon Health & Science University Evidence-based Practice Center under Contract No. 290-97-0018). AHRQ Publication No. 01-E032. Rockville, MD: Agency for Healthcare Research and Quality. January 2001.
- Nguyen TV, Sambrook PN, Eisman JA. Bone loss, physical activity, and weight change in elderly women: the Dubbo Osteoporosis Epidemiology Study. // J. Bone Miner Res 1998; 13:1458–67
- Pace D.G, Blotner S., Guerciolini R. Short-term orlistat treatment does not affect mineral balance and bone turnover in obese men. // J. Nutr. - 2001 – Jun ;131(6): 1694-9.
- Stevenson J.C, Lees B., Devenport M., Cust M.P., Gagner K.F. Determinants of bone density in normal women: risk factors for future osteoporosis? // Br. Med. J.1989; 298:924-928.
- Slemenda C, Hui SL, Longcope C, Johnston CC. Sex; and bone mass. A study of changes about the time of menopause. // Clin Invest. 1987 - 80:1261-1269.
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


