
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
- Новини 26.10.2021 Аппаратура для УЗИ: применение, принципы работы, разновидности
- Новини 23.10.2021 Интимная пластика после родов: когда необходима операция
Применение орлистата и пиоглитазона при синдроме поликистозных яичников и ожирении
Проведена сравнительная оценка влияния 6-месячного курса терапии орлистатом (n = 20) и пиоглитазоном (n = 11) на метаболические параметры и эндокринную функцию репродуктивной системы больных с синдромом поликистозных яичников (СПКЯ) и ожирением. После приема орлистата масса тела снизилась на 11,3 ± 1,3 кг, после пиоглитазона — повысилась на 2,9 ± 0,7 кг. Коррекция ги- перинсулинемии и инсулинорези- стентности на фоне двух видов терапии носит схожий характер, однако орлистат характеризуется более выраженным положительным воздействием на показатели липидного спектра крови и толерантность к глюкозе. Препараты оказывают сопоставимый эффект на гормональные показатели, что проявляется тенденцией к снижению гонадотро- пинов, нормализацией уровня сома- тотропного гормона (СТГ) и достоверным снижением уровня тестостерона. Применение орлистата приводит к повышению половых стероид- связывающих глобулинов (ПССГ) и соответственно к более выраженному снижению индекса свободных андрогенов. Лечение орлистатом, как и пиоглитазоном, сопровождается регуляцией ритма менструаций примерно у каждой второй пациентки с СПКЯ и ожирением.
СПКЯ является одной из наиболее распространенных причин нарушений менструального цикла, гирсутизма и бесплодия, по поводу которых молодые женщины обращаются к гинекологу. С современных позиций СПКЯ трактуется как своеобразная форма метаболического синдрома, для которой характерны инсулинорезистентность, гиперинсулинемия, дислипопротеидемия и повышенный риск возникновения сахарного диабета (СД) 2 типа и кардиоваскулярных заболеваний [9, 10, 17, 20, 34 ]. Известно, что гиперинсулинемия за счет прямого и опосредованного влияния на стероидогенез в яичниках может индуцировать секрецию андрогенов, а также повышать их биологическую активность, в связи с чем ее можно считать одним из ведущих факторов нарушения функции яичников, приводящих к бесплодию при СПКЯ [7, 11, 27]. В связи с этим в качестве консервативной терапии больных с СПКЯ с успехом используются инсулиносенситайзеры: с середины 1990-х г. — бигуаниды (метформин) и тиазолидиндионы I поколения (троглитазон), а с начала нового столетия — накапливается опыт по применению тиазолидиндионов II поколения (розиглитазон и пиоглитазон). Терапия этими препаратами способствует не только улучшению чувствительности к инсулину и снижению гиперинсулинемии, но и коррекции гормональных нарушений, что, в свою очередь, восстанавливает ритм менструаций и фертильность у женщин с СПКЯ.
СПКЯ часто сочетается с ожирением, являющимся самостоятельным фактором риска инсулинорезистентности, гиперинсулинемии и развития метаболических нарушений, которые ассоциируются с репродуктивной дисфункцией [15, 36, 38]. Адекватное снижение массы тела способствует коррекции гормональных, метаболических нарушений и регуляции ритма менструаций у больных с ожирением и нарушениями функции яичников [4, 5, 12, 23, 24, 28, 32]. Проводившиеся нами ранее исследования показали, что монотерапия орлистатом позволяет восстановить овуляцию у каждой третьей женщины с ожирением и эндокринным бесплодием [5]. Публикации, посвященные использованию фармакопрепаратов, снижающих массу тела, при СПКЯ, крайне малочисленны [26]. Вместе с тем логично предположить, что такая терапия у больных с СПКЯ и ожирением будет не менее эффективной, чем применение инсулиносенситайзеров, которые не оказывают существенного влияния на массу тела.
Целью исследования стала сравнительная оценка влияния орлистата и пиоглитазона на метаболические параметры и эндокринную функцию репродуктивной системы женщин с СПКЯ и ожирением.
В исследование были включены 31 женщина в возрасте от 18 до 40 лет с СПКЯ и ожирением. В зависимости от вида проводимой терапии пациентки были разделены на две группы: 1-ю составили 20 женщин, которым был назначен орлистат (ксеникал — Хоффман Ла Рош, Швейцария) в суточной дозе 360 мг, 2-ю — 11 женщин, которым был рекомендован пиоглитазон (актос — Eli Lilly, США) в суточной дозе 30 мг. Длительность терапии составила 6 мес. Диагностика СПКЯ проводилась на основании характерных клинических, эхографических и гормональных признаков. Женщины с дефицитом 21-гидроксилазы, гиперпролактинемией, болезнью Кушинга и андрогенпродуцирующими опухолями в исследование не включались. В течение 3 мес, предшествующих началу лечения, пациентки не принимали гормональных препаратов. Критериями исключения явились противопоказания к назначению орлистата и пиоглитазона, беременность, лактация, тяжелая сопутствующая соматическая и психическая патологии, СД с медикаментозной терапией, прием гиполипидемических, ферментативных препаратов, содержащих липазу, а также трициклических антидепрессантов.
Средний возраст женщин, которым была назначена терапия орлистатом, составлял 27,7 ± 0,9 лет, пиоглитазоном — 25,6 ± 1,4 года. Средняя масса тела соответственно — 92,3 ± 3,3 кг и 82,6 ± 3,4 кг; индекс массы тела (ИМТ) — 33,8 ± 0,9 и 30,1 ± 0,7; объем талии (ОТ) — 97,7 ± 2,1 см и 92,4 ± 2,1 см; объем бедер (ОБ) — 114,9 ± 2,3 см и 109,1 ± 2,8 см; ОТ/ОБ — 0,85 ± 0,01 и 0,85 ± 0,02.
Клинические признаки андрогенизации имели место у 18 (90 %) больных в 1-й группе (гирсутное число — 19,5 ± 2,5), и у 10 ± 90,9%) больных во 2-й группе (гирсутное число — 14,7 ± 1,1). УЗИ-признаки СПКЯ в 1-й группы диагностированы у 17 (85%) пациенток, во 2-й группе — у 10 (90,9%). Нарушение функций яичников отмечено у всех больных. В 1-й группе ановуляция диагностирована у 20 (100 %) пациенток, из них олигоменорея — у 17 (85%) больных и вторичная аменорея — у 3 (15%), во 2-й группе эти показатели соответственно составили 11 (100%), 8 (72,7%) и 2 (18,2%), у 1 (9,1%) пациентки ановуляция наблюдалась на фоне регулярного менструального цикла. У подавляющего большинства пациенток обеих групп, нарушения менструального цикла наблюдались с менархе, в ряде случаев они возникли на фоне увеличения массы тела и приема комбинированных оральных контрацептивов. Две пациентки из числа обследованных в 1-й группе не были заинтересованы в беременности, среди остальных пациенток — у 12 (66,7%) было бесплодие I и у 6 (33,3%) — бесплодие II степени, во 2-й группе в беременности также не были заинтересованы 2 пациентки, у 7 (77,8%) — диагностировано бесплодие, еще у двоих (22,2%) — бесплодие II.
У всех больных, включенных в исследование, до и после лечения проводился мониторинг антропометрических, метаболических и гормональных показателей, а также оценивался характер менструального цикла. Все пациентки 2-й группы прошли 6-месячный курс терапии, из 1-й группы 3 человека были исключены из исследования: одна в связи с беременностью после 3-месячного лечения орлистатом, другая в связи с холецистэктомией, еще одна женщина отказалась от приема препарата по причинам, не связанным с побочными явлениями в результате проводимой терапии.
Радиоимунными методами с использованием тест-систем Immunotech (Чехия) или ИБОХ (Беларусь), согласно приложенным к ним инструкциям, проводилось исследование содержания в сыворотке крови больных лютеинизирующего (ЛГ) и фолликулостимулирующего (ФСГ) гормонов, эстрадиола (Е2), СТГ, тестостерона и ПССГ. По расчетным формулам вычислялись свободный андрогенный индекс (САИ) = 100 х тестостерон (нмоль/л)/ ПССГ(нмоль/л) и свободный эстрогенный индекс (СЭИ) = 0,1 х Е2 (пмоль/л)/ ПССГ(нмоль/л). Гиперинсулинемия диагностировалась на основе определения уровня имунореактивного инсулина (ИРИ) натощак и результатов перорального 2-часового глюкозотолерантного теста (ГТТ) с 75 г глюкозной нагрузки, который проводился исходно и через 6 месот начала терапии. Содержание ИРИ оценивалось методом IRMA, с использованием тест-систем ИБОХ (Беларусь). Количественная оценка инсулиновых ответов на глюкозную нагрузку проводилась расчетным путем по величинам молярных площадей (S) под соответствующими секреторными кривыми, рассчитанными по трапецевидному правилу. Инсулинорезистентность оценивалась по расчетному индексу: HOMA (Homeostasis model assessment) = ИРИ (мкЕД/мл) х глюкоза (ммол/л)/22,5.
Статистический анализ проводился с использованием программ «Statistica-6»; для определения значимости (достоверности) различий сопоставляемых величин использовали непараметрические критерии Вилкоксона для связанных совокупностей, различия считали достоверными при p 0,05.
После 6-месячного курса терапии орлистатом масса тела снизилась на 1 1,3 ± 1,3 кг (с 92,4 ± 3,3 до 79,2 ± 3,5 кг), что составило 13,0 ± 1,3 % от исходного значения. Если до лечения ожирение III степени встречалось у 10 % больных, то после лечения ни у одной больной столь выраженного ожирения уже не отмечалось, частота ожирения II степени снизилась в 2,5 раза (от 30 до 11,8%), I степени — в 1,7 раза (с 50 до 29,4%), соответственно увеличилась частота избыточной массы тела с 10 до 58,8%. На фоне терапии пиоглитазоном снижения массы тела ни у одной пациентки не отмечалось, у 3 (27,3%) больных вес оставался стабильным, у 8 (72,3%) выявлялось его увеличение. Масса тела выросла от 82,4 + 3,7 до 84,8 + 3,7 кг, что в среднем составило 2,9 ± 0,7 кг. При этом случаев развития ожирения у пациенток с избыточной массой тела, а также увеличения числа больных с выраженными степенями ожирения выявлено не было.
Применение орлистата сопровождалось закономерной коррекцией антропометрических параметров: достоверно снизилось среднее значение ОТ (до лечения — 97,7 ± 2,1; после — 84,7 ± 2,4), ОБ (до лечения — 114,9 ± 2,3; после — 102,4 ± 2,5); ОТ/ОБ (до лечения 0,85 ± 0,01; после — 0,83 ±0,01) (p < 0,05). На фоне терапии пиоглитазоном средние значения ОТ, ОБ и ОТ/ОБ фактически ни изменились: ОТ — до терапии — 91,2 ± 2,0, после — 92,6 ( 2,0; ОБ соответственно 108,9 ± 3,1 и 109,2 ± 3,1; ОТ/ОБ — 0,84 ± 0,02 и 0,84 ± 0,02 (p > 0,05).
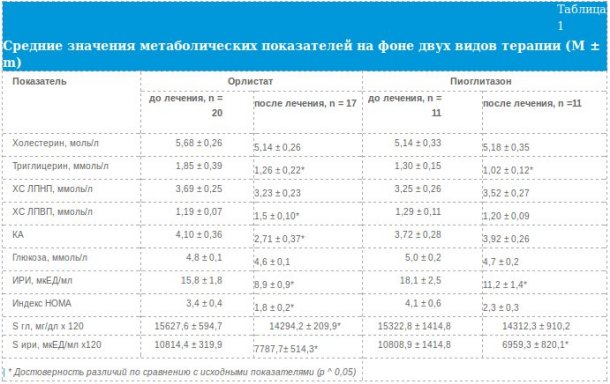
Применение обоих видов терапии оказывало влияние на метаболические параметры. На фоне приема орлистата и пиоглитазона произошло достоверное снижение содержания триглицеридов в сыворотке крови больных (табл. 1). После приема орлистата частота гипертриглицеридемии снизилась примерно в 2,5 раза (с 30 до 11,8%), в группе пиоглитазона как до, так и после лечения не выявлено ни одного случая гипертриглицеридемии, хотя общий уровень триглицеридов тоже снизился. Существенных изменений средних уровней холестерина в обеих группах отмечено не было. Вместе с тем более детальный анализ показал, что если до лечения орлистатом гиперхолестеринемия выявлялась у 15 (75%) больных, то после лечения она была диагностирована у 9 человек (52,9%), в группе больных, получавших пиоглитазон, эти показатели составили 6 (54,5%) и 5 (45,5%). Как видно из данных, представленных в таблице 1, положительная динамика липидных показателей сыворотки крови после приема орлистата проявлялась в достоверном повышении холестерина липопротеидов высокой плотности (ЛПВП), тогда как после приема пиоглитазона содержание этой фракции липопротеидов существенно не изменилось. Гипоалипопротеидемия до приема орлистата встречалась у 14 (70%) больных, после — у 7 (41,2 %), в группе пиоглитазона у 6 (54,5%), как до, так и после терапии.
Терапия вышеуказанными препаратами оказывала положительное влияние на показатели углеводного обмена. Несмотря на отсутствие существенной динамики по средним уровням глюкозы, исследуемой натощак, как после приема орлистата, так и после приема пиоглитазона снизились суммарные гликемические ответы на ГТТ, что подтверждается уменьшением молярных площадей под гликемическими кривыми (табл. 1). Следует отметить, что прием орлистата оказывал более выраженное положительное влияние на показатели углеводного обмена. Так, до лечения орлистатом нарушение толерантности к глюкозе (НТГ) (как натощак, так и на фоне ГТТ) имело место у 5 (25%) больных, а после терапии не было диагностировано ни в одном случае; в группе больных, принимавших пиоглитазон, исходная частота НТГ составила 27,3%, после лечения — 18,2%.
Как видно из данных, представленных в таблице 1, существенной динамики в тощаковых уровнях ИРИ отмечено не было, вместе с тем выявлено достоверное снижение молярных площадей под кривыми секреции ИРИ. Прием препаратов способствовал схожему снижению частоты гиперинсулинемии, которая после лечения орлистатом снизилась с 70 до 23,5%, а после приема пиоглитазона — с 90,9 до 27,3%.
Результаты исследования указывают на положительный эффект двух видов терапии на чувствительность к ИРИ, о чем свидетельствует снижение средних показателей индекса НОМА (табл. 1).
Проведенная терапия оказала влияние на содержание гормонов в сыворотке в крови. Из данных, представленных в таблице 2, видно, что среднее содержание гонадотропинов на фоне двух видов терапии существенно не изменилось. Однако если до начала терапии повышенный уровень ЛГ диагностировался у 11 (55%) больных 1-й группы и у 6 (54,5%) больных 2-й группы, то после проведенного лечения эти показатели составили 35,3 и 63,6%. Повышение индекса ЛГ/ФСГ ( 2,5 до лечения орлистатом отмечалось у 9 (45%) больных, после лечения — у 4 (23,5%), т. е. снизилось в 1,9 раз, на фоне пиоглитазона частота повышенного индекса ЛГ/ФСГ значительно не изменилась — 5 (45,5%) и 6 (54,5%). На фоне обоих видов терапии отмечена четкая тенденция к нормализации исходно низких значений СТГ (табл. 2).
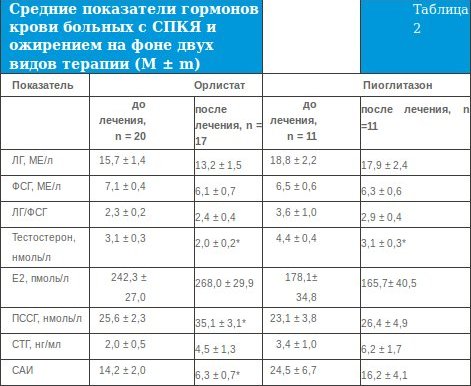
На фоне приема как пиоглитазона, так и орлистата достоверно снизился средний уровень тестостерона в крови — по сравнению с исходным показателем. Следует отметить, что исходно повышенные уровни тестостерона были выявлены у 13 (65%) пациенток, после лечения орлистатом лишь у 2 (11,8%). Во 2-й группе исходные уровни тестостерона были повышены у 10 (90,9%) больных, после приема пиоглитазона — у 6 (54,5%) пациенток.
Терапия орлистатом сопровождалась достоверным ростом исходно низкого уровня ПССГ, тогда как прием пиоглитазона не оказывал существенного влияния на уровень этого транспортного белка (табл. 2). Эти изменения сказались на средних показателях САИ, которые после 6-месячного приема орлистата снизились примерно в 2,2 раза, после пиоглитазона — в 1,5 раза.
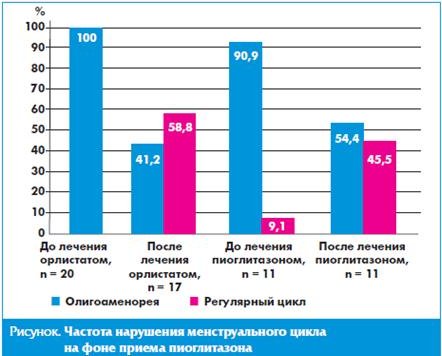
Коррекция гормональных параметров клинически проявлялась положительными изменениями в характере менструального цикла. После приема орлистата частота ановуляции снизилась со 100 до 41,2%, частота олигоменореи — с 85 до 41,2%. У 58,8% больных удалось добиться регуляции ритма менструаций, при этом двухфазный цикл восстановился у 5 (29,4%) пациенток, еще у 5 (29,4%) диагностирована недостаточность лютеиновой фазы менструального цикла. Положительная динамика в характере менструального цикла отмечалась и на фоне пиоглитазона, после 6-месячного приема препарата частота регулярного цикла выросла от 9,1 до 45,5 %. На рисунке отражена частота нарушения менструального цикла на фоне двух видов терапии.
К концу 3-го месяца приема орлистата у одной пациентки наступила беременность. Переносимость препаратов у всех больных была хорошей. Побочные эффекты, возникшие на фоне орлистата, проявлявшиеся в виде диареи, маслянистых выделений из прямой кишки, метеоризма, были слабо выражены, отмечались в начале лечения и имели проходящий характер. Эти побочные явления являлись следствием неумеренного потребления жиров и свидетельствовали о достаточной эффективности препарата. Побочные эффекты, возникавшие на фоне приема пиоглитазона, выражались только в незначительном повышении массы тела.
В настоящее время в качестве одного из ведущих патогенетических механизмов возникновения СПКЯ рассматривается гиперинсулинемия, в результате сниженной чувствительности периферических тканей к действию инсулина [16, 29]. Частота ее возникновения и выраженность коррелируют с наличием и степенью ожирения, которое характерно примерно для 50% женщин с СПКЯ [36, 38]. Имеется достаточное количество доказательств того, что ожирение усугубляет выраженность гормональных и метаболических нарушений при СПКЯ и отягощает клиническое течение синдрома [1, 15, 31, 32]. Известно также, что традиционное использование комбинированных оральных контрацептивов с целью регуляции цикла и/или лечения гирсутизма нередко способствует прибавке массы тела и ухудшению метаболических параметров, что, в свою очередь, создает предпосылки к сохранению нарушений функций яичников. Эволюция взглядов на патогенез СПКЯ явилась основанием для пересмотра подходов к консервативной терапии и внедрения в клиническую практику лекарственных средств, повышающих чувствительность к инсулину, коррегирующих гиперинсулинемию и гиперандрогению [6, 16, 27]. Однако эти препараты не оказывают существенного влияния на снижение массы тела; остается открытым вопрос о возможности их длительного применения для коррекции метаболических и гормональных нарушений у больных с СПКЯ. В связи с этим нами была предпринята попытка провести сравнительную оценку эффективности инсулиносенситайзера — пиоглитазона, зарекомендовавшего себя в качестве одного из препаратов выбора при СПКЯ, и орлистата, являющегося эффективным медикаментозным средством для лечения ожирения.
Как и следовало ожидать, прием пиоглитазона не привел к снижению массы тала, а у 72,3% больных даже наблюдалась тенденция к некоторому ее увеличению, которое объясняют либо возрастанием доли подкожной жировой ткани, с одновременным уменьшением висцерального жира, либо развитием отека [20]. Шестимесячный же курс терапии орлистатом способствовал снижению массы тела на 13,0 ± 1,3%, что сопоставимо с данными других исследований по применению этого препарата [2, 13, 22, 37]. Это неплохой результат, если принять во внимание тот факт, что клинически значимым является снижение массы тела более чем на 10% от исходных значений [1, 3, 5].
Несмотря на столь выраженную разницу во влиянии на массу тела оба вида терапии оказывали положительный эффект на метаболические параметры. Под влиянием обоих препаратов частота гиперинсулинемии снизилась примерно в 3 раза, после приема пиоглитазона в 1,5 раза реже выявлялось НТГ, после приема орлистата случаев НТГ диагностировано не было. Указанные изменения во многом обусловлены нормализацией чувствительности периферических тканей к ИРИ в результате прямого влияния пиоглитазона на механизмы передачи инсулинового сигнала за счет стимуляции пероксисомального пролиферата PPARy и опосредованного влияния орлистата путем ингибирования циркулирующих свободных жирных кислот и снижения глюконеогенеза в печени [21, 33]. О повышении чувствительности к ИРИ косвенно свидетельствует снижение индекса НОМА, который рассматривается в качестве возможного и доступного критерия инсулинорезистентности. Отсутствие выраженных изменений данного показателя можно объяснить его значительной вариабельностью и небольшой выборкой больных [26].
Наряду с уменьшением степени выраженности гиперинсулинемии и инсулинорезистентности на фоне пиоглитазона и особенно орлистата наблюдались положительные сдвиги в липидном спектре крови. Так, хотя потери массы тела зафиксировано не было, прием пиоглитазона сопровождался достоверным уменьшением содержания триглицеридов в сыворотке крови. В ряде работ других исследователей также было отмечено триглицеридснижающее действие тиазолидиндионов [14], причем наиболее выраженным эффектом обладал пиоглитазон, который в меньшей степени увеличивал уровень холестерина ЛПНП [18, 25]. Несмотря на более выраженные исходные метаболические нарушения, в частности большую массу тела, у пациенток, принимавших орлистат, отмечалась более выраженная динамика как атерогенных, так и антиатерогенных фракций липопротеидов — определялось снижение суммарного атерогенного потенциала крови. Нормализация липидного спектра крови в значительной степени связана со снижением гиперинсулинемии, которая индуцирует возникновение липидных нарушений. Более выраженные сдвиги, выявленные после приема орлистата, могут быть обусловлены дополнительным ингибирующим эффектом препарата на абсорбцию липидов в желудочно-кишечном тракте.
Коррекция метаболических нарушений сочеталась с нормализацией гормональных показателей. Наибольшие изменения касались содержания тестостерона (снижение на фоне пиоглитазона составило примерно 30%, на фоне орлистата — 35%). Традиционно считается, что снижение уровня тестостерона в значительной степени связано с уменьшением гиперинсулинемии, приводящей к снижению стимулирующего влияния ИРИ на ферментативную активность клеток яичника, в частности на цитохром Р-450 и, соответственно, на секрецию андрогенов [ 27]. Однако имеются данные и о прямом ингибирующем влиянии тиазолидиндионов на ферментативную активность и биосинтез яичниковых андрогенов [8]. Секреция тестостерона в яичниках регулируется ЛГ. Однако лечение обоими препаратами не повлекло за собой значительного снижения уровня этого гормона, которое могло бы объяснить уменьшение тестостерона.
Известно, что ИРИ способствует увеличению свободных фракций андрогенов за счет ингибирования синтеза ПССГ печенью [19, 35]. По результатам данного исследования значительного изменения этого показателя, особенно после приема пиоглитазона, обнаружено не было. Это можно объяснить небольшим числом прошедших курс лечения больных, поскольку в ранее проведенных нами исследованиях, выполненных на большем количестве клинических наблюдений, даже через 3 мес терапии отмечалось достоверное повышение уровня ПССГ [5, 6].
Результаты исследования четко продемонстрировали повышение исходно низких уровней СТГ как после лечения пиоглитазоном, так и орлистатом. В литературе также имеются данные о нормализации содержания СТГ в сыворотке крови больных с ожирением на фоне снижения массы тела [30]. Однако, учитывая отсутствие снижения массы тела у больных, лечившихся пиоглитазоном, можно полагать, что в этом случае данный механизм не вовлечен в коррекцию уровня СТГ.
Коррекция гормональных нарушений сопровождалась нормализацией ритма менструаций, частота ановуляции в обеих группах снизилась примерно в 2 раза. После курса терапии пиоглитазоном регулярный менструальный цикл восстановился у 45% больных с СПКЯ и ожирением, после терапии орлитатом — у 58,8%. Это привело к наступлению беременности у 3 больных в 1-й группе (у одной на фоне и у 2 после отмены лечения), во 2-й группе после лечения беременность наступила также у 2 больных. Полученные данные согласуются с результатами большинства исследований, демонстрирующих, что коррекция гиперинсулинемии и яичниковой гиперандрогении может способствовать нормализации ритма менструаций и восстановлению фертильности [19, 26, 35].
Таким образом, на основании всего вышесказанного можно сделать заключение, что оба препарата одинаково эффективны в коррекции гиперинсулинемии, яичниковой гиперандрогении и лечении хронической ановуляции у больных с СПКЯ и ожирением. Орлистат, эффективно снижая массу тела, оказывает более выраженное положительное влияние на метаболические параметры. Анализ результатов работы дает основание рекомендовать применение орлистата, наряду с пиоглитазоном, для коррекции эндокринной функции репродуктивной системы у женщин с СПКЯ и ожирением.
Литература
- DeFronzo R. A. Pharmacologic therapy for type 2 diabetes mellitus, Ann Intern Med. 1999; 131.
- Diamanti-Kandarakis E., Bergiele A.// Int. Assoc. Study Obes. 2001; 2: 231238.
- Dunaif A. // Endocr. Rev. 1997; 18: 774-800.
- Franks S. Polycystic Ovary Syndrome// N Engl J Med. 1995; 333: 13: 853-861.
- Gegick C. G, Altheimer M. D. Comparison of effects of thiazolidinediones on cardiovascular risk factors: observations from a clinical practice //Endocr Pract. 2001; 7: 162-169.
- Glueck C. J., Moreira A. et al. // Hum Reprod. 2003; 18: 1618-1625.
- Glueck C. et al. //Expert Opin Pharmacother. 2002; 3: 1177-1189.
- Hauner H. The mode of action of thiazolidinediones//Diabetes Metab Res Rev 2002; 18: 10-15.
- Hollander P.//In Office Management of Obesity, Ed. By G. Bray, 2004. 187-201.
- Holte J., Bergh T. et al. //J Clin Endocrinol Metab.1995; 80: 25862593.
- Hubber-Buchholz M. M., Carrey D. G. et al.//J Clin Endocrinol Metab. 1999; 84: 1470-1474.
- King A. B. //Diadetec Care. 2000; 23: 557-557.
- Lazurova I., Draveska I., Kraus V., Petrovicova J.// Bratisl. Lek. Listy. 2004. 105. 207-210.
- Moghetti P., Castello R., Negri C. et al.// J Clin Endocrinol Metab. 1996; 81: 881-886.
- Moran L. J., Noakes M. et al.// J Clin Endocrinol Metab. 2003; 88: 812919
- Nestler J. E., Powers L. P., Matt D. W. et al.// J Clin Endocrinol Metab. 1991; 72: 83-89.
- Nestler J. E. //N Engl J Med. 1999; 340: 1314-1320.
- Norman R. J., Masters S. C., Hague W., Beng C., Pannall P., Wang J. X. Metabolic approaches to the subclassification of polycystic ovary syndrome//Fertil Steril. 1995; 63: 329335
- Pasquali R. et al. // Human Reproduction Update. 2003; 9: 359372.
- Reginato M. J., Lasar M. A.//Trends Endocrinol Metab. 1999; 10: 9-13.
- Revised 2003 consensus on diagnostic criteria and long-term heals risks related to polycystic ovary syndrome (POOS)//Hum Reprod. 2004; 19: 41-47.
- Romualdi D., Guido M. et al.//Hum. Repr. 2003; 18: 1210-1218.
- Sebire N. J., Jolly M. et al. //Int J Obes Relat Metab Disord. 2001; 25: 1175-1182.
- Wirth A. //Diab. Obes. Metab. 2005; 7: 21-22.
- Zaadstra B. M., Seidell J. C., Van Noord P. A. et al. Fat and female fecundity: prospective study of effect of body fat ... //Br. Med. J. 1993; 306: 484487.
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


