
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
- Новини 26.10.2021 Аппаратура для УЗИ: применение, принципы работы, разновидности
- Новини 23.10.2021 Интимная пластика после родов: когда необходима операция
Клинический опыт применения препарата Вабадин (симвастатин) для коррекции дислипидемии в условиях клинической практики
Додати статью Роздрукувати
Ингибиторы 3-гидрокси-3-метилглютарил-коэнзим-А (HMG-CoA/ГМГ-КоА) редуктазы (статины) наряду с аспирином и блокаторами бета-адренорецепторов составляют основу вторичной профилактики ишемической болезни сердца (ИБС).
Более четверти века эти препараты остаются наиболее эффективными средствами для коррекции нарушений липидного обмена. За последние десятилетия были получены убедительные доказательства положительного влияния статинов на прогноз больных, имеющих сердечно-сосудистую патологию, связанную с атеросклерозом. Симвастатин, первый полусинтетический препарат группы статинов, был синтезирован в 80-х гг. прошлого столетия. До настоящего времени симвастатин остается одним из наиболее изученных и назначаемых статинов, несмотря на то, что позднее появились другие, в том числе и более мощные гиполипидемические средства. С симвастатином связаны первые крупнейшие клинические исследования, которые определили основные показания для назначения статинов, продемонстрировали положительное влияние препаратов на прогноз больных ИБС и способность предотвращать развитие сердечно-сосудистых осложнений [10, 11, 14]. Такими классическими считаются Скандинавское исследование (4S) и НРS (Heart Protection Study).
В Скандинавском исследовании приняли участие 4444 больных ИБС с повышенным уровнем холестерина. Пациентов разделили на две группы — группу применения симвастатина и группу применения плацебо. Начальная доза препарата составляла 20 мг в сутки. Под контролем показателей липидного обмена у части больных ее увеличивали до 40 мг. Наблюдение за больными продолжалось в среднем до 5,4 года. Активная терапия симвастатином сопровождалась снижением показателей общей и сердечнососудистой смертности на 30 и 42 % соответственно. Результаты 4S не только продемонстрировали высокую гиполипидемическую эффективность и, что не менее важно, безопасность длительного приема препарата, но и сыграли революционную роль в формировании современной концепции лечения больных ИБС, поскольку были получены неоспоримые доказательства положительного влияния статинов на прогноз пациентов с ИБС и гиперхолестеринемией. Десять лет спустя авторы Скандинавского исследования представили отдаленные результаты наблюдения за больными, участвовавшими в 4S. Оказалось, что 82,2 % больных, начавших прием симвастатина, продолжили его в дальнейшем. Более 70 % пациентов из группы плацебо после завершения основного исследования начали принимать симвастатин. Однако больные, начавшие лечение симвастатином в более ранние сроки, во время исследования, в итоге имели более благоприятный прогноз и более низкий показатель смертности — 3,6 % против 4,9 % соответственно [1, 13].
НРS до настоящего времени остается одним из наиболее масштабных клинических исследований прогностической эффективности статинов. В нем участвовали более 20 с половиной тысяч человек [2, 3, 11]. Это проспективное рандомизированное исследование было выполнено с использованием классического протокола, включавшего плацебоконтроль и длительное, в среднем 5,5 года, наблюдение. Существенной особенностью НРS было его независимое финансирование. Руководили исследованием Совет медицинских научных исследований Великобритании (MCR) и Британский кардиологический фонд (BHF). В НРS включали больных в возрасте 40–80 лет с высоким риском осложнений ИБС: перенесших инфаркт миокарда (ИМ), имеющих другие проявления ИБС и/или признаки атеросклеротического поражения некоронарных артерий (церебральных и периферических), сахарный диабет или артериальную гипертензию. При этом уровень общего холестерина (ХС) мог варьировать в достаточно широких пределах, нижняя граница — 3,5 ммоль/л. В исследовании участвовали достаточно большие группы женщин, лиц старше 70 лет, больных с сахарным диабетом и атеросклерозом некоронарной локализации. Симвастатин назначался всем пациентам в дозе 40 мг в сутки. В контрольной группе получали плацебо. Назначение симвастатина сопровождалось снижением частоты основных сердечнососудистых событий (ИМ, инсультов, потребности в оперативной реваскуляризации миокарда). В целом в процессе терапии суммарный показатель риска сердечно-сосудистых осложнений снизился на 24 %. Положительные результаты наблюдались во всех исследуемых подгруппах пациентов, независимо от пола и возраста, а также, что особенно важно, независимо от исходного уровня ХС, его фракций, холестерина липопротеинов низкой плотности (ХС ЛПНП). Подтвердилась гипотеза о благоприятном влиянии симвастатина на прогноз больных с патологией, которая считается эквивалентной ИБС по риску возможных сердечно-сосудистых осложнений, включая сахарный диабет и атеросклероз некоронарных сосудов. Например, у больных диабетом, которые на момент включения в исследование не имели признаков ИБС, риск возникновения первого сердечно-сосудистого осложнения уменьшался на треть. Прием симвастатина сопровождался снижением количества мозговых инсультов на 27 %. Причем, учитывая статистические данные и достаточно большое количество инсультов, развившихся непосредственно в течение периода наблюдения, можно с уверенностью утверждать, что терапия симвастатином снижает частоту ишемических инсультов и не увеличивает риск геморрагических, чего опасались ранее [4, 11]. В ходе исследования было отмечено уменьшение на 38 % риска появления/прогрессирования клинических симптомов атеросклероза периферических артерий (перемежающейся хромоты). Различия в частоте значимых сердечно-сосудистых событий стали достоверными уже в течение второго года исследования и увеличивались в процессе дальнейшего наблюдения. На момент начала НРS вопрос о целесообразности назначения статинов больным ИБС с нормальным уровнем ХС оставался нерешенным. Вместе с тем такие пациенты с ИБС не редкость. Среди участников исследования лиц с относительно невысоким или нормальным уровнем ХС оказалось до 33 %. Под влиянием терапии симвастатином у больных с наличием ИБС и других проявлений атеросклероза и нормальными показателями ХС наблюдалось уменьшение количества сердечнососудистых осложнений (включая инфаркты, инсульты). Снижение относительного риска возникновения серьезных осложнений у таких пациентов составило 24 %, р = 0,0001. В итоге результаты НРS послужили основанием к пересмотру стандартов лечения больных с высоким риском развития осложнений атеросклероза, независимо от исходного уровня холестерина. Современные руководства по лечению ИБС рекомендуют статины всем пациентам с подтвержденным диагнозом при отсутствии противопоказаний.
Благоприятное влияние статинов на прогноз связано с многогранным воздействием на различные звенья патогенеза атеросклеротического процесса. Антиатеросклеротическое действие симвастатина было показано как в экспериментальных, так и в клинических исследованиях, включая достаточно масштабные. Например, в исследованиях MAAS (симвастатин 20 мг/сут), НАТS (симвастатин + ниацин) наблюдалось не только существенное снижение уровней холестерина и холестерина ЛПНП, но и достоверное антиатеросклеротическое действие препарата. Активная терапия сопровождалась замедлением прогрессирования атеросклероза у больных ИБС и частичной редукцией изменений в коронарных артериях. Особенно убедительными были результаты исследования MAAS, 1994 г. В исследовании участвовал 381 больной с повышенным уровнем ХС и поражением не менее 2 артерий по данным коронарографии. Основная группа больных получала симвастатин 20 мг 1 раз в сутки. Контрольная группа — плацебо. Средний срок наблюдения — 4 года. Диетические рекомендации в обеих группах не носили стандартного и обязательного характера. К концу наблюдения под влиянием симвастатина ХС снизился на 32 %, ХС ЛПНП — на 38 %, аполипопротеин В — на 12 %. При этом прогрессирование атеросклеротических изменений по данным коронарографии наблюдалось у 32 % больных контрольной группы и только у 23 % больных в основной. Обратное развитие атеросклеротических изменений было отмечено у 19 % пациентов основной группы и у 12 % — контрольной. В соответствии с различиями в динамике изменений коронарных артерий в группе плацебо наблюдалось большее число сердечно-сосудистых осложнений. Так, инфаркт миокарда перенесли 11 пациентов в контрольной группе и 7 — в основной.
Действие симвастатина связано с обратимой блокадой ГМГ-КоА-редуктазы [5, 10]. Названный фермент обеспечивает превращение HMG-CoA в мевалонат. Его блокада замедляет биосинтез холестерина. Основным местом действия статинов является печень. Торможение синтеза и уменьшение внутриклеточных запасов ХС в печени ведет к восстановлению/повышению функции клеточных рецепторов к липопротеинам низкой плотности, увеличению их катаболизма, повышению печеночного клиренса и снижению в плазме крови уровней общего ХС и его фракций (ЛПНП, ЛПОНП). Считают также, что препарат снижает печеночный синтез и секрецию аполипопротеинов В-100 и липопротеинов с высоким содержанием триглицеридов (ТГ). По химической структуре симвастатин является производным ловастатина — препарата, полученного из грибка Aspergillus terreus. Симвастатин — липофильное соединение. Препарат представляет собой неактивный лактон-пролекарство, который в организме подвергается гидролизу, после чего приобретает фармакологическую активность. После всасывания из желудочно-кишечного тракта и гидролиза до 85 % активного вещества захватывается печенью и лишь 5 % активных метаболитов попадают в системный кровоток. Максимальный фармакологический эффект регистрируется после 4–8-недельной терапии. Метаболическая блокада фермента ГМГ-КоА-редуктазы ограничивает процесс синтеза ХС на ранних этапах и не вызывает накопления в организме токсичных стероидных производных. Симвастатин метаболизируется системой печеночных цитохромов Р450 СYР3А4, что объясняет возможность межлекарственных взаимодействий с препаратами, влияющими на активность этих ферментов. В результате подобных взаимодействий могут значительно изменяться фармакокинетические характеристики симвастатина, биодоступность, длительность действия и т.д. В клинической практике препарат использовали в дозах от 10 до 80 мг, рекомендованный режим приема — один раз в сутки. Терапевтические дозы симвастатина, которые применялись в наиболее масштабных клинических исследованиях, составляют 20–40 мг/сут. Увеличение дозы препарата целесообразно проводить с интервалом в 4 недели под контролем лабораторных показателей.
Первоочередной задачей современной липидоснижающей терапии является влияние на повышенный уровень общего холестерина и его фракцию ЛПНП [8, 9], поскольку именно эти показатели прямо коррелируют с риском атеросклероза и связанных с ним сердечно-сосудистых осложнений. Их снижение в процессе лечения до целевых значений сопровождается достоверным улучшением прогноза заболевания. Общепринятыми в настоящее время целевыми уровнями для больных ИБС считаются показатели общего ХС < 4,5 ммоль/л, ХС ЛПНП < 2,5 ммоль/л. Выбор лекарственного препарата для коррекции липидных нарушений определяется эффективностью его воздействия на целевые показатели. По данным клинических исследований, симвастатин в терапевтических дозах 20–40 мг/сут снижает уровень общего холестерина в среднем на 23–27 % и ХС ЛПНП — на 27–48 %. Выраженность влияния препарата на показатели липидного обмена носит дозозависимый характер. Каждое удвоение дозы препарата, начиная с 20 мг в сутки, позволяет дополнительно снизить уровень ХС ЛПНП на 6–7 %. В случаях умеренного повышения общего холестерина и ХС ЛПНП (до 30 % выше нормы) назначение симвастатина оказывается вполне достаточным для достижения целевых значений указанных показателей.
Эффективность симвастатина доказана у больных с гетерозиготной семейной и несемейной/приобретенной гиперхолестеринемией типа ІІА и ІІБ по классификации D. Fredrickson (ВОЗ, 1970), наиболее часто встречающимися вариантами дислипидемий. Достичь существенного снижения ХС ЛПНП (не менее чем на 20 %) оказалось возможным у 70 % больных с гиперхолестеринемией ІІА типа. У больных с семейной, наследственной гетерозиготной формой гиперхолестеринемии на фоне приема препарата удваивалось количество ЛПНП-рецепторов при незначительном изменении скорости синтеза ЛПНП. Положительные результаты были получены при использовании симвастатина для коррекции вторичной гиперлипидемии у больных с сахарным диабетом и нефротическим синдромом. Статины не только снижают уровень ХС ЛПНП, но и благоприятно влияют на качественный состав фракций ХС, уменьшая количество его наиболее атерогенных субфракций, состоящих из мелких липопротеиновых частиц повышенной плотности. Хотя и в разной степени, статины снижают уровень триглицеридов и оказывают влияние на ХС липопротеинов высокой плотности (ЛПВП) [5, 10]. Степень влияния симвастатина на концентрацию триглицеридов определяется их исходным уровнем и более выражена при значительной гипертриглицеридемии. В среднем на фоне регулярной терапии регистрировалось снижение уровня ТГ на 10–40 %. Статины, в том числе и симвастатин, вызывают умеренное повышение ЛПВП, на 5–15 %. Существуют данные о снижении под влиянием терапии симвастатином липопротеинов, содержащих белки апоВ и апоЕ, связанных с риском развития ИБС и ее осложнений [10].
Помимо прямого действия на липидный обмен статины оказывают влияние на целый ряд процессов, связанных с формированием и прогрессированием атеросклероза. К ним относят противовоспалительное, антиоксидантное и антитромботическое действие, нормализующее влияние на функцию эндотелия, пролиферацию гладкомышечных элементов сосудистой стенки, апоптоз. Дополнительно статины оказывают влияние на некоторые кардиологические синдромы, не связанные непосредственно с атеросклерозом. Например, статины, включая симвастатин, способствовали регрессированию гипертрофии левого желудочка. В исследовании De Sutter и соавт. прием статинов сопровождался улучшением прогноза у больных с тяжелыми желудочковыми нарушениями ритма. Причем после 4 лет наблюдения частота пароксизмов фибрилляции сердца и желудочковых тахикардий в этом исследовании была более чем в 2 раза ниже при условии лечения гиполипидемическими средствами (22 % против 57 %, р < 0,01). Рассматривают возможность использования статинов для лечения болезни Альцгеймера и сосудистых деменций. Статины оказывают влияние на другие органы и системы. Существуют данные о возможности предотвращения с помощью статинов остеопороза и переломов костей у лиц пожилого возраста. Считается перспективным использование иммунодепрессивного эффекта статинов. Симвастатин снижает насыщение желчи холестерином и способствует растворению холестериновых камней в желчном пузыре.
Нелипидные эффекты статинов получили название плейотропных [4, 6, 10]. Существование плейотропных эффектов объясняют общим механизмом блокады печеночной 3-гидрокси-3-метилглютарил коэнзим-А-редуктазы. Их биохимическим субстратом являются продукты метаболизма мевалоната, отличные от холестерина (семейство изопреноидов). Считают, что последние вовлечены в регуляторные процессы пролиферации, дифференциации, миграции и апоптоза клеток, экспрессии эндотелиальной NO-синтазы. На фоне использования статинов в клинических и экспериментальных исследованиях наблюдалось снижение уровней С-реактивного протеина (СРП), провоспалительных цитокинов; предотвращение окислительной модификации липопротеинов и повышение концентрации естественных антиоксидантов. Клинические исследования подтверждают, что уменьшение концентрации СРП под влиянием терапии статинами оказывает достоверное влияние на прогноз пациентов. Эти факты позволяют считать, что показатели общего ХС, ХС ЛПНП и СРП являются взаимодополняющими маркерами эффективности статиновой терапии, и подтверждают гипотезу о клиническом значении нелипидных механизмов действия статинов. Имеются данные о противодействии статинов эффектам ангиотензина II. Под влиянием статинов отмечено уменьшение концентрации фибриногена, ингибитора активатора плазминогена 1, снижение вязкости крови [6]. Антиагрегантные свойства статинов частично связывают с уменьшением содержания холестерина в фосфолипидах мембран тромбоцитов. В экспериментах наблюдали медиаторную активность статинов в отношении процессов васкулогенеза, в том числе коронарных сосудов. Влияние статинов у больных сахарным диабетом 2-го типа, вероятно, носит прямой патогенетический характер, поскольку эти препараты повышают чувствительность тканей к инсулину, нарушение которой лежит в основе развития заболевания [12].
Учитывая высокую эффективность и безопасность симвастатина, на фармацевтическом рынке в настоящее время существует достаточно большое количество его препаратов-генериков. Один из них — препарат Вабадин производства фирмы Берлин-Хеми АГ (Менарини Групп). Это лекарственное средство использовали для коррекции нарушений липидного обмена у больных ИБС на базе отделения хронической ишемической болезни сердца Института кардиологии имени академика Н.Д. Стражеско. В группу наблюдения были включены 45 пациентов, 33 мужчины и 12 женщин, с диагнозом ИБС, стабильная стенокардия. Все пациенты с учетом диагноза имели повышение общего холестерина выше целевого уровня (> 4,5 ммоль/л). Завершили исследование 44 больных. Одна из участниц прервала лечение по собственному желанию. Вабадин назначали в дозе 20 мг 1 раз в сутки. Доза выбиралась как относительно невысокая, но имеющая, по данным крупных клинических исследований, доказанную терапевтическую эффективность. Средний возраст пациентов — 59,1 ± 2,2 года. Длительность терапии Вабадином составила 30 дней. Учитывая результаты крупных клинических исследований симвастатина 4S и HPS, эффективность исследуемого препарата считалась достаточной при снижении общего ХС и ХС ЛПНП не менее чем на 1,0 ммоль/л. В качестве целевых уровней рассматривались общепринятые показатели общего ХС < 4,5 ммоль/л и ХС ЛПНП < 2,5 ммоль/л.
По результатам нашего исследования Вабадин оказался эффективным у 38 из 44 больных (86,3 %). Целевые уровни общего ХС и ХС ЛПНП при назначении 20 мг препарата в сутки были достигнуты у 28 из 44 пациентов (63,6 %). Уровень общего ХС под воздействием препарата снизился с 6,39 ± 0,29 до 4,71 ± 0,28 ммоль/л, т.е. в среднем на 26,3 %, p < 0,01; ХС ЛПНП — с 4,41 ± 0,37 до 3,08 ± 0,15 ммоль/л (на 30,2 %), p < 0,01. Следует отметить, что полученные результаты, учитывая их количественные параметры, соответствуют данным существующих клинических исследований по гиполипидемической эффективности симвастатина. Исходный уровень триглицеридов наших пациентов был повышен незначительно, средний показатель — 1,87 ± 0,27 ммоль/л, что объясняет отсутствие его достоверной динамики на фоне лечения — 1,45 ± 0,19 ммоль/л, р > 0,2. Значимого влияния на показатель ХС ЛПВП также не наблюдалось, отмечена незначительная тенденция к его повышению. Прирост концентрации ХС ЛПВП за период наблюдения составил всего 0,06 ммоль/л, что вполне объяснимо с учетом невысокого уровня ТГ и короткого курса терапии. Динамика основных лабораторных показателей под влиянием терапии представлена на диаграмме (рис. 1).
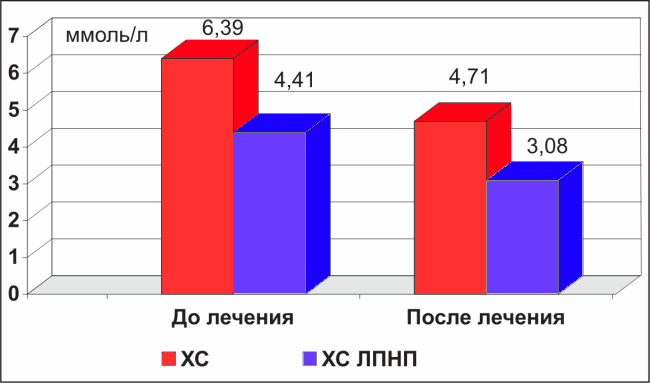
Рисунок 1. Динамика показателей общего ХС и ХС ЛПНП под влиянием 30-дневной терапии препаратом Вабадин (симвастатин) 20 мг/сут.
Изменения стандартов лечения больных с проявлениями атеросклероза и расширение показаний для назначения статинов требуют более жестких критериев для определения безопасности подобной терапии. По результатам наиболее масштабных исследований 4S и HPS, симвастатин продемонстрировал хорошую переносимость и высокий уровень безопасности [3, 11, 14]. Так, среди больных HPS риск миопатии составил 0,01 % в год. В данном исследовании, в котором общее количество пациентов составляло более 20 000 человек, признаки миопатии были обнаружены лишь у 10 пациентов из группы леченных симвастатином и у 4 — из группы плацебо. Все случаи миопатии закончились выздоровлением. Примерно у 6 % больных в течение всего периода наблюдения отмечались необъяснимые мышечные боли, в то же время достоверных различий между основной и контрольной группами, включая частоту повышения креатинфосфокиназы, не было. Вместе с тем миопатии/рабдомиолиз были зарегистрированы при монотерапии различными статинами [5]. Диагноз рабдомиолиза подразумевает 10-кратное и более повышение уровня креатинкиназы в сопровожении таких клинических симптомов, как мышечные боли, слабость, миоглобинемия, развитие острой почечной недостаточности. Механизм, ответственный за миотоксичность статинов, окончательно не установлен, существуют предположения о нарушении структуры клеточных мембран на фоне снижения холестерина. Вероятность миотоксичности статинов возрастает при сопутствующем назначении некоторых других лекарственных средств, включая циклоспорин, фибраты (гемфиброзил), никотиновую кислоту, антибиотики-макролиды (эритромицин), ингибиторы протеаз (нефазодон), иммунодепрессанты. Имеющаяся почечная недостаточность может быть фактором, повышающим миотоксичность статинов.
Потенциальная гепатотоксичность статинов специально изучалась в нескольких крупных клинических исследованиях [5, 10]. При использовании всех имеющихся препаратов этой группы наблюдались случаи повышения уровней печеночных трансаминаз. Однако гепатотоксичность, определяемая как более чем троекратное повышение уровней печеночных ферментов, регистрировалась менее чем в 2 % cлучаев. Поскольку нарушения функции печени наиболее часто наблюдаются в течение первых 4–12 месяцев лечения, при изменении дозы препарата, а также на фоне предшествующей патологии печени необходим соответствующий врачебный и лабораторный контроль. Суммируя данные, касающиеся безопасности длительной терапии симвастатином, следует отметить, что в исследованиях 4S и HPS увеличение выживаемости больных не сопровождалось ростом смертности от других заболеваний, не связанных с атеросклерозом и ИБС.
В нашем исследовании препарат Вабадин имел хорошую переносимость. Побочные явления наблюдались у 5 из 44 больных, причем четкую связь с приемом препарата отметили только двое из них. Через несколько дней после начала приема препарата у них появились диспептические расстройства, дискомфорт в животе, метеоризм. Указанные явления были незначительно выраженными и не потребовали прекращения лечения. Один из этих больных на фоне приема симвастатина отметил периодические нарушения сна. Однако подобные расстройства с ним случались и ранее. Потребности досрочного прекращения терапии в этом случае также не возникло. В течение месячного наблюдения за нашими пациентами не отмечалось изменений лабораторных показателей, включая печеночные трансаминазы, креатинкиназу, креатинин, глюкозу крови.
В заключение следует отметить, что симвастатин остается надежным, хорошо изученным, эффективным и безопасным препаратом для коррекции нарушений липидного обмена. Препарат оказывает благоприятное влияние на прогноз и рекомендован для вторичной профилактики больным ИБС. Учитывая экономическую составляющую терапии таких пациентов, представляется важной возможность выбора качественных и доступных лекарственных средств среди генерических препаратов. Препарат Вабадин (симвастатин) производства компании Берлин-Хеми АГ (Менарини Групп) по результатам нашего наблюдения продемонстрировал достаточную гиполипидемическую эффективность, которая по количественным параметрам соответствует результатам крупных клинических исследований, а также хорошую переносимость.
Список литературы
- Аронов Д.М. Каковы результаты лечения симвастатином при длительном (более 10 лет) применении? Возникает ли толерантность к симвастатину? Каковы плеотропные эффекты статинов? // Лечащий врач. — 2001. — № 5–6.
- Волков В.И. Фармакотерапия атеросклероза: решенные и нерешенные вопросы // УКЖ. — 2003. — № 4. — С. 125-134.
- Грацианский Н.А. Уроки церивастатина и результаты исследования «Защита сердца» // Consilium medicum. — 2003.— Т. 4, № 3.
- Затейщиков Д.А. Лечение атеросклероза: насколько важно действие статинов на уровень холестерина? // Фарматека. — 2003. — № 6. — С. 39-43.
- Метелица В.И. Справочник по клинической фармакологии сердечно-сосудистых лекарственных средств. — М.: Бином, 2002. — С. 551-619.
- Bellosta S., Ferri N., Paoletti R., Corsini A. Non-lipidrelated effects of statins // Ann. Med. — 2000. — Vol. 32. — P. 164-176.
- Di Napoli P., Taccardi A., Oliver M., De Caterina R. Statins and stroke: evidence for cholesterol-independent effects // Eur. Heart J. — 2002. — Vol. 23. — P. 1908-1921.
- European guidelines on cardiovascular disease prevention in clinical practice. Third Joint Task Force of European and other Societies on Cardiovascular Disease Prevention in Clinical Practice // Eur. Heart J. — 2003. — Vol. 24. — P. 1601-1610.
- ESC Guidelines for the Management of Stable Angina Pectoris // Eur. Heart J. — 2006. — 27. — 1341-1381.
- Gotto A.M. Contemporary Diagnosis and Management of Lipid Disorders. — 2001. — 236 p.
- Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol lowering with simvastatin in 20 536 high-risk individuals: a randomized placebo-controlled trial // Lancet. — 2002. — 360. — 7-22.
- McFariane S.I., Banerji M., Sowers J.R. Insulin resistance and cardiovascular disease // J. Clin. Endocrinol. Metab. — 2001. — Vol. 86. — P. 713-718.
- Pedersen T.R., Berg K. Safety and tolerability of cholesterol lowering with simvastatin during years in the Scandinavian simvastatin survival study // Arch. Int. Med. — 2000. — Vol. 176. — P. 1976-1984.
- The Scandinavian Simvastatin Survival Study group. Randomized trial of cholesterol lowering in 4444 patients with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S) // Lancet. — 1994. — Vol. 344. — P. 1383-1389.
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»




