
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 11.10.2024 Штучний інтелект у фармації: перспективи, переваги та потенційні ризики
- Новини 27.08.2024 Вакансії медсестри у Вінниці: особливості та вимоги до кандидатів
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
Вплив препарату Мелаксен на динаміку 6-сульфатоксимелатоніну в сечі у хворих на хронічне обструктивне захворювання легень у сполученні з гастроезофагеальною рефлюскною хворобою
Фадєєнко Г.Д., Крахмалова О.О., Каменір В.М., Ізмайлова О.В. ДУ «Національний інститут терапії імені Л.Т.Малої НАМН України»
Останнім часом все частіше висловлюється думка про те, що в поєднаних механізмах патогенезу різних захворювань, а саме хронічного обструктивного захворювання легень (ХОЗЛ) у сполученні з гастроезофагеальною рефлюксною хворобою (ГЕРХ) велику роль грає дисбаланс біологічно активних речовин, а саме гормон епіфіза - мелатонін (Мт).
Мт бере участь у забезпеченні багатьох життєво важливих фізіологічних процесів, таких як імунна відповідь, метаболізм вільних радикалів, регуляція настрою і сну, проліферація і диференціювання клітин та інi. Інтенсивність метаболізму Мт залежить від рівня освітленості [29] його синтез і секреція посилюється в темний час доби і пригнічується в денні години, таким чином, Мт приймає участь у циркадних ритмах і регуляції різних функцій організму. Відсутність у літературі достатніх даних про особливості секреції Мт на тлі ХОЗЛ у поєднанні з ГЕРХ послужило підставою для проведення цього дослідження.
Мета роботи: вивчити зміну рівня Мт у пацієнтів з ХОЗЛ у поєднанні з ГЕРХ.
Матеріали і методи дослідження: діагноз ХОЗЛ верифікували з урахуванням критеріїв Global Initiative for Chronic Obstructive Lung Disease GOLD та відповідно до наказу МОЗ України № 128 від 19.03.2007г, діагноз ГЕРХ у пацієнтів з ХОЗЛ верифікували з урахуванням Монреальського консенсусу, Гштадського керівництва по стратегії лікування ГЕРХ. Для діагностики форми ГЄРХ (ендоскопічно негативна ( НЕРХ ) або ендоскопічно позитивна (ЕРХ ступінь А, В, С, стравохід Баретта), проводилася ендоскопія з використанням відеоендоскопа фірми «Olimpus» GIF -V- 70 і « Fuginon » WG- 88FP . Ступінь вираженості рефлюкс езофагіту (РЕ ступінь А , В, С) оцінювалася згідно Лос- Анджелеської класифікації.
З метою вивчення рівня Мт при ХОЗЛ у поєднанні з ГЄРХ було досліджено зміст рівня його метаболіту - 6 - сульфатоксимелатоніну (6 - СОМ). Концентрацію 6 - СОМ досліджували в ранковій сечі, за допомогою імуноферментного аналізу ELIZA (Enzyme Linked Immuno Sorbent Assay). Це діагностичний in vitro тест, який заснований на методиці імуноферментного аналізу (ІФА), метод кількісного визначення антигенів і антитіл. Використовувався стандартний набір реагентів 6 - Sulfatoxymelatonin ELIZA (BUHLMANN LABORATORIES AG , Switzerland) Зважаючи на той факт, що синтез Мт залежить від рівня освітлення, перед забором проб, на визначення 6 - СОМ, хворих попереджали про неприпустимість включення освітлювальних приладів протягом нічного періоду, що передує ранковому забору проб [13]. Так само Мт має здатність впливати на елементи жіночого репродуктивного здоров'я, де він регулює секрецію статевих гормонів і внаслідок цього його рівень може змінюватися в залежності від фази менструального циклу жінки. Враховуючи ці особливості, забір сечі проводили в першій фазі менструального циклу, тоді коли його коливання мінімальні [13,14,15].
Усього під час дослідження було обстежено 131 пацієнта, з яких 62 були хворі на ХОЗЛ у поєднанні з ГЄРХ та 39 - на ізольовану ГЄРХ. Контрольну групу склали 30 практично здорових осіб.
Критерії включення в дослідження: наявність ознак ГЕРХ (печія 2 рази на тиждень і більше, регургітація або виявлення при відеоендоскопіЇ ознак ураження стравоходу; встановлений діагноз ХОЗЛ; У дослідження не включалися пацієнти за наявності у них хоч одного з перерахованих станів: органічні захворювання шлунково -кишкового тракту і системи органів дихання, інфікування H.Pilory, бронхіальної астма, артеріальна гіпертензія, ішемічна хвороба серця, туберкульоз, психічні захворювання, аутоімунні захворювання, цукровий діабет, зловживання алкоголем, вагітніст , відмова пацієнта від участі в дослідженні.
Залежно від схеми лікування, пацієнтів основної групи розподілили на дві підгрупи: 1а та 1б.
Підгрупа 1а отримувала ІПП – пантопразол у дозі 40 мг на добу + стандартну терапію ХОЗЛ (β2-агоністи короткої та тривалої дії, М-холінолітики, ІГКС та ін.) + «Мелаксен» – 3 мг на добу;
Підгрупа 1б так само отримувала пантопразол у дозі 40 мг на добу + стандартну терапію ХОЗЛ . Курс лікування склав 4 тижні.
Пацієнти групи порівняння отримували пантопразол – 40 мг на добу протягом 4-х тижнів.
Результати дослідження та їх обговорення: з метою визначення нормативних показників враховувались межі розподілу концентрації 6-СОМ у групі практично здорових осіб у форматі X ±d, які склали 29,50 ± 10,5 нг/мл.
Середній рівень концентрації 6-СОМ в сечі до проведеного лікування у групі з поєднаною патологією склав (14,66 ± 8,62) нг/мл, а у групі з ізольованою ГЕРХ – (20,78 ± 10,13) нг/мл. Ці дані представлені на рис. 1.
Як демонструють дані на рис. 1, рівень 6-СОМ у 1-й групі був достовірно, в 1,4 разу (14,66 ± 8,62 і 20,78 ± 10,13 нг/мл) нижчим, ніж у групі з ізольованою ГЕРХ (р = 0,002).
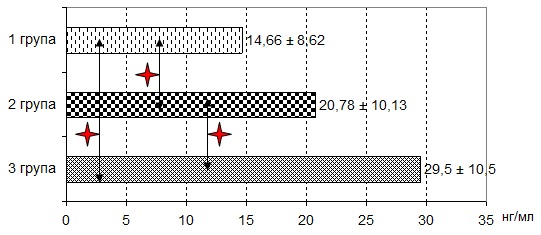
Рис. 1. Порівняльна характеристика концентрації 6-СОМ у групах
Примітка:  – статистично достовірна міжгрупова різниця (р = 0,002).
– статистично достовірна міжгрупова різниця (р = 0,002).
При вивченні концентрації 6-СОМ у досліджуваних пацієнтів порівнювали дані, отримані в результаті проведеного лікування (рис.2).
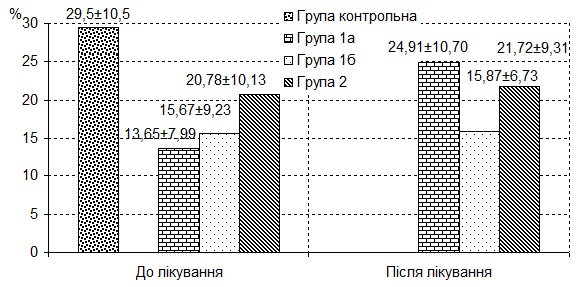
Рис. 2. Зміна рівня 6-СОМ у досліджуваних групах після проведеного лікування (нг/мл).
Було виявлено, що в пацієнтів підгрупи 1а, які додатково приймали «Мелаксен» концентрація 6-СОМ достовірно збільшилася в 1,7 раза в порівнянні з результатами до лікування (13,65 ± 7,99 і 24,91 ± 10,70 нг/мл) (р = 0,001) (рис. 3).
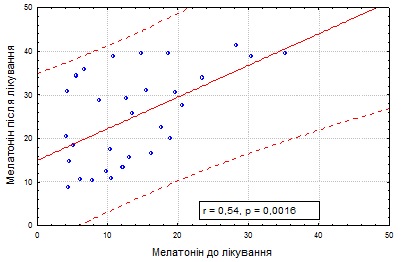
Рис. 3. Динаміка рівня 6-СОМ після проведеного лікування у хворих підгрупи 1а.
У хворих підгрупи 1б зміни рівня 6-СОМ були недостовірними (15,67 ± 9,23 і 15,87 ± 6,73 нг/мл) (р = 0,922) (рис.4.).
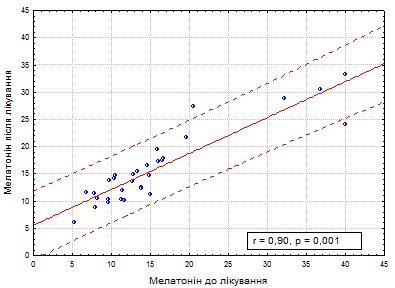
Рис. 4. Динаміка рівня 6-СОМ після проведеного лікування у хворих підгрупи 1б.
При ізольованій ГЕРХ також не відмітили статистично достовірної різниці між показниками до і після лікування (20,78 ± 10,13 і 21,72 ± 9,31 нг/мл) (р = 0,699) (рис. 5).
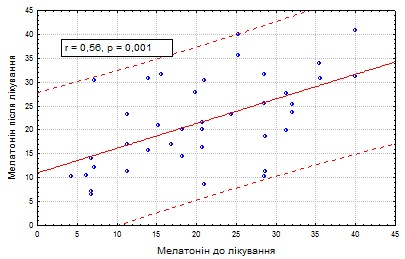
Рис. 5. Динаміка рівня 6-СОМ після проведеного лікування у хворих на ізольовану ГЕРХ.
У групі контролю рівень 6-СОМ склав (29,50 ± 10,5) нг/мл. Порівнюючи концентрацію 6-СОМ у пацієнтів підгруп 1а і 1б з показниками пацієнтів на ізольовану ГЕРХ, отримали такі результати: між значеннями в пацієнтів, які отримували «Мелаксен», і в пацієнтів з ізольованою ГЕРХ достовірних відмінностей не було (24,91 ± 10,70 та 21,72 ± 9,31 нг/мл) (р = 0,39), на відміну від пацієнтів, які не застосовували для свого лікування «Мелаксен», у них рівень 6-СОМ був у 1,3 раза нижчий, ніж у пацієнтів групи порівняння (15,87 ± 6,73 і 21,72 ± 9,31 нг/мл) (р = 0,005). Аналізуючи результати після проведеного лікування, визначили, що рівень 6-СОМ у пацієнтів груп 1а і 1б був у 1,1 (24,91 ± 10,70 та 29,50 ± 10,5 нг/мл), (р>0,05) і 1,8 (15,87 ± 6,73 та 29,50 ± 10,5 нг/мл), (р<0,05) раза, відповідно, нижчий, ніж у контролі, й у 1,3 раза нижчий, ніж у пацієнтів з ізольованою ГЕРХ (р> 0,05).
Виходячи з вищевикладених результатів, можна зазначити, що до проведеного лікування рівень 6-СОМ був значно менший у пацієнтів з поєднаною патологією в порівнянні з ізольованою ГЕРХ та контрольною групою. Після проведеного лікування рівень 6-СОМ достовірно збільшився у 1,7 раза в пацієнтів, які додатково до основного лікування отримували «Мелаксен», у пацієнтів же, які його не отримували, достовірних змін у концентрації 6-СОМ виявлено не було (р = 0,0016, r = 0,54).
Було проведено аналіз показників, отриманих після лікування, залежно від форми ГЕРХ (рис. 6).
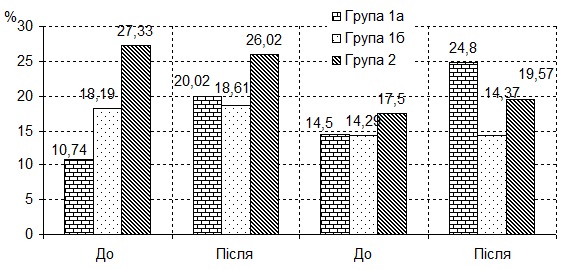
Рис. 6. Показники рівня 6-СОМ (в залежності від форми ГЕРХ) у пацієнтів досліджуваних груп до і після лікування.
Як представлено на рис. 6, при НЕРХ рівень 6-СОМ до лікування склав 10,74 ± 4,52 і (18,19 ± 8,60) нг/мл, відповідно, в підгрупах 1а і 1б. Після проведеного лікування ці значення достовірно збільшились у пацієнтів підгрупи, яка приймала «Мелаксен» - в 1,8 раза (10,74 ± 4,52 та 20,02 ± 10,7 нг/мл) (р < 0,05) і незначно - у пацієнтів підгрупи 1б (18,19 ± 8,60 та 18,61 ± 7,06 нг/мл) (р > 0,05). У хворих на ізольовану ГЕРХ рівень 6-СОМ практично не змінився (27,33 ± 8,12 та 26,02 ± 8,49 нг/мл) (р > 0,05). У пацієнтів з ЕРХ підгруп 1а та 1б рівень 6-СОМ склав 14,50 ± 8,63 і (14,29 ± 9,48) нг/мл, відповідно. Після проведеного лікування ці значення достовірно збільшились у пацієнтів підгрупи 1а - в 1,7 раза (14,50 ± 8,63 і 24,80 ± 10,03 нг/мл) (р < 0,05) і практично не змінилися в пацієнтів підгрупи 1б (14,29 ± 9,48 та 14,37 ± 6,22 нг/мл) (р > 0,05). У хворих на ізольовану ГЕРХ збільшилися в 1,1 раза в порівнянні з результатами до лікування (17,50 ± 9,52 і 19,57 ± 9,10 нг/мл) (р > 0,05).
При аналізі показників між підгрупами було показано, що рівень 6-СОМ при НЕРХ у пацієнтів підгрупи 1а в 1,07 раза (20,02 ± 10,7 і 18,61 ± 7,06 нг/мл) перевищував цей же показник у пацієнтів підгрупи 1б (р = 0,74); по відношенню до значень групи з ізольованою ГЕРХ у підгрупі, яка приймала «Мелаксен» він був менший в 1,2 раза (20,02 ± 10,7 і 26,02 ± 8,49 нг/мл) (р = 0,185), у хворих, які його не отримували, - у 1,3 раза (18,61 ± 7,06 і 26,02 ± 8,49 нг/мл) (р = 0,031). Рівень 6-СОМ у підгрупах 1а і 1б був у 1,4 і 1,5 раза (20,02 ± 10,7 проти 29,50 ± 10,5 нг/мл; 18,61 ± 7,06 проти 29,50 ± 10,5 нг/мл), відповідно, менший, ніж у контролі, а в пацієнтів з ізольованою ГЕРХ практично наблизився до нормальних значень (26,02 ± 8,49 і 29,50 ± 10,5 нг/мл). При ЕРХ рівень 6-СОМ в пацієнтів підгрупи 1а в 1,7 раза (24,80 ± 10,03 і 14,37 ± 6,22 нг/мл) перевищував цей же показник у пацієнтів 1б (р = 0,002); по відношенню до значення групи з ізольованою ГЕРХ у підгрупі «Мелаксен» він був у 1,2 раза більшим (24,80 ± 10,03 і 19,57 ± 9,10 нг/мл) (р = 0,059), у хворих, які не отримували «Мелаксен» - у 1,3 раза менший (14,37 ± 6,22 і 19,57 ± 9,10 нг/мл) (р = 0,034). Рівень 6-СОМ у підгрупах 1а і 1б був у 1,1 і 2,05 раза (24,80 ± 10,03 і 29,50 ± 10,5 нг/мл; 14,37 ± 6,22 і 29,50 ± 10,5 нг/мл), відповідно, менший, а в пацієнтів з ізольованою ГЕРХ – в 1,5 раза (19,57 ± 9,10 і 29,50 ± 10,5 нг/мл) нижчий, ніж у групі контролю.
Згідно з отриманими даними щодо змін 6-СОМ, можна зазначити, що до початку лікування спостерігалося істотне зниження 6-СОМ у групі з ізольованою ГЕРХ при наявності ерозивного ураження СОС, тоді як у пацієнтів з поєднаною патологією статистично достовірних відмінностей 6-СОМ між ЕРХ і НЕРХ виявлено не було, однак його рівень був значно нижчий у цих пацієнтів незалежно від форми ГЕРХ. Після проведеного лікування у пацієнтів, в терапії яких був присутній «Мелаксен», відзначено достовірне його підвищення: при НЕРХ – у 1,8 і при ЕРХ – у 1,7 раза.
При ізольованій ГЕРХ достовірної різниці до і після лікування не виявили як при ерозивному, так і при неерозивному ураженні стравоходу. Також помітили, що зміни в концентрації 6-СОМ були більш значними в пацієнтів, які приймали «Мелаксен», саме при ерозивному ураженні СОС. Рівень 6-СОМ при ЕРХ після лікування перевищив у 1,2 раза ці ж показники при НЕРХ. Пацієнти, які не отримували «Мелаксен», мали протилежний результат: рівень 6-СОМ був у 1,2 раза вищим при НЕРХ в порівнянні з ЕРХ. Подібний результат відзначали й у пацієнтів з ізольованою ГЕРХ: у них рівень 6-СОМ також у 1,3 раза був вищим при НЕРХ. Ці дані дали підставу припустити, що застосування «Мелаксену» в комплексному лікуванні особливо ефективне в плані підвищення концентрації мелатоніну у пацієнтів з ерозивним ураженням СОС, зважаючи на його більш важкий перебіг, що супроводжується розвитком тяжких і загрожуючих життю ускладнень.
Було вивчено зміни рівня 6-СОМ у залежності від ступеня РЕ. В процесі проведеного лікування рівень 6-СОМ змінився таким чином: концентрація 6-СОМ при РЕ А в пацієнтів підгруп 1а і 1б склала 28,16 ± 9,28 і (15,53 ± 6,49) нг/мл, що було в 1,4 і 1,03 раза, відповідно, більше, ніж показники до лікування (19,12 ± 9,85 і 28,16 ± 9,28; 14,95 ± 8,67 і 15,53 ± 6,49 нг/мл) (р < 0,05; р > 0,05), у пацієнтів з ізольованим перебігом ГЕРХ рівень 6-СОМ склав 20,48 ± 9,95 нг/мл, що в 1,1 раза перевищило вихідні показники до лікування (18,34 ± 8,77 проти 20,48 ± 9,95 нг/мл) (р > 0,05) (табл.1).
Таблиця 1
Середні значення рівня 6-СОМ до і після лікування в залежності від ступеня ураження СОС
|
Стадія ГЕРХ. Кількість хворих по групах |
Термін обстеження |
Група хворих |
Стат. показник (Р) |
||||
|
1а |
1б |
2 |
Р1а-1б |
Р1а-2 |
Р1б-2 |
||
|
РЕ А |
до лікування |
19,12±9,85 |
14,95±8,67 |
18,34±8,77 |
0,315 |
0,839 |
0,346 |
|
після лікування |
28,16±9,28 |
15,53±6,49 |
20,48±9,95 |
0,002 |
0,068 |
0,167 |
|
|
РЕ В |
до лікування |
11,51±7,33 |
15,60±11,56 |
20,3±11,9 |
0,422 |
0,105 |
0,471 |
|
після лікування |
24,15±11,60 |
14,16±6,07 |
19,96±8,09 |
0,062 |
0,439 |
0,155 |
|
|
РЕ С |
до лікування |
10,8±4,4 |
6,0±1,1 |
11,29±6,29 |
0,198 |
0,877 |
0,317 |
|
після лікування |
20,05±8,28 |
8,74±3,87 |
16,50±9,08 |
0,123 |
0,515 |
0,315 |
|
При порівнянні показників, які досліджувались, визначили, що у підгрупі 1а після лікування рівень 6-СОМ у 1,8 раза (28,16 ± 9,28 проти 15,53 ± 6,49 нг/мл) перевищував аналогічні показники в пацієнтів, які не отримували мелатонін, і в 1,3 раза (28,16 ± 9,28 проти 20,48 ± 9,95 нг/мл) в пацієнтів з ізольованою ГЕРХ (р = 0,002, р = 0,068). У хворих підгрупи 1б рівень 6-СОМ, навпаки, в 1,3 раза (15,53 ± 6,49 і 20,48 ± 9,95 нг/мл) був меншим, ніж при ізольованому перебігу ГЕРХ (р = 0,167).
При РЕ В рівень 6-СОМ після лікування склав (24,15 ± 11,60) нг/мл у пацієнтів, які додатково до основного лікування отримували «Мелаксен», і (14,16 ± 6,07) нг/мл у хворих, які «Мелаксен» не приймали. Отримані показники в 2 рази перевищували вихідні значення до лікування в пацієнтів підгрупи, яка приймала «Мелаксен» і статистично не змінювалися у пацієнтів підгрупи 1б (15,60 ± 11,56 і 14,16 ± 6,07 нг/мл) (р < 0,05; р > 0,05). При ізольованому перебігу ГЕРХ рівень 6-СОМ склав (19,96 ± 8,09) нг/мл, що статистично не відрізнялося від показників до лікування (20,3 ± 11,9 і 19,96 ± 8,09 нг/мл) (р > 0,05). У пацієнтів підгрупи 1а рівень 6-СОМ у 1,7 раза перевищував аналогічні показники в пацієнтів підгрупи 1б (24,15 ± 11,60 і 14,16 ± 6,07 нг/мл) та в 1,2 раза (24,15 ± 11,60 і 19,96 ± 8,09 нг/мл) у хворих з ізольованим перебігом ГЕРХ (р = 0,062, р = 0,439). У пацієнтів, які не отримували «Мелаксен», різниця з ізольованою ГЕРХ склала 1,4 раза (14,16 ± 6,07 і 19,96 ± 8,09 нг/мл) на користь ізольованого перебігу ГЕРХ (р = 0,155).
Аналізуючи той же показник при РЕ С, концентрація 6-СОМ у пацієнтів підгрупи 1а і 1б склала 20,05 ± 8,28 і (8,74 ± 3,87) нг/мл, відповідно. Рівень 6-СОМ у процесі лікування збільшився в 1,8 раза (10,8 ± 4,4 і 20,05 ± 8,28 нг/мл) у пацієнтів, у схемі лікування яких був присутній «Мелаксен», і в 1,4 раза (6,0 ± 1,1 і 8,74 ± 3,87 нг/мл) у пацієнтів, які «Мелаксен» не застосовували (р < 0,05; р > 0,05). У хворих з ізольованим перебігом ГЕРХ рівень 6-СОМ в процесі проведеного лікування збільшився в 1,4 раза (11,29 ± 6,29 і 16,50 ± 9,08 нг/мл) (р > 0,05).
Порівнюючи показники між групами, визначили, що в пацієнтів підгрупи 1а рівень 6-СОМ у 2,2 раза вищий, ніж у пацієнтів підгрупи 1б (20,05 ± 8,28 і 8,74 ± 3,87 нг/мл), та в 1,2 раза вищий, ніж у пацієнтів з ізольованою ГЕРХ (20,05 ± 8,28 і 16,50 ± 9,08 нг/мл) (р = 0,123, р = 0,515). Рівень 6-СОМ у пацієнтів, які не отримували додатково «Мелаксен», навпаки, був у 1,8 раза менший, ніж у пацієнтів групи 2 (8,74 ± 3,87 і 16,50 ± 9,08 нг/мл) (р = 0,315).
Аналізуючи показники 6-СОМ до і після лікування, отримали прогресивне зниження 6-СОМ у залежності від ступеня тяжкості ураження СОС, після лікування спостерігалася аналогічна закономірність. Підвищення концентрації 6-СОМ з високим ступенем достовірності відрізнялося від показників до лікування в пацієнтів підгрупи 1а. У хворих, які не використовували «Мелаксен», також відмічали збільшення аналогічних показників у залежності від ступеня тяжкості РЕ, однак ці зміни не мали статистично достовірної різниці. У пацієнтів з ізольованою ГЕРХ спостерігали незначне підвищення 6-СОМ після лікування, однак і ці показники також мали чіткий зв'язок із тяжкістю ураження СОС.
Було відзначено: що нижча концентрація 6-СОМ у сечі, то більш глибокі ураження СОС діагностують у цих пацієнтів.
Ці дані можуть свідчити про те, що мелатонін бере участь у патофізіологічних механізмах формування ерозивного ураження стравоходу і може служити маркером ступеня тяжкості РЕ.
У ході дослідження встановлено, що рівень 6-СОМ змінює свою концентрацію в пацієнтів з поєднаною патологією в залежності від ступеня тяжкості ХОЗЛ. Ці дані наведено в таблиці 2.
Результатами, представленими в таблиці 4.7, продемонстровано зміну рівня 6-СОМ у сечі в залежності від ступеня тяжкості ХОЗЛ. Так, при II ступені тяжкості ХОЗЛ рівень 6-СОМ вірогідно в 1,5 (16,40 ± 7,81 і 10,60 ± 8,04 нг/мл) раза перевищував аналогічний показник при III стадії ХОЗЛ і у 1,2 (16,40 ± 7,81 проти 13,07 ± 10,70 нг/мл) раза – при IV (р = 0,009, р = 0,416).
Таблиця 2
Порівняльна таблиця середніх значень рівня 6-СОМ у хворих 1 групи до і після лікування в залежності від стадії ХОЗЛ
|
Група, кількість хворих за стадіями ХОЗЛ |
Стадія ХОЗЛ. Термін обстеження. Статистичний показник (Р) |
||||||||
|
II стадія |
III стадія |
IV стадія |
|||||||
|
до лікув. |
після лікув. |
Р |
до |
після лікув. |
Р |
до |
після лікув. |
Р |
|
|
1а |
16,40± |
24,61± |
0,006 |
13,07± |
22,34± |
0,001 |
15,16± |
28,42± |
0,27 |
|
1б |
17,40± |
17,31± |
0,95 |
12,57± |
12,41± |
0,97 |
6,8 |
11,5 |
– |
|
Стат. показн. (Р1а-1б) |
0,704 |
0,006 |
|
0,334 |
0,020 |
|
– |
– |
|
У процесі проведеного лікування рівень 6-СОМ змінився таким чином: концентрація 6-СОМ у пацієнтів з II ступенем тяжкості ХОЗЛ, які використовували додатково «Мелаксен», склала 24,61 ± 10,74 і (17,31 ± 6,72) нг/мл, а в тих, які не отримували (що було в 1,5 та 1,03 раза, відповідно, більше, ніж показники до лікування) - 16,40 ± 7,81 і 25,93 ± 10,74; 17,40 ± 8,52 і 17,60 ± 6,92 нг/мл (р = 0,006; р = 0,95).
Порівняльний аналіз між групами показав, що в підгрупі «Мелаксену» після лікування рівень 6-СОМ був у 1,4 раза вищим, ніж у пацієнтів, які його не отримували: 25,93 ± 10,74 проти 17,60 ± 6,92 нг/мл) (р > 0,05). При III стадії ХОЗЛ рівень 6-СОМ склав (22,34 ± 10,65) нг/мл у пацієнтів, які додатково до основного лікування отримували «Мелаксен», і (12,41 ± 5,10) нг/мл у хворих, які «Мелаксен» не приймали. Отримані показники в 2,4 раза (8,98 ± 5,23 і 22,34 ± 10,65 нг/мл) перевищували вихідні значення до лікування в пацієнтів підгрупи 1а і не змінювалися в пацієнтів підгрупи 1б (12,57 ± 10,54 проти 12,41 ± 5,10 нг/мл) (р = 0,001; р = 0,96). У пацієнтів підгрупи «Мелаксену» рівень 6-СОМ у 1,8 раза (22,34 ± 10,65 і 12,41 ± 5,10 нг/мл) перевищував аналогічні показники в підгрупі 1б (р < 0,05). При IV ступені тяжкості ХОЗЛ концентрація 6-СОМ у пацієнтів підгрупи 1а і 1б склала 28,42 ± 13,41 і 11,5 нг/мл, відповідно. Рівень 6-СОМ у процесі лікування змінився в 1,8 раза (15,16 ± 12,13 і 28,42 ± 13,41 нг/мл) в пацієнтів, до схеми лікування яких було включено «Мелаксен», і в 1,6 раза (6,8 і 11,5 нг/мл) в пацієнтів, які «Мелаксен» не застосовували (р = 0,27).
Порівнюючи показники між групами, було визначено, що в пацієнтів підгрупи, яка додатково приймала «Мелаксен» рівень 6-СОМ у 2,4 раза перевищував ці ж значення у пацієнтів підгрупи 1б (28,42 ± 13,41 і 11,5 нг/мл) (р < 0,05).
Висновки: виходячи з вищенаведених результатів зміни динаміки 6-СОМ, можна припустити, що для цієї поєднаної патології характерне пропорційне зниження його концентрації в залежності від ступеня тяжкості ХОЗЛ. Ця тенденція зберігається як до, так і після лікування. В процесі лікування в пацієнтів, які додатково до основного лікування отримували «Мелаксен», достовірно зросли рівні 6-СОМ, на відміну від підгрупи 1б, де зміна була статистично незначною. Ці дані можуть свідчити про те, що мелатонін бере участь у патофізіологічних механізмах формування як ГЕРХ, так і ХОЗЛ, а його рівень корелює з рівнем тяжкості цієї поєднаної патології.
З точки зору математичної статистики, в усіх групах рівень 6-СОМ поводить себе як стабільна характеристика (r > 0,5). У пацієнтів підгрупи 1а спостерігали підвищення рівня 6-СОМ (стабільний позитивний терапевтичний ефект), середній рівень 6-СОМ після лікування підвищився на 82,5%, що забезпечувало статистично достовірну відмінність від стану до лікування з високим ступенем достовірності (р = 0,001). У підгрупі 1б у 30 % випадків рівень 6-СОМ знизився, однак загалом по групі спостерігали незначне (на 0,2 або на 1,3 %) його підвищення, що не забезпечувало статистично достовірної різниці від стану до лікування (р = 0,922). У хворих на ізольовану ГЕРХ у 40% випадків (16 хворих) рівень 6-СОМ також знизився, хоча загалом по групі спостерігали статистично незначуще підвищення його рівня на 0,94 нг/мл або 4,5 % (р = 0,669).
Производитель препарата Мелаксен UNIPHARM, Inc
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


