
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 11.10.2024 Штучний інтелект у фармації: перспективи, переваги та потенційні ризики
- Новини 27.08.2024 Вакансії медсестри у Вінниці: особливості та вимоги до кандидатів
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
Оптимизация результатов лечения у больных с генотипами 2 и 3 вируса гепатита С
Определение предикторов стойкого вирусологического ответа во время противовирусной терапии может иметь значение для оптимизации ее результатов у больных с генотипами 2 и 3 HCV. Ранний вирусологический ответ — это малоинформативный предиктор стойкого ответа у таких пациентов, так как его частота в данной группе достигает 97%. Однако быстрый вирусологический ответ, который оценивают через 4 недели, позволяет с высокой точностью предсказать стойкий вирусологический ответ у больных с генотипами 2 и 3 HCV, а его наличие может быть основанием для сокращения длительности противовирусной терапии. Опубликованы результаты нескольких небольших исследований, в которых изучалась эффективность более коротких курсов лечения больных с генотипами 2 и 3, однако различия дизайна исследований затрудняют их интерпретацию. В данном обзоре обсуждаются результаты этих исследований, а также данные АССЕLERATE— самого крупного рандомизированного исследования, целью которого было изучение возможности сокращения длительности противовирусной терапии у пациентов с генотипами 2 и 3. Полученные данные подтвердили, что быстрый вирусологический ответ в сочетании с исходными показателями может быть использован для оптимизации противовирусной терапии. Наличие быстрого вирусологического ответа сопровождается высокой частотой стойкого вирусологического ответа и может быть основанием для назначения более короткого курса противовирусной терапии, особенно у пациентов с низкой исходной вирусной нагрузкой. Однако при анализе преимуществ сокращенного курса лечения необходимо учитывать увеличение частоты рецидивов виремии. С другой стороны, отсутствие быстрого вирусологического ответа может указывать на целесообразность более интенсивной терапии (в течение более длительного срока и/или с применением более высоких доз). Как и при генотипах 1 и 4, оценка динамики виремии во время противовирусной терапии помогает оптимизировать ее без снижения частоты стойкого вирусологического ответа.
Введение
По мнению Lee и Ference [1], сегодня было бы неправильным говорить о том, что все больные с генотипами 1 и 4 HCV с трудом поддаются лечению, так как кинетика вирусной нагрузки свидетельствует об обратном. И наоборот, было бы ошибочным считать, что все больные с генотипами 2 и 3 HCV хорошо отвечают на противовирусную терапию. Генотип вируса имеет важное значение для оценки вероятности стойкого вирусологического ответа и выбора схемы первоначальной противовирусной терапии. Однако очевидно, что после начала лечения быстрый вирусологический ответ — это самый важный и мощный предиктор стойкого вирусологического ответа. Установлено, что независимо от генотипа вируса у больных с быстрым вирусологическим ответом вероятность стойкого ответа на 24-недельную теерапию пегилированным интерфероном α-2а и рибавирином составляет 90% [2,3].
Ранний вирусологический ответ имеет ограниченное значение при лечении больных с генотипами 2 и 3 HCV. Критериями раннего ответа являются клиренс HCV RNA (<50 МЕ/мл) или снижение вирусной нагрузки >2 loglO через 12 недель после начала лечения. В международном исследовании ACCELERATE ранний вирусологический ответ был достигнут фактически у всех (97%) больных, начавших 24-недельную противовирусную терапию пэгинтерфероном α-2а и рибавирином [4].
У больных с генотипами 2 и 3 оценка динамики виремии через 4 недели после начала комбинированной противовирусной терапии позволяет индивидуализировать схему дальнейшего лечения.
Сокращенный курс противовирусной терапии у больных с генотипами 2 и 3 HCV
В современных руководствах больным с генотипами 2 и 3 HCV рекомендуется проводить 24-недельный курс комбинированной терапии пэгинтерфероном α-2а и ри-бавирином в дозе 800 мг/сут [5,6]. Эта рекомендация основывается на результатах крупного рандомизированного международного исследования, в котором пациенты получали 24 или 48-недельные курсы противовирусной терапии пэгинтерфе-роном α-2а (Пегасис, Roche) и рибавирином (Копегус, Roche) в дозе 800 мг/сут или 1000/1200 мг/сут (в зависимости от массы тела) [7]. Частота стойкого вирусологического ответа в четырех группах составляла 79-84% и не зависела от длительности лечения или дозы рибавирина [7].
Тот факт, что 24-недельный курс противовирусной терапии обеспечивает максимальную частоту стойкого вирусологического ответа у больных с генотипами 2 и 3 HCV, послужил основанием для изучения возможности дальнейшего сокращения длительности лечения. Более короткие курсы дешевле и удобнее стандартной 24-недельной схемы и могут привести к улучшению переносимости. К настоящему времени эффективность 12-16-недельных курсов противовирусной терапии у больных с генотипами 2 и 3 изучена в 5 исследованиях [3,8-11]. Они значительно отличались по дизайну, поэтому необходимо очень осторожно оценивать полученные результаты, особенно при попытке их сравнения или обобщения.
Таблица 1. Исследования; в которых изучалась эффективность более коротких курсов противовирусной терапии у больных с генотипами 2 и 3 HCV

Особенности дизайна 5 исследований приведены в табл. L Длительность противовирусной терапии варьировалась от 12 до 16 недель, однако частота стойкого вирусологического ответа в первую очередь зависела от факторов, которые учитывали при назначении более короткого курса. В трех исследованиях длительность лечения определяли на основании наличия быстрого вирусологического ответа через 4 недели [8-10]. Напротив, в двух других клинических исследованиях пациентов рандомизировали исходно и назначали более короткий или стандартный курсы лечения [3,11]. Учитывая известное влияние быстрого вирусологического ответа на частоту стойкого ответа, очевидно, что выбор длительности лечения с учетом динамики виремии через 4 недели, должен был обеспечить более высокую частоту стойкого вирусологического ответа, что и произошло на самом деле.
Более короткий курс при наличии быстрого ответа
Достоинства более короткого курса противовирусной терапии можно оценить на основании тщательного анализа результатов двух исследований. В нервом из них решение о целесообразности сокращения длительности лечения принимали на основании быстрого вирусологического ответа [9]. Во втором более крупном исследовании (ACCELERATE) пациенты были рандомизированы на две группы исходно и получали более короткий или стандартный курсы противовирусной терапии [3]. В исследовании Mangia и со-авт. [9] рандомизировали 283 больных с генотипами 2 и 3 HCV, которым проводили стандартную 24-недельную противовирусной терапию или вариабельную по длительности (12 или 24 недели) терапию пегилированным интерфероном α-2Ь (ПегИнтрон, Schering-Plough) в дозе 1,0 мкг/кг/нед и рибавирином в дозе 1000 или 1200 мг/сут. Во второй группе длительность лечения определяли через 4 недели с учетом наличия быстрого вирусологического ответа. Как и следовало ожидать, самой высокой частота стойкого вирусологического ответа в этой группе оказалась у пациентов с быстрым вирусологическим ответом, которые продолжали лечение в течение 12 недель (85% против 64% у пациентов без быстрого ответа, получивших 24-недельный курс лечения; рис. 1). Общая частота стойкого вирусологического ответа у больных, которым исходно была назначена 24-недельная противовирусная терапия, составила 76% [9].
Рис. 1. Частота вирусологического ответа и рецидивов у больных, получавших пегилированный интерферон α-2Ь в рандомизированном исследовании.
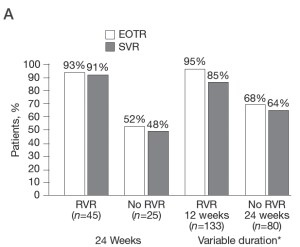
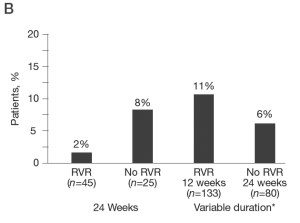
А - частота вирусологического ответа, В - частота рецидивов. В рандомизированном исследовании Mangia и соавт. [9] пациенты получали пегилированный интерферон α-2Ь в дозе 1,0 мкг/кг/нед и рибавирин в дозах 1000 или 1200 мг/ сут. Длительность лечения выбирали на основании быстрого вирусологического ответа (HCV RNA<50 МЕ/мл) через 4 недели). E0TR - ответ в конце противовирусной терапии, SVR - стойкий вирусологический ответ.
При сравнении результатов лечения в двух группах обращает на себя внимание небольшая разница частоты стойкого вирусологического ответа между ними: 76% у пациентов, которым был назначен стандартный 24-недельный курс лечения, и 77% у больных, которым проводили вариабельный по длительности курс противовирусной терапии с учетом наличия быстрого вирусологического ответа. Полученные данные позволяют рассматривать последнюю схему как приемлемую альтернативу стандартному 24-недельному курсу лечения. Однако при более внимательном рассмотрении полученных результатов видны возможные недостатки сокращенного курса. После его завершения частота рецидивов виремии была выше, чем после стандартного курса противовирусной терапии. В выборке пациентов, у которых был достигнут быстрый вирусологический ответ, частота рецидивов после 24-недельной противовирусной терапии была значительно ниже (2%), чем после 12-недельной терапии (11%; рис. 1) [9]. Пациенты, которым была назначена 24-недельная схема, чаще прекращали лечение, чем пациенты, получавшие более короткий курс противовирусной терапии. Таким образом, более высокая частота рецидивов после короткого курса и более высокая частота отмены стандартной схемы нивелируют друг друга, поэтому создается впечатление, что результаты двух схем являются сходными. Самым крупным исследованием, в котором изучались преимущества более короткого курса противовирусной терапии у больных с генотипами 2 и 3 HCV, было ACCELERATE. В этом исследовании были рандомизированы 1469 больных, которым проводили 16 или 24-недельные курсы противовирусной терапии пэгинтерфероном α-2а в дозе 180 мкг/нед и рибавирином в дозе 800 мг/сут [3].
Из первичного анализа исключали пациентов, нарушавших протокол или получивших менее 80% доз назначенных препаратов. Частота стойкого вирусологического ответа у больных, получавших 24-недельную противовирусную терапию, была значительно выше, чем у пациентов, которым был назначен 16-недельный курс лечения (76% и 65% соответственно; отношение шансов 0,59; 95% доверительный интервал 0,46-0,76; р<0,001). Результаты анализав выборке intent-to-treat оказались сходными, 70% и 62% соответственно (отношение шансов 0,67; 95% доверительный интервал 0,54-0,84; р<0,001) [3]. Эти данные были получены несмотря на более высокую частоту выхода из исследования пациентов, получавших 24-недельную противовирусную терапию.
Рис. 2. Частота стойкого вирусологического ответа при наличии и отсутствии быстрого вирусологического ответа
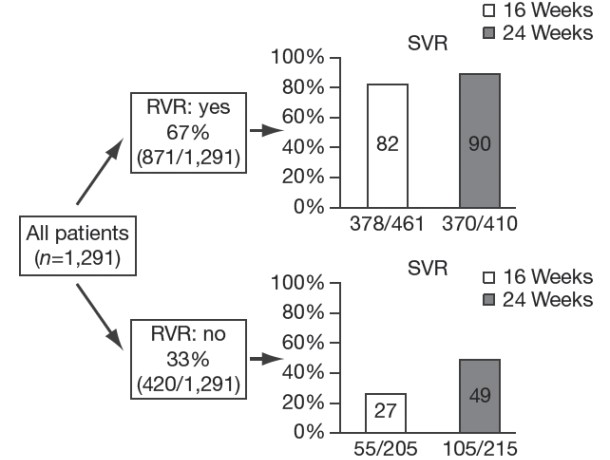
На рисунке приведена частота стойкого вирусологического ответа (SVR) у больных, достигших и не достигших быстрого вирусологического ответа (RVR; HCV RNA <50 МЕ/мл через 4 недели) на лечение пэгинтерфероном α-2а 180 мкг/нед и рибавирином 800 мг/сут в исследовании ACCELERAT [4]
Рис. 3. Частота стойкого вирусологического ответа у больных с быстрым вирусологическим ответом
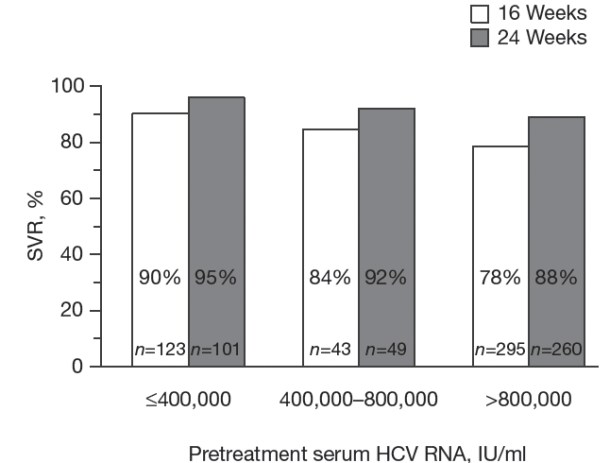
Приведена частота стойкого вирусологического ответа (SVR) у больных с быстрым вирусологическим ответом (RVR; HCV RNA<50 МЕ/мл через 4 недели) у больных, получавших пэгинтерферон α-2а 180 мкг/нед и рибавирин 800 мг/сут, в зависимости от длительности лечения и исходной вирусной нагрузки в исследовании ACCELERATE [4]
Какие выводы можно сделать на основании результатов исследования ACCELERATE по поводу схемы лечения больных с генотипами 2 и 3 HCV? Очевидно, что не следует рекомендовать более короткий курс противовирусной терапии всем этим пациентам [3]. На первый взгляд, этот вывод противоречит результатам исследования Mangia и со-авт. [9]. Однако более тщательный анализ результатов ACCELERATE подтверждает предсказательное значение быстрого вирусологического ответа у больных с генотипами 2 и 3 HCV и указывает на адекватность выбора длительности лечения с учетом наличия быстрого ответа [3].
В целом в исследовании ACCELERATE быстрый вирусологический ответ был достигнут у 67% больных. В этой выборке частота стойкого вирусологического ответа на 24-недельный курс противовирусной терапии была выше (90%), чем на 16-недельный (82%; рис. 2). При отсутствии быстрого вирусологического ответа частота стойкого ответа была значительно ниже (49% и 27% при продолжении лечения в течение 24 и 16 недель, соответственно).
При анализе исходного уровня HCV RNA и быстрого вирусологического ответа очевидно, что эти два фактора оказывали выраженное влияние на частоту стойкого вирусологического ответа. Хотя, как видно из рис. 2,24-недельный курс противовирусной терапии обеспечивал более высокую частоту стойкого вирусологического ответа, чем 16-недельный, независимо от исходной вирусной нагрузки. В исследовании ACCELERATE у больных с низкой вирусной нагрузкой (<400000 МЕ/мл) частота стойкого вирусологического ответа на 24-и 16-недельные курсы противовирусной терапии составила 95% и 90%, соответственно (рис. 3), а у пациентов с исходной концентрацией HCV RNA >800000 МЕ/мл — 88% и 78%. Видно, что абсолютная разница частоты стойкого вирусологического ответа в выборках пациентов с высокой и низкой исходной вирусной нагрузкой выше при проведении более короткого курса противовирусной терапии (12% против 7% при продолжении лечения в течение 24 недель).
Как указано выше, ранний вирусологический ответ был достигнут у большинства больных с генотипами 2 и 3 HCV. Интересная тенденция была выявлена при анализе результатов лечения в зависимости от сроков клиренса виремии. Если HCV RNA переставала определяться через 4 недели (быстрый вирусологический ответ) или 12 недель (полный ранний вирусологический ответ), то частота вирусологического ответа в конце курса противовирусной терапии была практически одинаковой (95% и 94%, соответственно). Однако рецидивы виремии редко развивались у больных с быстрым вирусологическим ответом и чаще встречались у пациентов, у которых клиренс HCV RNA происходил только через 12 недель. В связи с этим частота стойкого вирусологического ответа в этих группах отличалась — 90% и 57%, соответственно. Это напоминает ситуацию у пациентов с генотипом 1 HCV (Lee и Ferenci в [1]). У больных с генотипом 1, достигших частичного раннего вирусологического ответа, частота стойкого ответа была значительно ниже (27%), чем у пациентов с быстрым вирусологическим ответом (87%) или полным ранним вирусологическим ответом (68%), из-за более высокой частоты рецидивов ви-ремии после прекращения лечения.
Разница между пациентами с генотипами 2 и 3
В исследовании ACCELERATE частота вирусологического ответа отличалась у больных, инфицированных генотипами 2 и 3 вируса [3]. В выборке intent-to-treat (24-недельный курс лечения) у больных с генотипом 2 была выше частота быстрого вирусологического ответа (69% и 59%), раннего вирусологического ответа (94% и 85%), ответа в конце курса противовирусной терапии (84% и 80%) и стойкого вирусологического ответа (75% и 66%). Сходная тенденция наблюдалась у пациентов, получавших 16-недельный курс противовирусной терапии, хотя частота стойкого вирусологического ответа была идентичной у пациентов с генотипами 2 и 3 (62%).
При наличии быстрого вирусологического ответа частота стойкого ответа была одинаковой у больных с генотипами 2 и 3, получавших 24-недельный курс противовирусной терапии (85%), и сходной у пациентов, которым проводилось 16-недельное лечение (78% и 80%, соответственно). Самая большая разница была у пациентов без быстрого вирусологического ответа, которым был назначен 24-недельный курс противовирусной терапии: частота стойкого вирусологического ответа составила 53% у больных с генотипом 2 и 39% у пациентов с генотипом 3 [3].
Mangia и соавт. [9] также выявили разницу частоты стойкого вирусологического ответа у больных с генотипами 2 и 3 HCV. В целом частота стойкого вирусологического ответа в этих выборках составила 80% и 66%, соответственно (р<0,001). Частота стойкого вирусологического ответа была идентичной у пациентов с генотипами 2 и 3, получавших стандартный 24-недельный курс лечения (76%), поэтому эта разница была связана с разницей частоты ответа у пациентов, которым проводился вариабельный по длительности курс противовирусной терапии (82% у больных с генотипом 2 и 62% у пациентов с генотипом 3).
Высокая исходная вирусная нагрузка оказывала выраженное влияние на частоту стойкого вирусологического ответа у больных с генотипом 3. Эта тенденция наблюдалась в нескольких исследованиях и была особенно очевидной у больных, которым назначали более короткие схемы противовирусной терапии [3,8,10].
Эффект дозы рибавирина
Вызывает интерес вопрос о том, влияет ли доза рибавирина на частоту стойкого вирусологического ответа у больных, получающих короткий курс противовирусной терапии (роль дозы этого препарата более подробно обсуждается в статье Dusheiko и соавт. [12]). У больных с генотипами 2 и 3 вируса рекомендуемая доза рибавирина является фиксированной и составляет 800 мг/сут. Эта доза была выбрана на основании результатов крупного исследования Hadziyannis и со-авт. [7]. Частота стойкого вирусологического ответа существенно не отличалась у больных с генотипами 2 и 3, получавших 24-недельный (или 48-недельный) курс противовирусной терапии пегилирован-ным интерфероном и рибавирином в дозах 800 мг/сут или 1000/1200 мг/сут. Это свидетельствует о том, что доза рибавирина у пациентов с генотипами 2 и 3 имеет меньшее значение, чем у пациентов с генотипами 1 или 4. Если проводится стандартный 24-недельный курс противовирусной терапии, то возможно даже дополнительное снижение дозы этого препарата [13].
В нескольких исследованиях применялась более высокая доза рибавирина (800-1400 мг/сут) [8-11], однако отсутствие контрольной группы не позволяет судить о том, привело ли это к улучшению результатов лечения.
Хотя в исследовании ACCELERATE рибавирин применяли в фиксированной дозе 800 мг/сут, полученные результаты дают возможность оценить важность дозы рибавирина при проведении более короткого курса противовирусной терапии. Более высокая экспозиция рибавирина имела значение, если пациенты, достигшие и не достигшие быстрого вирусологического ответа, получали менее 17 доз пэгинтерферона α-2а. Однако если число доз последнего превышало 17, то экспозиция рибавирина существенно не отражалась на частоте стойкого вирусологического ответа [14].
Необходимо дополнительное исследование для подтверждения оптимальной дозы рибавирина у больных с генотипами 2 и 3, получающих сокращенный курс противовирусной терапии.
Увеличение длительности лечения при медленном ответе на него
Результаты рандомизированных проспективных исследований свидетельствуют о возможности повышения частоты стойкого вирусологического ответа при увеличении длительности противовирусной терапии у больных с генотипом 1, которые медленно отвечают на лечение [15,16] (Ferenci и Lee в [1]). Возникает вопрос, может ли интенсификация терапии привести к увеличению частоты стойкого ответа у больных с генотипами 2 и 3, у которых отсутствует быстрый вирусологический ответ. В проспективных исследованиях этот вопрос не изучался, его анализировали ретроспективно [17] на основании исследования Hadziyannis и соавт. [7]. В этом исследовании частота стойкого вирусологического ответа составляла 65-76% в 4 группах (рис. 4). Как и у больных с генотипом 1, частота рецидивов снижалась при увеличении интенсивности лечения и была самой низкой у больных, получавших пэгинтерферон α-2а и рибавирин в дозе 1000/1200 мг/сут в течение 48 недель (4%), и самой высокой у пациентов, которым проводился 24-недельный курс лечения пэгинтерфероном α-2а и рибавирином в дозе 800 мг/сут (26%) [17]. Хотя эти данные необходимо подтвердить в проспективном исследовании, они свидетельствуют о том, что интенсификация противовирусной терапии может привести к увеличению частоты стойкого вирусологического ответа у пациентов с генотипами 2 и 3, не достигших клиренса виремии через 4 недели.
Рис. 4. Частота стойкого вирусологического ответа и рецидивов виремии у больных без быстрого вирусологического ответа, получавших пэгинтерферон α-2а и рибавирин в течение 24 или 48 недель в крупном рандомизированном международном исследовании
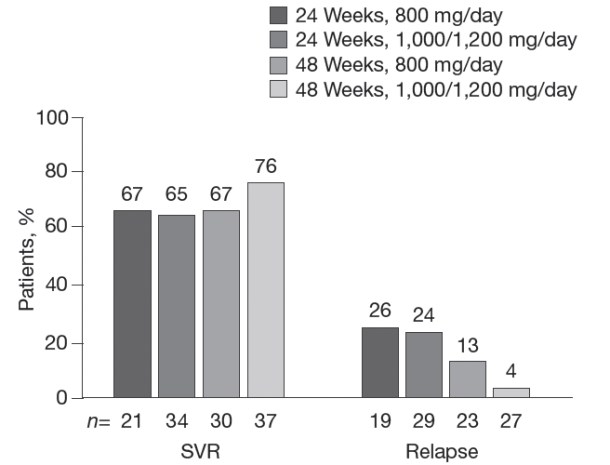
Приведена частота стойкого вирусологического ответа (слева) и рецидивов (справа) у пациентов, не достигших быстрого вирусологического ответа и получавших лечение пэгинтерфероном α-2а 180 мкг/нед и рибавирином в дозах 800 или 1000/1200 мг/сут в течение 24 или 48 недель
Заключение
Результаты исследования ACCELERATE и менее крупных исследований свидетельствуют о том, что при наличии быстрого вирусологического ответа у больных с генотипами 2 и 3 можно добиться высокой частоты стойкого ответа на более короткий курс противовирусной терапии. Недостаток его — несколько более высокая частота рецидивов, а недостаток стандартного курса — несколько более высокая частота досрочного прекращения лечения. Увеличение дозы рибавири-на у пациентов, получающих более короткий курс, может привести к снижению частоты рецидивов, однако этот вопрос нуждается в дополнительном изучении, как и целесообразность увеличения длительности лечения до 48 недель при отсутствии быстрого вирусологического ответа через 4 недели. Самая высокая частота стойкого вирусологического ответа и самая низкая частота рецидивов наблюдаются у больных с быстрым вирусологическим ответом и низкой исходной концентрацией HCV RNA (<400000 МЕ/мл). Дополнительная информация о потенциальных преимуществах выбора схемы противовирусной терапии с учетом ответа на нее будет получена в когортном исследовании PROPHESYS.
Список литературы
- Lee SS, Ferenci P. Optimizing outcomes in patients with hepatitis C virus genotype 1 or 4. Antivir Ther 2008; 13 Suppl 1:9-16.
- Jensen DM, Morgan TR, Marcellin P, et al. Early identification of HCV genotype 1 patients responding to 24 weeks peginterferon alpha-2a (40 kd)/ribavirin therapy. Hepatology 2006; 43:954-960.
- Shiffman ML, Suter FS, Bacon BR, et al. Peginterferon alpha-2a and ribavirin for 16 or 24 weeks in HCV genotype 2 or 3. N EnglJMed 2007; 357:124-134.
- Shiffman M, Pappas S, Bacon B. et al. Utility of virological response at weeks 4 and 12 in the prediction of SVR rates in genotype 2/3 patients treated with peginterferon alpha-2a plus ribavirin: findings from ACCELERATE. Hepatology 2006; 44 Suppl 1:316A-317A.
- Dienstag JL, McHutchison JG. American Gastroenterological Association medical position statement on the management of hepatitis C. Gastroenterology 2006; 130:225-230.
- Strader DB, Wright T, Thomas DL, Seeff LB. Diagnosis, management, and treatment of hepatitis C. Hepatology 2004;39:1147-1171.
- Hadziyannis S, Sette H, Morgan T, et al. Peginterferon-alpha2a and ribavirin combination therapy in chronic hepatitis C: a randomized study of treatment duration and ribavirin dose. Ann Intern Med 2004; 140:346-355.
- Dalgard O, Bjoro K, Helium KB, et al. Treatment with pegylated interferon and ribavarin in HCV infection with genotype 2 or 3 for 14 weeks: a pilot study. Hepatology 2004; 40:1260-1265.
- Mangia A, Santoro R, Minerva N, et al. Peginterferon alpha-2b and ribavirin for 12 vs. 24 weeks in HCV genotype 2 or 3. N Engl J Med 2005; 352:2609-2617.
- von-Wagner M, Huber M, Berg T, et al. Peginterferon alpha-2a and ribavirin for 16 or 24 weeks in patients with genotype 2 or 3 chronic hepatitis C. Gastroenterology 2005; 129:522-527.
- Yu ML, Dai CY, Huang JF, et al. A randomized study of peginterferon and ribavirin for 16 versus 24 weeks in patients with genotype 2 chronic hepatitis C. Gut 2007; 56:553-559.
- Dusheiko G, Nelson D, Reddy KR. Ribavirin considerations in treatment optimization. Antivir Ther 2008; 13 Suppl 1:23-30.
- Ferenci P, Brunner H, Laferl H, et al. Further reduction of ribavirin dose in HCV genotype 2/3 patients receiving peginterferon alpha-2a (Pegasys) plus ribavirin (Copegus): interim results of a randomized controlled trial. JHepatol 2006; 44 Suppl 2:S37.
- Shiffman M, Pappas S, Greenbloom S, et al. Effect of drug exposure on sustained virological response (SVR) in patients with chronic hepatitis C virus genotype 2 or 3 treated with peginterferon alpha-2a (Pegasys) plus ribavirin (Copegus) for 16 or 24 weeks. Hppatology 2006; 44 Suppl 1:317A.
- Berg T, von Wagner M, Nasser S, et al. Extended treatment duration for hepatitis C virus type 1: comparing 48 versus 72 weeks of peginterferon-alpha-2a plus ribavirin. Gastroenterology 2006; 130:1086-1097.
- Sanchez-Tapias JM, Diago M, Escartin P, et al. Peginterferon-alfa2a plus ribavirin for 48 versus 72 weeks in patients with detectable hepatitis C virus RNA at week 4 of treatment. Gastroenterology 2006; 131:451-460.
- Willems B, Hadziyannis SJ, Morgan TR, et al. Should treatment with peginterferon plus ribavirin be intensified in patients with HCV genotype 2/3 without a rapid virological response? / Hepatol 2007; 46 Suppl 1:S6.

Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


