
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 11.10.2024 Штучний інтелект у фармації: перспективи, переваги та потенційні ризики
- Новини 27.08.2024 Вакансії медсестри у Вінниці: особливості та вимоги до кандидатів
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
Современные принципы лечения гепатита С
Хронический гепатит С — это главная причина цирроза и гепато-целлюлярной карциномы, что определяет необходимость активного изучения механизмов развития болезни и подходов к ее лечению. За последнее десятилетие в этой области был достигнут значительный прогресс, прежде всего благодаря применению пегилированных интерферонов и рибавирина. В данном обзоре обсуждаются физические свойства, фармакокинетика, кинетика вирусной нагрузки и побочные эффекты пегилированных интерферонов и рибавирина, которые сегодня стали стандартом лечения хронического гепатита С.
Введение
В мире 170 млн. человек инфицированы вирусом гепатита С (HCV), который является главной причиной развития цирроза и гепатоцеллюлярной карциномы и трансплантации печени [1]. По данным ВОЗ, в 2002 году декомпенсированный цирроз печени был причиной примерно 1 из 40 случаев смерти [2]. Эти цифры обосновывают затраты на изучение HCV-инфекции, которое началось в 1989 году после открытия генома вируса [3]. С этого времени наши представления об этиологии и патогенезе хронического гепатита С значительно расширились. В свою очередь, это привело к разработке новых подходов к лечению, которые за последние 10 лет существенно усовершенствовались. Первоначально больным гепатитом С проводили монотерапию интерфероном-α (три раза в неделю) в течение 24 или 48 недель, однако результаты лечения были в целом неудовлетворительными — частота стойкого вирусологического ответа (уровень HCV RNA<50 МЕ/мл через 24 недели после прекращения терапии) составляла всего 10-20% [4,5]. Однако применение рибавирина в комбинации с интерфероном-α (с 1998 года) привело к значительному увеличению частоты стойкого ответа до 30-40% [6,7]. Дальнейшие достижения в лечении HCV-инфекции были связаны с появлением в 2000 году пегилированного интерферона, который представляет собой молекулу интерферона-а, соединенного с полиэтиленгликолем. При комбинированной терапии этим препаратом и рибавирином частота стойкого вирусологического ответа впервые превысила 50% [8,9]. Средняя частота стойкого ответа на лечение пэгинтерфероном α-2а (Пегасис, Roche) и рибавирином достигала 66% [8,10,11]. В настоящее время комбинацию пегилированного интерферона и рибавирина считают золотым стандартом лечения хронического гепатита С [12-14].
Современные анти-HCV средства
Сегодня зарегистрированы два пегилированных интерферона. Пэгинтерферон α-2а представляет собой интерферон α-2а, соединенной стабильной амидной связью с крупной разветвленной молекулой полиэтиленгликоля массой 40 кДа. Он состоит из 6 позиционных изомеров [15,16].
В состав пегилированного интерферона α-2b входит небольшая линейная молекула полиэтиленгликоля массой 12 кДа, которая соединена с интерфероном α-2b менее стабильным уретановым мостиком. Препарат состоит из 14 позиционных изомеров [16-19].
Особенности строения двух препаратов определяют разницу схем их применения и форм выпуска. Пэгинтерферон α-2а выпускается в виде готовых шприцев и вводится в фиксированной дозе 180 мкг/нед [20], в то время как пегилированный интерферон α-2b выпускается в виде лиофилизированного порошка, который необходимо растворить перед применением. Дозу подбирают с учетом массы тела (1,5 мкг/кг/нед) [21]. Биохимическое строение определяет также особенности фармакокинетики двух препаратов и динамики вирусной нагрузки при их применении и, соответственно, разницу частоты стойкого вирусологического ответа. Уровни пэгинтерферона α-2а в плазме постоянные и поддерживаются на протяжении всего интервала дозирования [22,23], что приводит к стойкому подавлению репликации вируса (рис. 1) [24], в то время как уровни пегилированного интерферона α-2b в плазме колеблются на протяжении интервала дозирования, что сопровождается увеличением вирусной нагрузки (рис. 2) [25-28].
Рис. 1. Фармакокинетика пэгинтерферона α-2а и кинетика вирусной нагрузки
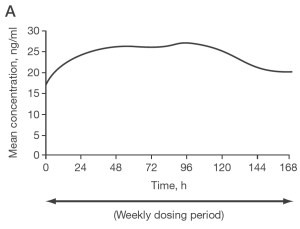
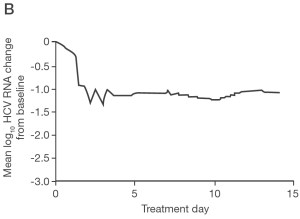
А — Фармакокинетика пэгинтерферона α-2а 180 мкг один раз в неделю [23]. В — Кинетика вирусной нагрузки при введении пэгинтерферона α-2а [24]
Рис. 2. Фармакокинетика пэгинтерферона а-2Ь и кинетика вирусной нагрузки
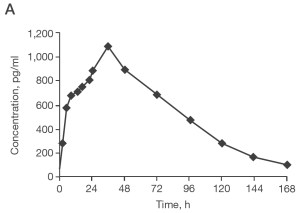
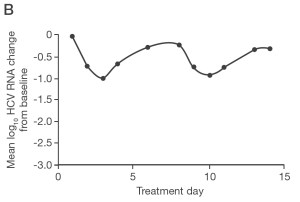
А — Фармакокинетика пэгинтерферона α-2а 1,5 мкг/кг один раз в неделю 128]. В — Кинетика вирусной нагрузки при введении пэгинтерферона а-2Ь [25,26]. Пациенты с генотипом 1, не ответившие на комбинированную терапию.
Значение кинетики вирусной нагрузки
Помимо различий противовирусной активности двух пегилированных интер-феронов, изучение кинетики вирусной нагрузки может быть использовано для установления параметров, оказывающих влияние на эффективность противовирусной терапии и позволяющих предсказать ответ на нее. С помощью математического моделирования и статистического анализа было установлено, что снижение уровня HCV RNA в ответ на противовирусную терапию является двух- или возможно трехфазным [29]. В первую фазу (индукция) блокируется продукция вируса (фактор ξ), в то время как наклон второй фазы (поддерживающей) отражает гибель инфицированных клеток (σ) (рис. 3 А). Третья фаза может отражать гибель инфицированных клеток в результате замедленной воспалительной реакции, индуцированной лечением (рис. 3 В). Факторы вируса, пациента и лечения, определяющие частоту стойкого вирусологического ответа (например, генотип вируса, этническое происхождение пациента, цирроз, индекс массы тела, тип пегилированного интерферона и его доза), оказывают влияние на кинетику вирусной нагрузки [29-33]. Механизм действия рибавирина окончательно не установлен. Однако хорошо известно, что он усиливает вирусологический ответ и предупреждает развитие рецидива виремии (Dusheiko и соавт. [34]). Изучение кинетики вирусной нагрузки может быть также использовано для выяснения механизмов резистентности HCV, позволяющих ему ускользнуть от эффекта противовирусных средств [29].
Улучшение результатов лечения
Хотя первая фаза кинетики вируса при лечении интерфероном α-2а и пэгинтерфероном α-2а сходная, последний вызывает значительно более быстрое снижение вирусной нагрузки во вторую фазу [31]. Соответственно, он обеспечивает более высокую частоту стойкого вирусологического ответа, по сравнению со стандартным интерфероном-α. Применение пэгинтерферона α-2а и рибавирина позволило улучшить результаты лечения больных со всеми генотипами HCV (средняя частота стойкого вирусологического ответа на 48-недельную терапию достигает 66%) [8,10,11]. Основным исходным фактором, определяющим частоту стойкого вирусологического ответа, является генотип вируса (частота ответа значительно выше при наличии генотипов 2 и 3) [35]. Hadziyannis и со-авт. [10] показали, что пациенты с генотипом 1 чаще отвечают на 48-недельный курс противовирусной терапии пэгин-терфероном α-2а и рибавирином в дозе 1000/1200 мг/сут, в то время как у больных с генотипами 2 и 3 частота стойкого вирусологического ответа была одинаково высокой при проведении 24-и 48-недельных курсов противовирусной терапии и применении рибавирина в дозе 800 мг/сут. Соответственно, эти схемы были включены в современные рекомендации [12,13,36]. Частота стойкого вирусологическое ответа на лечение пэгинтерфероном α-2а и рибавирином у больных с генотипом 1 достигала 60% [8,10,11,37], а у пациентов с генотипами 2 и 3 — 84% [10,38,39]. При применении пегилированного интерферона α-2b и рибавирина эти показатели составляли 42% и 81%, соответственно [9,40-42].
Другие независимые предикторы стойкого вирусологического ответа включают в себя исходную вирусную нагрузку (низкая или высокая), возраст (<40 лет и >40 лет) и наличие цирроза [8,35]. Однако пегилированный интерферон оказался эффективным и у «трудных больных» гепатитом С. Например, частота стойкого вирусологического ответа на лечение пэгинтерфероном α-2 а и рибавирином составляет 47-52% у больных с генотипом 1 и высокой вирусной нагрузкой или мостовидным фиброзом/циррозом [8,10]. При применении пегилированного интерферона (α-2b и рибавирина этот показатель составлял 32-44% [9,42].
Недавно были изучены сроки сохранения стойкого вирусологического ответа на лечение пэгинтерфероном α-2а и ри-бавирином [43]. В этом исследовании у больных, принимавших участие в 1 из 9 рандомизированных исследований, определяли уровень HCV RNA в течение 5 лет после завершения лечения. Более чем у 99% больных достигнутый ответ сохранялся в течение 5 лет, что свидетельствовало об их излечении [43].
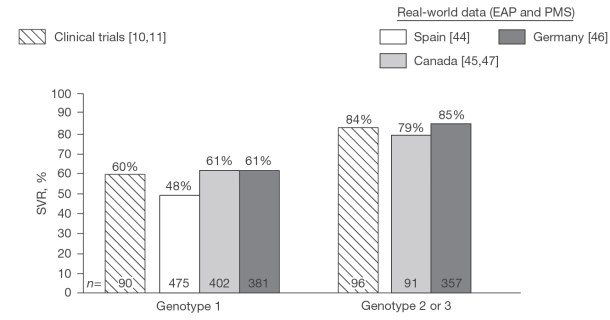
Отражением результатов клинических исследований является высокая частота стойкого вирусологического ответа при всех генотипах вируса в реальной клинической практике (рис. 4) [10,11,44-47]. Эти данные подтверждают выводы, сделанные на основании рандомизированных контролируемых исследований.
Рис. 3. Математическое описание результатов изменения HCV RNA при лечении пэгинтерфероном α-2а и рибавирином.
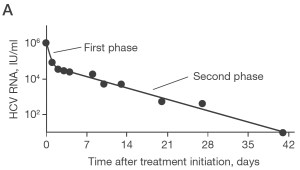
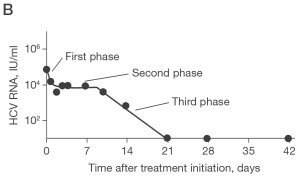
А — двухфазная модель, В — трехфазная модель [29]
Рис. 4. Сравнение результатов применения пэгинтерферона α-2а и рибавирина в клинических исследованиях и реальной клинической практике [10,11,44-47]
Возможно ли дальнейшее улучшение результатов лечения?
Увеличение частоты стойкого вирусологического ответа у больных с генотипом 1 вируса и сохранение высокой частоты стойкого ответа у пациентов с генотипами 2 и 3 связано с оптимизацией стратегий ведения больных. Сокращение длительности лечения до 24 недель у пациентов, инфицированных генотипами 2 и 3, и изучение профиля побочных эффектов пегилированных интерферонов и риба-вирина позволили снизить частоту досрочного прекращения лечения. По сравнению со стандартным интерфероном, пэгинтерферон α-2а реже вызывал депрессию [8]. Более того, в проспективном двойном слепом, рандомизированном исследовании при сравнении психоневрологических побочных эффектов двух пегилированных интерферонов было показано, что при лечении пэгинтерфероном α-2а больным реже требовалось применение психотропных средств, чем при применении пегилированного интерферона α-2b [48].
Индивидуализация противовирусной терапии на основании вирусологического ответа через 4 и 12 недель позволит добиться дальнейшего улучшения ее результатов. В настоящее время решение о целесообразности продолжения противовирусной терапии у больных с генотипом 1 принимают на основании раннего вирусологического ответа (клиренс HCV RNA или снижение вирусной нагрузки по крайней мере на 2 log10 через 12 недель) [12-14]. Если ранний вирусологический ответ отсутствует, то лечение прекращают. В то же время если достигнут ранний ответ, а через 24 недель перестает определяться HCV RNA (<50 МЕ/мл), то лечение продолжают в течение 48 недель, а в конце терапии оценивают вирусологический ответ. Через 24 недели после завершения лечения определяют стойкий вирусологический ответ. У больных с генотипами 2 и 3 оценивать вирусологический ответ на фоне лечения не рекомендуют. В таких случаях достаточно его оценки в конце курса и через 24 недели после его завершения [12-14]. Если противовирусная терапия проводится на основании ответа на нее, то оценивают уточненные критерии раннего вирусологического ответа, а также быстрый вирусологический ответ (HCV RNA<50 МЕ/мл через 4 недели).
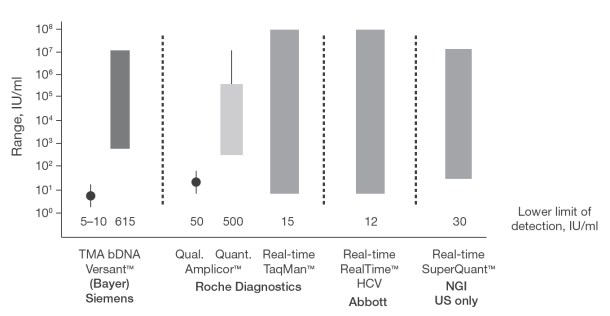
Рис. 5. Коммерческие методы анализа вирусной нагрузки (полимеразная цепная реакция). По оси ординат — диапазон, внизу — порог определения, МЕ/мл
Измерение уровней HCV RNA
Существует несколько методов измерения уровней HCV RNA: Bayer Versant, Abbott Real Time, NGI SuperQuant, Roche COBAS Amplicor HCV Test, v2.0 (качественные методы) и COBAS Amplicor HCV Monitor Test, v2.0 (количественный метод; рис. 5).
Более чувствительный метод (COBAS TaqMan) в настоящее время применяется более чем в 30 странах мира. Он позволяет измерить вирусную нагрузку в диапазоне от 15 МЕ/мл до 100 млн. МЕ/мл. Установлена тесная корреляция результатов этого метода и методов Amplicor [49]. Применение нового метода может отразиться на результатах оценки быстрого, раннего и стойкого вирусологического ответа, что необходимо изучить в проспективных исследованиях.
Значение нерандомизированных исследований
Рандомизированные контролируемые исследования считают стандартом при изучении эффективности лечебных вмешательств. Они позволяют избежать систематических ошибок, связанных с особенностями набора пациентов и предпочтениями исследователей. Однако рандомизированные исследования сопровождаются значительными затратами времени и средств и обычно предполагают изучение эффективности лечения у тщательно отобранных пациентов. Неконтролируемые исследования позволяют оценить возможность использования результатов рандомизированных исследований в клинической практике. Большой объем подобных исследований имеет значение для выявления редких нежелательных явлений, а также изучения возможных затрат, особенностей ведения пациентов и их предпочтений. Исследования-наблюдения проводятся в обычной практике, что позволяет исключить этические проблемы и свести к минимуму финансовые затраты. В них включают любых пациентов и не ограничивают число вмешательств. Однако подобные исследования являются открытыми и неконтролируемыми [50]. Напротив, рандомизированные контролируемые исследования позволяют оценить приверженность пациентов и снизить вероятность искажения результатов лечения за счет рандомизации. Двойной слепой метод повышает надежность установленных исходов, которые могут включать в себя «суррогатные», «мягкие» или «твердые» конечные точки [50,51].
Заключение
Изучение кинетики вирусной нагрузки и совершенствование методов диагностики привели кразработке современных схем лечения гепатита С. Противовирусная терапия пегилированными интерферонами и рибавирином позволяет добиться прекрасного ответа у больных с генотипами 1 и 2/3. Хотя частота стойкого вирусологического ответа за последние годы увеличилась, тем не менее, сохраняется возможность дальнейшего улучшения результатов лечения. Установлена целесообразность проведения противовирусной терапии с учетом вирусологического ответа, который определяют через 4 и 12 недель. Доказанная эффективность пэгинтерферона α-2а и рибавирина в сочетании с уникальными фармакокинетическими свойствами и влиянием на кинетику вируса означает, что он останется основой терапии HCV-инфекции в обозримом будущем.
Список литературы
- Global surveillance and control of hepatitis C. Report of a WHO Consultation organized in collaboration with the Viral Hepatitis Prevention Board, Antwerp, Belgium. / Viral Hepat 1999; 6:35-47.
- Perz JF, Armstrong GL, Farrington LA, Hutin YJ, Bell BP. The contributions of hepatitis B virus and hepatitis C virus infections to cirrhosis and primary liver cancer worldwide. J Hepatol 2006; 45:529-538.
- Choo QL, Kuo G Weiner AJ, Overby LR, Bradley DW, Houghton M. Isolation of a cDNA clone derived from a blood-borne non-A, non-B viral hepatitis genome. Science 1989; 244:359-362.
- Tine F, Magrin S, Craxi A, Pagliaro L. Interferon for non-A, non-B chronic hepatitis. A meta-analysis of randomised clinical trials. / Hepatol 1991; 13:192-199.
- Poynard T, Leroy V, Cohard M, et al. Meta-analysis of interferon randomized trials in the treatment of viral hepatitis C: effects of dose and duration. Hepatology 1996; 24:778-789.
- McHutchison JG, Gordon SC, Schiff ER, et al. Interferon alfa-2b alone or in combination with ribavirin as initial treatment for chronic hepatitis C. Hepatitis Interventional Therapy Group. N EnglJ Med 1998; 339:1485-1492.
- Poynard T, Marcel lin P, Lee SS, et al Randomised trial of interferon alpha2b plus ribavirin for 48 weeks or for 24 weeks versus interferon alpha2b plus placebo for 48 weeks for treatment of chronic infection with hepatitis C virus. International Hepatitis Interventional Therapy Group (IHIT). Lancet 1998; 352:1426-1432.
- Fried MW, Shiffman ML, Reddy KR, et al Peginterferon alfa-2a plus ribavirin for chronic hepatitis C virus infection. N Engl J Med 2002; 347:975-982.
- Manns MP, McHutchison JG, Gordon SC, et at. Peginterferon alfa-2b plus ribavirin compared with interferon alfa-2b plus ribavirin for initial treatment of chronic hepatitis C: a randomised trial. Lancet 2001; 358:958-965.
- Hadziyannis SJ, Sette H, Jr., Morgan TR, et al. Peginterferon-alpha2a and ribavirin combination therapy in chronic hepatitis C: a randomized study of treatment duration and ribavirin dose. Ann Intern Med 2004; 140:346-355.
- Zeuzem S, Pawlotsky JM, Lukasiewicz E, et al. International, multicenter, randomized, controlled study comparing dynamically individualized versus standard treatment in patients with chronic hepatitis C. / Hepatol 2005; 43:250-257.
- Strader DB, Wright T, Thomas DL, Seeff LB. Diagnosis, management, and treatment of hepatitis C. Hepatoto^y 2004; 39:1147-1171.
- National Institutes of Health. National Institutes of Health consensus development conference statement: management of hepatitis C: 2002-June 10-12, 2002. Hepatology 2002; 36:S3-S20.
- Dienstag JL, McHutchison JG. American Gastroenterological Association medical position statement on the management of hepatitis C. Gastroenterology 2006; 130:225—230.
- Bailon P, Palleroni A, Schaffer CA, et at. Rational design of a potent, long-lasting form of interferon: a 40 kDa branched polyethylene glycol-conjugated interferon alpha-2a for the treatment of hepatitis C. Bioconjug Chem 2001; 12:195-202.
- Kozlowski A, Charles SA, Harris JM. Development of pegylated interferons for the treatment of chronic hepatitis C. BioDrugs 2001; 15:419-429.
- Wang YS, Youngster S, Bausch J, Zhang R, McNemar C. Wyss DF. Identification of the major positional isomer or pegylated interferon alpha-2b. Biochemistry 2000; 39:10634-10640.
- Grace M, Youngster S, Gitlin G, et al. Structural and biologic characterization of pegylated recombinant IFN-alpha2b. J Interferon Cytokine Res 2001; 21:1103-1115.
- Youngster S, Wang YS, Grace M, Bausch J, Bordens R, Wyss DF. Structure, biology, and therapeutic implications of pegylated interferon alpha-2b. Curr Pbarm Des 2002; 8:2139-2157.
- F.Hoffmann-La Roche. PEGASYS Summary of Product Characteristics, revised 2007. 2007.
- Schering-Plough Corporation. Peglntron Summary of Product Characteristics, revised 2007. 2007.
- Algranati NE, Sy S. Modi M. A branched methoxy 40 kDa polyethylene glycol (PEG) moiety optimizes the pharmacokinetics (PK) or peginterferon alfa-2a (PEC-IFN) and may explain its enhanced efficacy in chronic hepatitis C (CHC). Hepatology 1999; 30:190A.
- Modi MW, Fried MW, Reindollar RW, et al. The pharmacokinetic behavior of pegylated (40kDa) interferon alfa-2a (PEGASYS™) in chronic hepatitis C patients after multiple dosing. Hepatology 2000; 32 Pt 2:394.
- Kieffer TL, Sarrazin C, Miller JS, et at. Telaprevir and pegylated interferon-alpha-2a inhibit wild-type and resistant fenotype 1 hepatitis C virus replication in patients. iepatology 2007; 46:631-639.
- Zeuzem S, Sarrazin C, Wagner F, et al. Combination therapy with the HCV protease inhibitor, SCH 503034, plus Peglntron in hepatitis C genotype-1 Peg-Intron non-responders: Phase IB results. Hepatology 2005; 42 Suppl 1:276A.
- Sarrazin C, Rouzier R, Wagner F, et al. SCH 503034, a novel hepatitis C virus protease inhibitor, plus pegylated interferon alpha-2b for genotype 1 nonresponders. Gastroenterology 2007; 132:1270-1278.
- Formann E, Jessner W, Bennett L, Ferenci P. Twice-weekly administration of peginterferon-alpha-2b improves viral kinetics in patients with chronic hepatitis C genotype 1. / Viral Hepat 2003; 10:271-276.
- Glue P, Fang JW, Rouzier-Panis R, et al. Pegylated interferon-alpha2b: pharmacokinetics, pharmacodynamics, safety, and preliminary efficacy data. Hepatitis C Intervention Therapy Group, Clin Pharmacol Ther 2000; 68:556-567.
- Herrmann E. Sarrazin C. Hepatitis-C-virus - viruskinetik und resistenzmecnanismen [Hepatitis C-virus - virus kinetics and resistance mechanisms]. Z Gastroenterol 2004; 42:387-396.
- Herrmann E, Lee JH, Marines G, Modi M, Zeuzem S. Effect of ribavirin on hepatitis C viral kinetics in patients treated with pegylated interferon. Hepatology 2003; 37:1351-1358.
- Zeuzem S, Herrmann E, Lee JH, et al. Viral kinetics in patients with chronic hepatitis C treated with standard or peginterferon alpha2a. Gastroenterology 2001; 120:1438-1447.
- Neumann AU, Lam NP, Dahari H, et al. Hepatitis C viral dynamics in vivo and the antiviral efficacy of interferon-alpha therapy. Science 1998; 282:103-107.
- Karino Y, Toyota J, Sugawara M, et al. Hepatitis C virus genotypes and hepatic Tibrosis regulate 24-n decline of serum hepatitis C virus RNA during interferon therapy in patients with chronic hepatitis C. / Gastroenterol Hepatol 2003; 18:404-410.
- Dusheiko G, Nelson D, Reddy KR. Ribavirin considerations in treatment optimization. Antivir Tber 13 Suppl 1:23-30.
- Lee SS, Heathcote EJ, Reddy KR, et al. Prognostic factors and early predictability of sustained viral response with peginterferon alfa-2a (40KD)./ Hepatol 2002; 37:500-506.
- Dienstag JL, McHutchison JG. American Gastroenterological Association technical review on the management of hepatitis C. Gastroenterology 2006; 130:231-264.
- Ferenci P, Formann E, Laferl H, et al. Randomized, double-blind, placebo-controlled study of peginterferon alfa-2a (40KD) plus ribavirin with or without amantadine in treatment-naive patients with chronic hepatitis C genotype 1 infection./ Hepatol 2006; 44:275-282.
- von Wagner M, Huber M, Berg T, et al. Peginterferon-alpha-2a (40KD) and ribavirin for 16 or 24 weeks in patients with genotype 2 or 3 chronic hepatitis C. Gastroenterology 2005; 129:522-527.
- Shiffman ML, Suter F, Bacon BR, et al. Peginterferon alfa-2a and ribavirin for 16 or 24 weeks in HCV genotype lor 3. N EnglJ Med 2007; 357:124-134.
- Zeuzem S, Hultcrantz R, Bourliere M, et al. Peginterferon alfa-2b plus ribavirin for treatment of chronic hepatitis C in previously untreated patients infected with HCV genotypes 2 or 3. / Hepatol 2004; 40:993-999.
- Mangia A, Santoro R, Minerva N, et al. Peginterferon alfa-2b and ribavirin for 12 vs. 24 weeks in HCV genotype 2 or 3. N EnglJ Med 2005; 352:2609-2617.
- Jacobson IM, Brown RS, Freilich B, et al. Weight-based ribavirin dosing (WBD) increases sustained viral response (SVR) in patients with chronic hepatitis C (CHC): final results of the WIN-R study, a US community based trial. Hepatology 2005; 42 Suppl 1:749A.
- Swain MG, Lai MY, Shiffman M, et al. Durable sustained virological response after treatment with peginterferon alpha-2a (PEGASYS) alone or in combination with ribavirin (COPEGUS): 5-year follow-up and the criteria of a cure.
J Hepatol 2007; 46 Suppl 1:S3. - Diago M, Castellano G, Garcia-Samaniego J, et al. Association of pretreatment serum interferon gamma inducible protein 10 levels with sustained virological response to peginterferon plus ribavirin therapy in genotype 1 infected patients with chronic hepatitis C. Cut 2006; 55:374-379.
- Lee SS, Bain VG, Peltekian K, et al. Treating chronic hepatitis C with pegylated interferon alfa-2a (40 KD) and ribavirin in clinical practice. Aliment Pharmacol Ther 2006; 23:397-408.
- Zehnter E, Huppe D, Mauss S, et al. Efficacy of peginterferon alfa-2a (40KD) (PEGASYS®) and ribavirin in patients with chronic hepatitis C in a real world setting - a contribution to health care research. Hepatology 2005; 42 Suppl 1:683A.
- Bain VG, Lee SS, Peltekian K, et al. Exposure to ribavirin predicts EVR and SVR in patients with HCV genotype 1 infection: analysis of the Canadian PEGASYS® Expanded Access Program. Hepatology 2006; 44:335A-336A.
- Sylvestre D, Smith A, Barrett L, Greene D. A prospective double-blinded neuropsychiatric comparison of pegylated interferons alfa-2a and alfa-2b. Hepatology 2006; 44 Suppl 1:337A.
- Sarrazin C, Gartner BC, Sizmann D, et al. Comparison of conventional PCR with real-time PCR and branched DNA-based assays for hepatitis C virus RNA quantification and clinical significance for genotypes 1 to 5. / Gin Microbiol 2006; 44:729-737.
- Sorensen HT, Lash TL, Rothman KJ. Beyond randomized controlled trials: a critical comparison of trials with nonrandomized studies. Hepatology 2006; 44:1075-1082.
- Grimes DA, Schulz KF. An overview of clinical research: the lay of the land. Lancet 2002; 359:57-61.

Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


