
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 11.10.2024 Штучний інтелект у фармації: перспективи, переваги та потенційні ризики
- Новини 27.08.2024 Вакансії медсестри у Вінниці: особливості та вимоги до кандидатів
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
Бифосфонаты в терапии постменструального остеопороза
Остеопороз — это прогрессирующее системное заболевание скелета, характеризующееся снижением плотности и нарушением микроархитектоники костной ткани с постоянным увеличением хрупкости костей и риска переломов. Актуальность проблемы остеопороза в современной медицине вызвана прежде всего социальными и экономическими последствиями переломов. При этом проблема остеопороза в перспективе должна приобрести еще более глобальный характер, поскольку в современном обществе наблюдается у величение продолжительности жизни, всеобщее постарение населения.
Большую часть людей, подверженных остеопорозу, составляют женщины. За первые 5 лет после наступления менопаузы потеря костной массы у женщины может составить до 1/3 от костной массы, утраченной за всю жизнь [7, 11 ]. В постменопаузе почти у 30% женщин отмечается остеопороз, а примерно у 54 % — остеопения, что предопределяет их уязвимость для развития остеопороза и остеопоротических переломов. Так, для 50-летней женщины риск перелома позвоночника составляет в среднем 15,5%, шейки бедра— 17,5%, костей запястья — 16,0%, а любого из трех участков скелета — 39,7%. Кроме того, 50% женщин старше 50 лет в течение своей последующей жизни переносят остеопо-ротический перелом [18].
Остеопороз — основная причина переломов шейки бедра, часто встречающихся у женщин старше 65 лет. У лиц пожилого возраста 90% переломов шейки бедра, как показали международные исследования, происходят на фоне остеопороза [7, 11]. К сожалению, наметилась четкая тенденция к увеличению частоты переломов шейки бедра на фоне остеопороза и в возрастной группе 50-60 лет. Последствия переломов шейки бедра катастрофические: 20% больных погибают в течение полугода, у половины выживших после перелома бедра снижается качество жизни, а треть нуждаются в длительном уходе показываются в зависимом состоянии [1, 2, 11]. Переломы проксимального отдела бедра считаются наиболее затратными, так как помимо прочего требуют госпитализации. Поданным ВОЗ, именно переломы проксимального отдела бедренной кости ставят остеопороз на 4-е место среди всех причин инвалидности и смертности [1, 11, 18].
В настоящее время существуют эффективные программы профилактики и лечения остеопороза, включающие сочетание нефармакологических методов с современными противоостеопоротическими препаратами. Ранняя профилактика и лечение остеопороза позволяют замедлить развитие заболевания, снизить частоту переломов костей и улучшить качество жизни пациента. Основными целями лечения остеопороза являются замедление или прекращение потери костной массы, предотвращение возникновения переломов, уменьшение болевого синдрома и улучшение качества жизни. Среди средств патогенетической фармакотерапии остеопороза, в зависимости от преобладающего механизма действия, выделяют три основные группы: препараты, замедляющие костную резорбцию; препараты, стимулирующие костеобразование; лекарственные средства многопланового действия.
Среди препаратов, подавляющих костную резорбцию, бифосфонаты наиболее широко применяются в терапии остеопороза и другой патологии костей [4, 20, 22]. Это класс лекарственных препаратов, созданных на основе неорганических пирофосфатов, синтетические производные фосфоновых кислот, которые отличаются в своей химической структуре заменой атома кислорода в молекуле пирофосфата на атом углерода — Р-С-Р. Кроме того, в структуре боковых цепей бифосфонатов имеются два радикала, один из которых облегчает физико-химическое связывание бифосфонатов с гидроксиапатитом, а другой — определяет биологическое действие препаратов на костные клетки [2, 7]. Селективное действие бифосфонатов на костную ткань связано с их высоким сродством с кристаллами гидроксиапатита кости. Это свойство определяет их способность откладываться в местах образования новой кости. Бифосфона-ты сохраняются в местах нового костеобразования до тех пор, пока не произойдет замена старой кости на новую кость [1, 8]. Основным фармакологическим эффектом бифосфонатов является снижение костного ремоделирования с более выраженным угнетением костной резорбции, чем костеобразования, а также снижение частоты активации ремоделирования. Препараты уменьшают или предупреждают отрицательное влияние на кость практически всех известных стимуляторов резорбции [4, 14]. Проникая в костную ткань, бифосфонаты концентрируются вокруг остеокластов, создавая высокую концентрацию в лакунах резорбции. В исследованиях in vitro было показано, что бифосфонаты влияют на глубину лакун резорбции, уменьшая ее.
Антирезорбционная активность отдельных препаратов из этой группы существенно варьирует, что связано с особенностями химической структуры.
Ниже перечислим бифосфонаты в зависимости от их активности.
- 1 × — этидронатовая кислота (ксидифон, дидронель);
- 10 × — клодроновая кислота (бонефос, лодронат, остак), тилудроновая кислота (скелид);
- 1 00 × — памидроновая кислота (аредиа, аминомакс);
- 1 000 × — алендроновая кислота (фосамакс, остеотаб);
- 1 0000 × — ризедроновая кислота (актонель), ибандроновая кислота (бонвива), золедроновая кислота (зомета, акласта).
Первое поколение бифосфонатов — этидронат, клодронат динатрий итилудронат, не содержащих в своей структуре атомов азота, метабо-лизируются остеокластами внутриклеточно до цитотоксичных аналогов аденозин трифосфата. Блокируя синтез фарнезил-дифосфат синтазы, азотсодержащие бифосфонаты снижают образование мевалоната, который необходим для поддержания нормальной цитоархитектоники и жизнедеятельности остеокластов [21, 22]. Последние являются более сильными ингибиторами остеокластической активности и остеолизиса, чем препараты, не содержащие в своей структуре азота [24]. Структурные отличия в азотсодержащей цепочке бифосфонатов также влияют на их эффективность в отношении ингибирования костной резорбции.
Бифосфонаты захватываются остеокластами, где они нарушают формирование цитоскелета, необходимого для прикрепления остеокласта к костной ткани, а также снижают секрецию лизосомальных ферментов. Клеточный механизм действия бифосфонатов заключается в прямом ингибировании активности остеокластов, их подвижности, а также блокировании связывания остеокластов с костной тканью [20, 21]. Присутствие атома азота в боковой цепи объясняет особый механизм действия азотсодержащих бифосфонатов, связанный со способностью ингиби-ровать процесс модификации белков в остеокластах, что ведет к апоптозу зрелых клеток и подтверждается появлением специфических изменений в клетке и структуре ядра [13, 24]. Действие азотсодержащих бифосфонатов, кроме того, ведет к потере клетками-предшественниками остеокластов способности дифференцировки и созревания, что в дальнейшем влечет за собой уменьшение популяции остеокластов. Однако точный молекулярный механизм действия бифосфонатов до сих пор не выяснен.
Наряду с антирезорбционными эффектами, бифосфонаты обладают тормозящим влиянием на процессы минерализации тканей скелета и мягких тканей [2, 21 ]. Остеобласты также являются потенциальными мишенями для бифосфонатов, поскольку влияют на функциональную активность остеокластов. Данные in vitro свидетельствуют о том, что под влиянием бифосфонатов остеобласты снижают секрецию остеокластстимулирую-щего фактора [1, 13, 14].
Помимо антирезорбционного действия, бифосфонаты обладают рядом анаболических эффектов, поскольку блокируют апоптоз остеобластов и остеоцитов и стимулируют образование новой кости [19, 21]. Важно отметить положительное влияние бифосфонатов на механическую прочность кости. Длительное применение бифосфонатов сопровождается положительными изменениями микроархитектоники кости, увеличением толщины трабекул. Так, гистоморфометрическое исследование костных биоптатов показало, что микроархитектоника кости у женщин, получавших лечение бифосфонатами в течение 5-10 лет, соответствует микроархитектонике пременопаузальных женщин [19]. Всасывание препаратов происходит частично в желудке, и в основном — в тонком кишечнике [2, 6]. При пероральном приеме бифосфонатов всасывается 1-10% препарата, однако от 20 до 50% всосавшегося препарата депонируется в костях. Процесс всасывания снижается при их приеме одновременно с пищей, а также в присутствии солей кальция и железа. Также абсорбционный процесс уменьшают средства антацидного ряда. В костной ткани они сохраняются в течение очень длительного времени, практически всю оставшуюся часть жизни индивидуума [1,2, 20]. Бифосфонаты неметаболизируются в организме и выводятся с мочой в неизмененном виде.
К числу побочных эффектов бифосфонатов при пероральном использовании относятся прежде всего нарушения со стороны желудочно-кишечного тракта (6-30% случаев): тошнота, рвота, диспепсические явления, абдоминальные боли, изъязвления слизистой оболочки пищевода и желудка [6, 10, 15]. Риск побочных явлений со стороны желудочно-кишечного тракта повышается при одновременном назначении вместе с нестероидными противовоспалительными препаратами. Редко наблюдаются мышечные и головные боли, кожные аллергические реакции и транзиторное повышение температуры. При внутривенном введении, особенно при несоблюдении правила медленной инфузии раствора, могут наблюдаться повреждения почек. Поскольку препараты этой группы проникают через плаценту и способны отрицательно влиять на плод, их не следует применять во время беременности.
Одним из условий эффективного лечения остеопороза бифосфонатами при наличии у больного гипокальциемии является обязательная ее коррекция до начала терапии. Длительная терапия бифосфонатами эффективна при дополнительном приеме солей кальция (1-1,5 г/сут) и 500 ME витамина D [6, 8, 17]. Интервал между приемом бифосфонатов и других лекарственных препаратов должен составлять как минимум 1 ч.
В клинической практике бифосфонаты эффективно используются для лечения практически всех форм остеопороза, а также терапии гипер-кальциемии, остеолитических состояний при злокачественных опухолях и метастазировании в кости [4, 21, 23].
До настоящего времени при остеопорозе на практике в основном использовались этидроновая и алендроновая кислоты как наиболее изученные препараты. Наибольший опыт лечения больных остеопорозом накоплен в отношении препаратов первого поколения (этидроновая кислота). Алендроновую кислоту, представителя группы аминобифосфонатов, при остеопорозе назначают по 70 мг 1 раз в неделю или по 10 мг ежедневно. Препарат, как и другие бифосфонаты, следует применять за 60 мин до приема пищи. Необходимо сохранять вертикальное положение тела в течение часа после приема.
Терапия остеопороза, являющегося тяжелым хроническим заболеванием, должна проводиться в течение длительного времени. В связи с этим нередко на практике возникает проблема приверженности больных к лечению, тесным образом связанная с эффективностью терапии. Широкие клинические перспективы имеет бифосфонат нового поколения бонвива (ибандроновая кислота), основное преимущество которого состоит не только в большей антирезорбтивной активности, но и в возможности применения 1 таблетки 1 раз в месяц при терапии больных остеопорозом [15, 16, 23]. Так, при изучении возможности ибандроновой кислоты вызывать угнетение костной резорбции на модели ретиноид-индуцированной костной резорбции было показано ее значительное преимущество по отношению к памидроновой и алендроновой кислотам [21].
Бонвива (ибандроновая кислота) относится к азотсодержащим бифосфонатам третьего поколения и используется в терапии остеопороза перо-рально по 150 мг 1 раз в месяц [16, 22, 24]. После всасывания бонвива быстро распределяется, и 40-50% дозы препарата, находящегося в системной циркуляции, связывается с костной тканью и накапливается в ней, что соответствует концепции о высоком сродстве препарата с гидроксиапатитом кости. После связывания с минералами кости высвобождение препарата осуществляется чрезвычайно медленно. Биодоступность не снижается, если принимать пищу не ранее чем через 1 ч после приема препарата. Как и другие бифосфонаты, бонвива не метаболизируется в организме и в неизмененном виде экскретируется с мочой. Клиренс ибандроновой кислоты зависит от функции почек. Часть препарата, связавшаяся с костной тканью, не элиминируется из организма до тех пор, пока в этом участке кости не завершится процесс костного ремоде-лирования. Согласно данным экспериментальных исследований, период полувыведения бонвивы из костей составляет около 1 года.
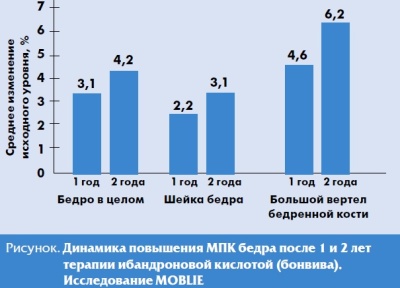
Клиническая эффективность бонвива была подтверждена данными ряда многоцентровых исследований по изучению влияния различных доз ибандроновой кислоты на минеральную плотность кости (МПК) и качество кости, риск развития новых переломов и переносимость препарата [16, 22, 24]. Результаты исследования MOBILE (многоцентровое, рандомизированное, двойное слепое) показали, что при частоте введения ибандроновой кислоты 1 раз в месяц у женщин с постменопаузальным остеопорозом минерализация костной ткани поясничного отдела позвоночника повышается столь же эффективно, как и при ежедневном приеме 2,5 мг [16]. В исследование были включены 1609 женщин (возраст 55-80 лет) с продолжительностью постменопаузы 5 лет и более, имевших диагностированный остеопороз в поясничном отделе позвоночника (Т-критерий МПК от -2,5 СО идо -5,0 СО). Пациентам назначались несколько режимов приема бонвивы или плацебо: 2,5 мг бонвивы в сутки внутрь и плацебо 1 раз в месяц; 100 мг бонвивы внутрь 1 раз в месяц и ежедневный прием плацебо; 100 мг бонвивы внутрь 1 раз в месяц по 50 мг/сут 2 дня подряд (50/50 мг) и ежедневный прием плацебо; 150 мг бонвивы внутрь 1 раз в месяц и ежедневный прием плацебо. Кроме того, все участники исследования ежедневно принимали препараты кальция (500 мг) и витамина D (400 ME). Первичной конечной точкой при оценке эффективности было изменение показателей МПК поясничных позвонков через 1 год лечения по сравнению с исходным уровнем. Вторичные конечные точки эффективности включали динамику МПК поясничных позвонков через 2 года, МПК проксимального отдела бедра через 1 и 2 года терапии, изменение уровня маркеров костного обмена (С-телопептида СХ-цепи коллагена I типа (СТх) сыворотки крови) через 1 и 2 года. Через 1 год было отмечено достоверное повышение МПК поясничного отдела позвоночника относительно исходных показателей на 4,3% при приеме 50 мг/50 мг бонвивы, на 4,1 % — при приеме 1 00 мг, на 4,9% — при ежемесячном приеме 150 мг и на 3,9%— при ежедневном приеме 2,5 мг бонвивы [9]. Прирост МПК поясничных позвонков через 2 года исследования составил 5,3%, 5,6% и 6,6% при приеме соответственно 50 мг/50 мг, 100 мг и 150 мг бонвивы и на 5,0% при ежедневном приеме препарата [25]. Достоверное увеличение показателей МПК бедра в целом, шейки бедра и области большого вертела отмечалось во всех группах лечения через 1 год после проведения терапии и сохранялось в течение второго года лечения, (рис.). По сравнению с ежедневным режимом приема препарата прием 150 мг бонвивы 1 раз в месяц сопровождался самым большим и прогрессивным увеличением показателей МПК во всех точках обследования проксимальных отделов бедренной кости (р < 0,05 через 2 года). Изучение уровня маркеров костного обмена показало снижение их уже через 3 мес лечения. Снижение продолжалось в течение всего периода наблюдения. Через 2 года уменьшение уровня СТх сыворотки крови составило 56,1-61,5% в группах лечения с наибольшим снижением в группе, получавшей 150 мг ибандроновой кислоты.
В рамках исследования BONE проводились гистологические и гистоморфометрические анализы костных биоптатов в подгруппе пациенток, участвовавших в программе по оценке влияния интермиттирующего и ежедневного приема ибандроновой кислоты на качество и микроархитектонику костной ткани [6]. Полученные результаты показали, что как интермиттирующий, так и ежедневный прием бонвивы перорально ассоциировался сформированием новой кости без признаков нарушения минерализации костного матрикса, при этом отмечались признаки улучшения ее микроархитектоники.
Как было отмечено выше, эффективность терапии любого хронического заболевания тесно связана с приверженностью пациента лечению. Результаты многоцентрового исследования BALTO, посвященного сравнительной оценке приверженности пациентов лечению, показали, что 66,1% женщин с постменопаузальным остеопорозом предпочитают ежемесячный прием 150 мг бонвивы еженедельному приему 70 мг алендроновой кислоты [9].
Результаты приведенных и ряда других исследований также свидетельствовали о том, что относительно большая доза, которая была необходима для приема препарата в режиме 1 раз в месяц, не оказывала существенного влияния на переносимость бонвивы. Кроме того, прием бонвивы не ассоциировался с повышенным риском развития побочных эффектов со стороны верхних отделов желудочно-кишечного тракта [16, 22, 24].
В заключение следует отметить, что бонвива является эффективным средством терапии остеопороза. Длительное его применение в комплексном лечении различных форм остеопороза приводит не только к прогрессивному увеличению МПК в поясничном отделе позвоночника и проксимальном отделе бедренной кости, но и снижает риск переломов позвонков.
Литература
1. Риггз Б.Л ., Мелтон Л. Д. Остеопороз. Этиология, диагностика, лечение. М.: Бином, 2000.
2. Щварц Г.Я . Фармакотерапия остеопороза. М.: Медицинское информационное агентство, 2002.
3.Amin S., Felson D. P. Osteoporosis in men// Rheumatic disease clinics of North America. 2001; 27(1): 19-47.
4. Boivin G. Y., Chavassieux P. M., Santora A. C, Yates Jv Meun/er P. J. Alendronate increases bone strength by increasing the mean degree of mineralization of bone tissue in osteoporotic women// Bone. 2000; 27(5): 687-694.
5. Bone H. G., Hosfcing D., Devogelaer J. P. et al. Alendronate Phase III Osteoporosis Treatment Study Group. Ten years' experience with alendronate for osteoporosis in postmenopausal women// N. Engl. J. Med. 2004; 350( 1 2): 1189-99.
6. Chesnuf C. H. Skag A., Christiansen C. et al. Effects of oral ibandronate administered daily or intermittently on fracture risk in postmenopausal osteoporosis// J. Bone Miner. Res. 2004; 19(8): 1241-1249.
7. Davidson M. R. Pharmacotherapeutics for osteoporosis prevention and treatment// J. Midwifery Womens Health. 2003; 48: 39-52.
8. Eastell R. Treatment of Postmenopausal Osteoporosis. N. Engl. Med. J. 1998; 338(11): 736-746.
9. Emfcey P., Koltun W., Beusrerien K. et al. Patient preference for once-monthly ibandronate versus once-weekly alendronate in a randomized, open-label, cross-over trial: the Boniva Alendronate Trial in Osteoporosis (BALTO)// Curr Med Res Opin. 2005;21(12): 1895-1903.
10. Ensrud K. E., Barrett-Connor E. L., Schwartz A. et al. Fracture Intervention Trial Long-Term Extension Research Group. Randomized trial of effect of alendronate continuation versus discontinuation in women with low BMD: results from the Fracture Intervention Trial long-term extension//J. Bone Miner Res. 2004; 19(8): 1259-69.
11. Heaney R. P. Advances in therapy for osteoporosis// Clin. Med. Res. 2003; 1 (2): 93-99.
12. Hodsman B., Han/ey D. A., Josse R. Effects of oral ibandronate administered daily or intermittently on fracture risk in postmenopausal osteoporosis// J. Bone Miner Res. 2004; 19(8): 1241-1249.
13. Hughes D. E., Wright K. R., Uy H. L. et al. Bisphosphonates promote apoptosis in murine osteoclasts in vitro and in vivo// J. Bone Miner Res. 1995; 10: 1478-1487.
14. Mashiba J., Turner C. H., Hirano T. et al. Effects of suppressed bone turnover by bisphosphonates on microdamage accumulation and biomechanical properties in clinically relevant skeletal sites in beagles// Bone. 2001; 28(5): 524-31.
15. Mellsfrom D. D. Sorensen O. H., Goemaere S. et al. Seven Years of Treatment with Risedronate in Women with Postmenopausal Osteoporosis// Calcif Tissue Int. 2004; 75(6): 462-468.
1 6. Miller P. D., McClung M., Macoveil. etal. Monthly oral ibandronate therapy in postmenopausal osteoporosis: 1-year results from the MOBILE study// J. Bone Miner. Res. 2005; 20: 1315-1322.
17. Monier-Faugere M. C, Geng Z. Paschalis E. P. et al. Intermittent and continuous administration of the bisphosphonate ibandronate in ovariectomized beagle dogs: effects on bone morthometry and mineral properties// J. Bone Miner. Res. 1999; 14: 1768-1778.
18. Nguyen T. V., Center J. R., Eisman J. A. Osteoporosis: underdiagnosed and undertreated. Med. J. Aust. 2004; 180(5): 18–22.
19. Recker R., Ensrud K., Diem S. et al. Normal bone histomorphometry and 3D microarchitecture after 10 years alendronate treatment of postmenopausal women// J. Bone Miner. Res. 2004; 19:45.
20. Rodan G., Reszka A., Golub E., Rizzoli R. Bone safety of long-term bisphosphonate treatment// Curr. Med. Res. Opin. 2004; 20(8): 1291–1300.
21. Rogers M. J. New insights into molecular mechanisms of action of bisphosphonates// Curr. Pham. Des. 2003; 9: 2643–58.
22. Papapoulos S. E. Ibandronate: a potent new bisphosphonate in the management of postmenopausl osteoporosis//IJCP. 2003; 57: 417–422.
23. Pecherstorfer M., Steinhauer E. U., Rizzoli R. et al. Efficacy and safety of ibandronate in the treatment of hypercalcemia of malignancy: a randomized multicentric comparison to pamidronate// Support Care Cancer. 2003; 11(8): 539-47.
24. Pyon E. Y. Once-monthly ibandronate for postmenopausal osteoporosis: review of a new dosing regimen// Clin Ther. 2006; 28(4): 475–490.
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


