
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 11.10.2024 Штучний інтелект у фармації: перспективи, переваги та потенційні ризики
- Новини 27.08.2024 Вакансії медсестри у Вінниці: особливості та вимоги до кандидатів
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
Вемурафениб – новый сертифицированный препарат для лечения неоперабельного рака кожи
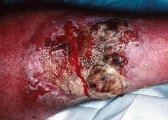
Управление по контролю за качеством пищевых продуктов и лекарственных препаратов США (англ. Food and Drug Administration – FDA) заявило об успешной сертификации препарата Zelboraf (вемурафениб) для лечения ряда тяжелых форм метастатического рака кожи и меланобластом, не подлежащих хирургическому удалению.
Препарат Zelboraf (вемурафениб) сертифицирован для лечения форм меланомы, вызванных мутацией BRAF V600E. Белок BRAF регулирует рост клеток здорового человека, но его мутации приводят к развитию тяжелых форм рака кожи – около 50% случаев неоперабельной меланомы связаны с BRAF-мутацией.
Препарат Zelboraf – ингибитор, блокирующий функции BRAF-белков с мутацией V600E. Безопасность и эффективность препарата была установлена в ходе международного испытания с участием 675 пациентов с тяжелой формой меланомы и наличием BRAF V600E мутаций, не получавших предварительной терапии. Результаты впечатляющи – 77% пациентов, получавших лечение вемурафенибом, были живы на момент сертификации (17.08.2011). Эффективность препарата Zelboraf в случаях рака кожи, не связанных с мутацией гена BRAF, не была исследована.
Среди самых распространенных побочных эффектов препарата Zelboraf, обнаруженных в ходе клинических испытаний, боль в суставах, высыпания на коже, потеря волос, головокружения, утомляемость и повышенная чувствительность кожи к солнечным лучам. У 26% пациентов сформировалась операбельная форма рака клеток плоского эпителия. FDA обязала производителей выпускать препарат вместе с подробной медицинской инструкцией.
Наряду с препаратом вемурафениба, одобрение FDA получил инновационный диагностический тест, позволяющий проверить наличие мутации BRAF V600E (cobas 4800 BRAF V600 Mutation Test). Для клинических испытаний точности диагностики были использованы образцы тканей пациентов, принимавших участие в испытаниях самого препарата.
«Zelboraf и сопровождающий его тест – это великолепный пример целевой диагностики и последующей эффективной, безопасной терапии, соответствующей потребностям отдельно взятого пациента», – говорит директор отдела оценки эффективности и безопасности средств In vitro диагностики центра исследовании аппаратных средств и радиологии FDA.
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


