
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 11.10.2024 Штучний інтелект у фармації: перспективи, переваги та потенційні ризики
- Новини 27.08.2024 Вакансії медсестри у Вінниці: особливості та вимоги до кандидатів
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
Многоцентровое исследование применения Lactobacillus GGс пероральным раствором для регидратации у детей с острой диареей
Было проведено многоцентровое исследование, цель которого — изучить эффективность Lactobacillus GG в применении с пероральным раствором для регидратации у пациентов с острой диареей.
Применение пробиотика Lactobacillus GG эффективно, — способствует более быстрому выздоровлению детей с ротавирусным энтеритом с симптомами острой водянистой диареи.
Однако, известно несколько исследований потенциальной роли Lactobacillus GG в лечении пациентов с диареей неротавирусной этиологии. Кроме того, нет данных об эффективности Lactobacillus GG, назначенной с пероральным раствором для регидратации во время пероральной регидратирующей терапии.
Было проведено многоцентровое исследование, цель которого — изучить эффективность Lactobacillus GG в применении с пероральным раствором для регидратации у пациентов с острой диареей.
Методы: дети в возрасте от одного мес. до 3 лет с острой диареей были включены в двойное слепое плацебо-контролируемое исследование. Пациенты бали рандомизированы на группу А, которая получала пероральный раствор для регидратации плюс плацебо, и группу В, которая получала тот же препарат плюс препарат живых Lactobacillus GG (как минимум 1010 колониеобразующих единиц/250 мл). После регидратации в течение первых 4-6 часов, пациентам было предложено их обычное питание плюс свободный доступ к аналогичному раствору до прекращения диареи.
Результаты: в группу А было включено 140 детей, в группу В — 147 детей. На момент госпитализации между группами не было различий в возрасте, поле, предшествующих видах кормления, предшествующей продолжительности диареи, применении антибиотиков, массе тела, росте, соотношениях массы тела/роста, распространенности лихорадки, состоянии в целом и степени дегидратации. Продолжительность диареи после включения в исследование составила 71,9 ± 35,8 часов в группе А по сравнению с 58,3 ± 27,6 часов в группе В (средняя ± стандартное отклонение, р = 0,03). У детей, инфицированных ротавирусом, диарея продолжалась 76,6 ± 41,6 часов в группе А по сравнению с 56,2 ± 16,9 часов в группе В (р < 0,008). Диарея продолжалась более 7 дней у 10,7% пациентов в группе А по сравнению с 2,7% пациентов в группе В (р < 0,01). Длительность госпитализации была существенно меньше в группе В, чем в группе А.
Выводы: пероральное применение раствора для регидратации, содержащего Lactobacillus GG, у детей с острой диареей безопасно и эффективно. Приводит к уменьшению продолжительности диареи, снижает вероятность развития затяжного течения заболевания и сокращает длительность госпитализации.
Острая диарея сегодня является достаточно распространенной патологией. Особую ценность приобретают медикаментозные средства, которые безопасно и эффективно сокращают продолжительность заболевания или предотвращают развитие затяжной формы заболевания. В последние годы было показано, что пробиотик Lactobacillus GG(АТС 53103), штамм, который, как известно, колонизирует кишечник человека, эффективен в обеспечении более быстрого выздоровления детей с острой водянистой диареей ротавирусной этиологии [в Украине препараты, содержащие пробиотик Lactobacillus GG, представлены в частности торговыми марками Бифиформ® Комплекс, Бифиформ® Детский и Мультитабс® Иммуно, производства Датской компании Ферросан (прим. редакции)]. В то же время недостаточно данных о потенциальной роли Lactobacillus GG в лечении диареи неротавирусной этиологии. Также неизвестно, эффективны ли Lactobacillus GG в аспекте профилактики развития затяжной формы заболевания или в сокращении продолжительности госпитализации стационарных пациентов. Кроме того, в ранее проведенных исследованиях, пробиотики использовались только в качестве дополнительной терапии после завершения регидратации, в то время как возможно, что их применение на ранних этапах лечения (то есть во время регидратации) более эффективно. Чтобы ответить на эти вопросы, Рабочая группа Острой Диареи Европейского общества Детской Гастроэнтерологии, Гематологии, и Питания начала в 2006 г. исследование продолжительностью 1 год, которое включало 11 центров в 10 странах.
Материалы и методы
Мы включили в исследование детей в возрасте от 1 месяца до 3 лет с более чем 4 дефекациями в день жидким или полужидким стулом на протяжении 1-5 дней. Этические комитеты в лечебных учреждениях, включенных в исследование, одобрили проведение исследования. Критериями исключения из исследования были предшествующее применение любых пробиотиков, хроническое нелеченное заболевание тонкой кишки, и любые другие хронические заболевания или иммуно-супрессивные состояния. Исследование было двойным слепым и плацебо контролируемым. После получения согласия от родителей, пациенты были разделены методом рандомизации на группу А или В. Дети, вошедшие в группу А, получали раствор, приготовленный в каждом центре, путем растворения содержания маленького пакета А в 250 мл воды. Таким образом, создавали гипотонический раствор перорального применения для регидратации (ORS), составленный согласно рекомендациям специального комитета ESPGHAN1 плюс плацебо. Дети, вошедшие в группу В, получали раствор, также приготовленный в каждом центре путем растворения содержания маленького пакета В в 250 мл воды. В результате получали идентичный раствор ORS (см. табл. 1), однако, в него был добавлен препарат живых Lactobacillus GG (как минимум 1010 колониеобразующих единиц/250 мл).
Таблица 1
|
Ингредиент |
Содержаниеа |
|
Глюкоза |
111 |
|
Натрий |
60 |
|
Калий |
20 |
|
Цитрат |
14 |
|
Хлорид |
37 |
|
Аспартам |
4,6 мг/дл |
|
Осмотическая концентрация |
248 mOsm/кг |
а — ммоль/л, если не указано иначе
Пакеты Lactobacillus GG для обеих групп пациентов были предоставлены каждому центру-участнику Dicofarm (Рим, Италия) и хранились в охлажденном виде до применения. Всем пациентам проводилась регидратация в течение первых 4-6 часов в соответствии с рекомендациями специального комитета ESPGHAN1.
Собранные данные включали результаты антропометрических измерений на момент госпитализации, массу тела через короткие временные промежутки, количество и характеристики каждого стула во время наблюдения, потребление жидкости и случаи рвоты.
Образцы стула были собраны на момент госпитализации и каждые 48 часов. У большинства пациентов были сделаны попытки собрать образцы стула на 14 день и 30 день после включения в исследование. Собранные образцы стула были проанализированы на наличие ротавирусов, аденовирусов, Salmonella, Shigella, Campylobacter, Yersinia, Giardia, Cryptosporidium, Amoeba.
В конце исследования был открыт код. Анализ данных был выполнен координационным комитетом при применении программного обеспечения для статистического анализа Epi-Info5, распределенного Центрами контроля заболевания, (Атланта, Джорджия, США). Были изучены: процент неэффективности лечения (определяемый, как необходимость проведения внутривенной регидратации), продолжительность диареи после включения в исследование (определенный, как время в часах до последнего задокументированного жидкого стула), прогрессирование массы тела, процент детей, которым был проведен курс в течение более 7 дней и, для стационарных больных, продолжительность госпитализации. Данные представлены как среднее ± стандартное отклонение. Статистический анализ был выполнен с помощью теста t Стьюдента для непарных случайных величин χ2(где применимо) точного критерия Фишера.
Данные на момент включения в исследование
323 формы были отправлены в координационный центр. Данные из 36 форм были признаны неприемлемыми для оценки в связи с их незаконченностью и/или несоответствием протоколу. Следовательно, для оценки были доступны 287 форм. 140 пациентов были включены в группу А и 147 пациентов — в группу В. На рис. 1 продемонстрировано количество пациентов по разным исследовательским центрам.
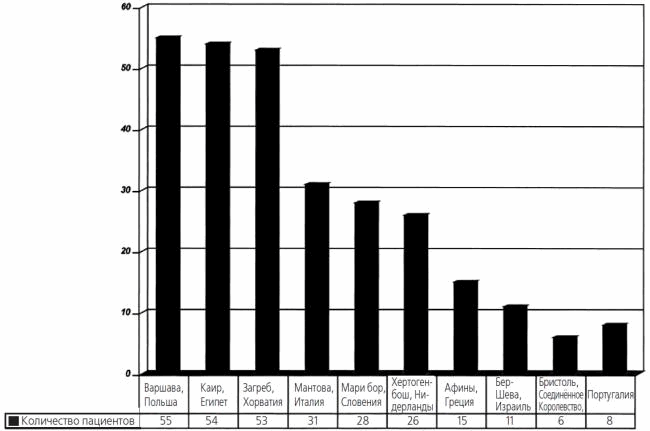
Рис. 1 Распределение 287 пациентов среди центров, участвующих в исследовании. Данные, указанные как группа Португалия, включала 2 центра: Порто (1,7% от общего количества пациентов) и Лиссабон (1% от общего количества пациентов).
В табл. 2 представлены наиболее важные клинические показатели на момент госпитализации.
Таблица 2. Характеристики 287 пациентов на момент включения в исследование. Данные представлены как среднее ± стандартное отклонение, если не указано иначе.
|
Группа А: плацебо (n = 140) |
Группа В: Lactobacillus GG (n = 147) |
p | |
|
Стационарные пациенты (%) |
83 |
90 |
НД |
|
Возраст (месяцы) |
12,1±8,6 |
12,5 ± 8,0 |
НД |
|
Пол (% женского пола) |
37 |
40 |
НД |
|
Масса тела (кг) |
8,75 ± 2,7 |
8,83 ± 2,7 |
НД |
|
Рост (см) |
73,4 ± 11,4 |
73,9 ± 10,2 |
НД |
|
Масса тела — рост (процент) |
33±25 |
30 ± 25 |
НД |
|
Частично вскормленные грудью (%) |
25 |
20,4 |
НД |
|
Предшествующее применение антибиотиков (%) |
17,8 |
18,1 |
НД |
|
Предшествующая продолжительность диареи (часы) |
51,0 ± 30,9 |
52,1 ± 3,1 |
НД |
|
Характеристики стула (%): |
|
|
|
|
Водянистый |
67 |
74,1 |
НД |
|
Редкий |
22,8 |
19,7 |
НД |
|
Слизистый |
28,5 |
21,7 |
НД |
|
Кровянистый |
10,7 |
6,8 |
НД |
|
Рвота (%) |
62 |
58 |
НД |
|
Лихорадка (%) |
58,3 |
60 |
НД |
|
Состояние (%) |
|
|
|
|
хорошее |
45,7 |
37 |
НД |
|
вполне удовлетворительное |
47,8 |
54,4 |
НД |
|
неудовлетворительное |
6,4 |
8,5 |
НД |
|
Нормальная гидратация (%) |
|
8,5 |
НД |
|
Дегидратация (%) |
31 |
|
|
|
легкой степени |
50,7 |
47,6 |
НД |
|
средней степени |
17,5 |
25,1 |
НД |
|
тяжелая |
0,7 |
0,7 |
НД |
|
НД — не достоверно |
|
|
|
Между двумя группами на момент включения в исследование не было различий в проценте амбулаторных больных (процент стационарных больных был высоким в обеих группах), возрасте, поле, массе тела, росте, предшествующих видах кормления, предшествующем применении антибиотиков, предшествующей продолжительности диареи, характеристиках стула, распространенности лихорадки и рвоты, состоянии в целом, и степени дегидратации. Результаты причинной связи, выполненные на момент госпитализации, сообщены в табл. 3.
Таблица 3
|
Патогенный возбудитель |
Группа А (n = 140) |
Группа В (n = 147) |
Р |
|
Рота в и рус |
45 (32%) |
56 (38%0 |
НД |
|
Salmonella |
8 (5,7%0 |
12 (8,2% |
НД |
|
Campylobacter |
9 (6,4%) |
9 (6,1%) |
НД |
|
Entamoeba |
б (4,3%) |
5 (3,4%) |
НД |
|
Аденовирус, кишечный тип |
1 (0,7%) |
4 (2,8%) |
НД |
|
Yersinia |
1 (0,7%) |
1 (0,7%) |
НД |
|
Shigella |
2 (1,4%) |
0 |
НД |
|
Giardia |
0 |
2 (1,4%) |
НД |
|
Escherichia coli |
б (4,3%) |
3 (2,0%) |
НД |
|
Другие или смешанные патогенные возбудители |
8 (5,7%) |
10 (6,8%) |
НД |
|
Известный патогенный возбудитель отсутствовал |
54(38,5%) |
45 (30,6%) |
НД |
Пациенты группы А получали только раствор для регидратации для перорального применения. Пациенты группы В получали раствор для регидратации для перорального применения с добавлением Lactobacillus GG. Представленные данные ― количество пациентов с диареей (процент группы).
НД ― недостоверно.
а ― Escherichia coli относится к наличию данного вида как единственный бактериальный штамм. Однако не была выполнена дальнейшая характеристика патогенности. Даже если эти пациенты были классифицированы с пациентами без известного патогенного возбудителя, различия между группой А (60, 42%) и группой В (48, 32,6%) оставались незначимыми (р = 0,07).
Ротавирус был единственным патогенным возбудителем, который наиболее часто выявлялся в обеих группах (32% в группе А, 38% в группе В). В группе А был 21 пациент и в группе В было 22 пациента (по 15% в каждой группе) с инвазивным энтеритом (Salmonella, Campypobacter, Yersinia ). У 49 (35%) пациентов в группе А и у 35 (24%) пациентов в группе В не было идентифицированного патогенного возбудителя в образцах стула (статистическое различие; р = 0,05). Между двумя группами не наблюдалось статистическое различие в частоте выявления любых из выявленных патогенных возбудителей.
Исходы. Неэффективность терапии
У 11 пациентов группы А (7,8%) и у 12 пациентов группы В (8,1%, р = не достоверно) пероральная регидратация была неэффективна. Этим пациентам в связи с дегидратацией средней-тяжелой степени проводилась внутривенная регидратация. В итоге, состояние пациентов нормализовалось. Причины неэффективности лечения были сопоставимыми в обеих группах. Наиболее частой причиной была сильная рвота. Лечение было неэффективным у трех пациентов в группе А и у одного пациента в группе В в связи с их отказом принимать ORS. Этим пациентам проводилась внутривенная регидратация. Данные об этих пациентах были исключены из дальнейшего анализа.
Прием внутрь раствора для пероральной регидратации
Количество принятого ORS представлено в табл. 4 для исследуемой и контрольной группы. Во время фазы регидратации (первые 4 часа) или впоследствии не было отмечено существенных различий между группами в приеме внутрь указанного раствора.
Таблица 4. Прием внутрь раствора для пероральной регидратации
|
|
Группа А |
Группа В |
Р |
|
Во время ORT (первые 4 часа) |
347 + 183,3 (10-850) |
381,7 ± 222,5 (50-1000) |
НД |
|
Во время последующих 20 часов |
403 +24,8 (0-1580) |
459 + 252(15-1300) |
НД |
|
Общее количество |
1050 + 671,6 (40-3900) |
1193,6 + 948 (80-5120) |
НД |
Пациенты группы А получали только раствор для регидратации для перорального применения. Пациенты группы получали раствор для регидратации для перорального применения при добавлении Lactobacillus GG. Представленные данные — средний прием в миллилитрах ± стандартное отклонение (диапазон).
ORT — пероральная регидратационная терапия.
НД ― недостоверно.
Продолжительность диареи
В таблице 5 представлены данные о продолжительности диареи до и после включения в исследование. Сообщены данные для всех детей, вошедших в группу А и группу В, а также в зависимости от отдельных патогенных возбудителей.
Таблица 5. Продолжительность диареи
|
Исследуемая группа |
Продолжительность диареи до госпитализации |
Р |
Продолжительность диареи после госпитализации |
Р |
Общая продолжительность диареи |
Р |
|
А (общая) |
51,0 ± 30,9 |
нд |
71,9±35,8 |
<0,03 |
122,9 ± 33 |
<0,03 |
|
В (общая) |
52,1 ±31 |
нд |
58,3±41,6 |
|
110,4 ± 28,1 |
|
|
А (только рота в и рус, n = 45) |
59,7 ± 33,5 |
нд |
76,6 ± 41,6 |
< 0,008 |
136,3 ±29,0 |
< 0,008 |
|
В (только ротавирус, n = 56) |
58,5 ± 30,3 |
нд |
56,2 ± 16,9 |
|
114,7 ± 16,9 |
|
|
А(инвазивные причины,n = 26) |
48,8±30,5 |
нд |
72,0 ± 32,4 |
нд |
120,8±44,1 |
нд |
|
В(инвазивные причины,n = 27) |
50,7 ± 35,1 |
нд |
73,3 ± 29,3 |
|
124,0 ± 46,4 |
|
|
А (патогенный возбудитель неизвестен, n = 54) |
47,9 ± 29,9 |
нд |
64,2 ± 30,5 |
<0,05 |
112,1±29,5 |
<0,05 |
|
В (патогенный возбудитель неизвестен, n = 45)а |
45,7 ± 29,2 |
нд |
53,2 ± 32,4 |
|
98,9±37,2 |
|
Представленные данные ― часы в среднем ± стандартное отклонение.
НД ― не достоверно.
А ― группа плацебо.
В ― группа, получавшая Lactobacillus GG.
а ― статистическая достоверность данных оставалась неизмененной, если 9 детей с Escherichia coli в качестве единственного бактериального штамма из культуры стула (см. рис. 3) включены в соответствующие группы неизвестного патогенного возбудителя.
Как показывают результаты, прием ORS, содержащего Lactobacillus GG, сопровождался существенным уменьшением диареи в группе в целом (р = 0,03). Этот эффект был в основном результатом высоко достоверного (р = 0,008) снижения диареи, которая отмечалась у пациентов с ротавирусной инфекцией.
У этой подгруппы пациентов, которые были существенно (р = 0,005) более часто дегидратированы, чем пациенты, инфицированные другими патогенными возбудителями, диарея продолжалась примерно на 20 часов меньше в исследуемой группе, чем в контрольной группе. При рассмотрении всех причин стало очевидно, что у детей с инвазивным патоген-индуцированным энтеритом (то есть с диареей, вызванной Salmonella, Shigella, Campylobacter, Yersinia или Entamoeba) не отмечалось повышение эффективности терапии при применении ORS, содержащего Lactobacillus GG. Однако следует отметить, что в группе 99 детей, у которых патогенный возбудитель не был идентифицирован, прием ORS, содержащего Lactobacillus GG, ассоциировался с сокращением продолжительности диареи (р = 0,05).
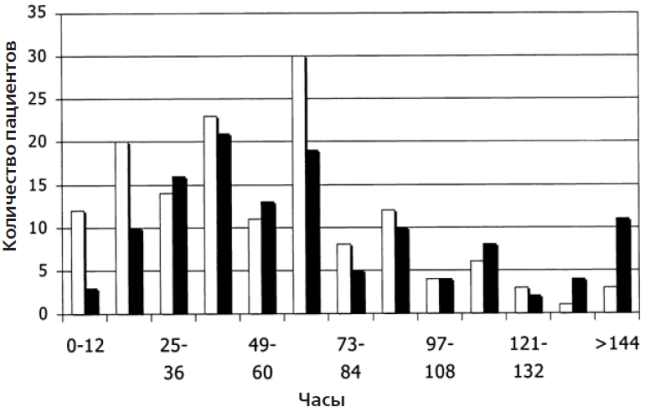
Рис. 2 Продолжительность диареи у пациентов в группе А (плацебо) или группе В (Lactobacillus GG). Пациенты сгруппированы в соответствии с продолжительностью диареи в 12-часовые группы. Средняя продолжительность диареи у пациентов, леченных Lactobacillus GG, составила 51 час по сравнению с 61,5 часов у пациентов контрольной группы (как продемонстрировано на левой части асимметричной кривой). Кроме того, у существенно большего числа пациентов из контрольной группы отмечалась диарея, которая продолжалась более 132 часов. Столбики белого цвета ― Lactobacillus GG. Столбики черного цвета — плацебо.
Чтобы детальнее рассмотреть влияние Lactobacillus GG на продолжительность диареи, пациенты были сгруппированы в зависимости от 12-часовых сегментов, отражающих продолжительность диареи (рис. 2). Очевидно, что данные в группе детей, леченных Lactobacillus GG, были отклонены влево, и также четко прослеживается существенное различие в проценте пациентов с затяжным течением заболевания. Если мы рассмотрим количество детей с продолжительностью диареи более 132 часов после включения в исследование (то есть более 7 дней с начала), очевидно, что только у 4 (2,7%) из 147 пациентов из группы терапии Lactobacillus GG по сравнению с 15 (10,7%) пациентами из группы плацебо отмечается затяжное течение диареи (χ2 = 7,41; р = 0,0064). Относительный риск диареи на протяжении более 7 дней оказался в 3,94 раза (1,34 < относительный риск < 11,58) больше в группе плацебо, чем в группе терапии Lactobacillus GG.
Влияние на водную фазу диареи
На рис. 3 представлено среднее количество испражнений, определенных как водянистые, у 101 ребенка с ротавирусным энтеритом. Как свидетельствуют результаты, применение ORS, содержащего Lactobacillus GG, существенно уменьшает количество водянистого стула у пациентов с энтеритом ротавирусной этиологии.
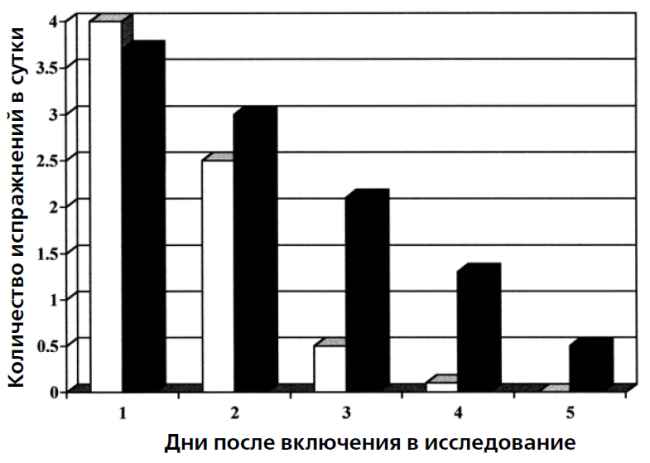
Рис. 3 Среднее количество водянистых испражнений у пациентов, инфицированных ротавирусной инфекцией. В группе из 101 пациента с ротавирусным энтеритом статистически достоверно влияние на среднее количество водянистых испражнений наблюдалось (р < 0,05) с третьего дня.
Столбики белого цвета — Lactobacillus GG. Столбики черного цвета ― плацебо.
Кроме того, согласно данным, представленным на рис. 4, достоверный, но менее выраженный эффект отмечался у пациентов, у которых не был обнаружен патогенный возбудитель.
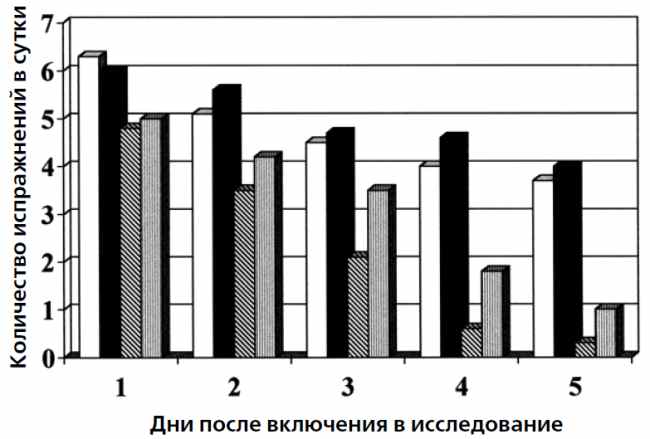
Рис. 4 Среднее количество водянистых испражнений у пациентов с инвазивными возбудителями диареи или с неустановленным патогенным возбудителем.
Несмотря на отсутствие существенных различий в количестве водянистых испражнений у детей с инвазивными возбудителями диареи между группами лечения Lactobacillus GG и плацебо, у пациентов с неустановленным патогенным возбудителем, применение раствора для регидратации для перорального применения, содержащего Lactobacillus GG, привело к достоверному сокращению (р < 0,05) количества водянистого стула на 3-й и 4-й день после включения детей в исследование. Столбики белого цвета ― пациенты с инвазивными возбудителями диареи, получавшие Lactobacillus GG. Столбики черного цвета ― пациенты с инвазивными возбудителями диареи, получавшие плацебо. Заштрихованные столбики ― пациенты с неустановленным патогенным возбудителем, получавшие плацебо.
Увеличение массы тела
У пациентов, получавших ORS, содержащий Lactobacillus GG, отмечали увеличение массы тела в первые 24 часа на 220 ± 120 г (диапазон, 8830 ± 2620 до 9050 ± 2630 г). У пациентов, получавших только ORS, в аналогичный период отмечали увеличение массы тела на 160 ± 200 г (диапазон, 8750 ± 2790 до 8910 ± 2680). Подобные результаты были получены при разделении пациентов в зависимости от причины диареи.
Таким образом, несмотря на то, что у детей, получавших ORS, содержащий Lactobacillus GG, отмечали в среднем лучшее увеличение массы тела, различие между группой плацебо было статистически недостоверным.
Продолжительность госпитализации
На рис. 5 представлены данные о продолжительности госпитализации в часах. У детей, получавших ORS, содержащий Lactobacillus GG, продолжительность госпитализации составила 78,8 ± 22,2 часа, в то время как продолжительность госпитализации у пациентов группы плацебо составила 96,3 ± 21,4 часа (р = 0,04). При рассмотрении групп пациентов в зависимости от причины, очевидно, что наиболее четкое преимущество применения ORS, содержащего Lactobacillus GG, отмечалось у детей, инфицированных ротавирусом.
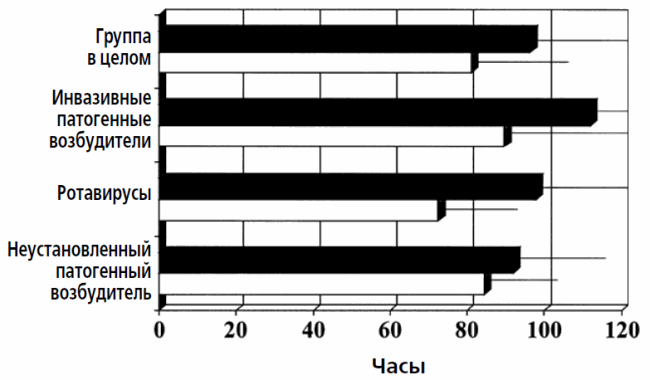
Рис. 5 Продолжительность госпитализации. Наблюдаемые различия были статистически достоверными у всех пациентов независимо от этиологического фактора диареи (общая группа; р = 0,04) и у пациентов, инфицированных ротавирусной инфекцией (р = 0,04). Различия не были статистически достоверными у пациентов с инвазивным патогенным возбудителем (р = 0,1) и у пациентов с неустановленным патогенным возбудителем (р = 0,08).
Столбики белого цвета — Lactobacillus GG. Столбики черного цвета ― плацебо.
Продолжительность госпитализации составила 76,5 ± 15 часов у пациентов, получавших лечение Lactobacillus GG, по сравнению с 97,9 ± 16,5 часов в контрольной группе пациентов (р = 0,04). Несмотря на то, что средняя продолжительность госпитализации также оказалась короче у пациентов, получавших лечение Lactobacillus GG, в группе детей с инвазивным патогенным возбудителем или с неустановленным патогенным возбудителем, эти различия не были статистически достоверными.
Обсуждение
Применение лактобацилл в лечении различных заболеваний не является новой концепцией2,3. Фактически, с целью нейтрализации кишечных инфекций, лактобациллы находятся среди наиболее часто применяемых штаммов бактерий. Среди них, штамм Lactobacillus rhamnosus (ATCC 53103) до настоящего времени является наиболее изученным. Было показано, что этот штамм (со способностью кратковременной колонизации желудочно-кишечного тракта человека, что доказано5), обладает рядом разнообразных, потенциально благоприятных, биологических эффектов. В нескольких клинических исследованиях была продемонстрирована эффективность данного штамма в профилактике6,7 и/или лечении острой диареи у детей (обзор8,9 и у взрослых (обзор)10). [В Украине с целью лечения и профилактики диарей различного генеза широко применяются препараты Бифиформ® Комплекс, Бифиформ® Детский, производства Ферросан, Дания. Кроме Lactobacillus GG (LGG) Бифиформ® Комплекс содержит Lactobacillus acidophilus (LA- 5®), Bifidobacterium lactis (BB-12®) и пробиотик — Инулин 450 мг (из корня Cichorium int.). Бифиформ® Детский дополнительно содержит Bifidobacterium lactis (BB1 2) и витамин B1 и В6. (прим. редакции)].
Однако, несмотря на то, что в настоящее время действие данного пробиотика считается хорошо изученным в лечении острой диареи в результате ротавирусного энтерита, не подтверждена эффективность или неэффективность данного препарата при лечении бактериального энтерита.
Большинство клинических исследований были проведены в популяциях пациентов с подавляющим количеством детей, инфицированных ротавирусной инфекцией11,18. Кроме того, в сообщениях, в которых часть исследуемых детей, вероятно, была инфицирована бактериальными патогенными возбудителями (то есть пациенты с кровянистой диареей и/или дизентерией19,20) или среди которых у подгруппы пациентов были обнаружены бактериальные патогенные возбудители18, эффективность данного пробиотика была сомнительной.
Результаты нашего исследования подтвердили неэффективность Lactobacillus GG в лечении диареи, вызванной подтвержденной бактериальной инфекцией. Действительно, в подгруппе, состоявшей из 53 детей с инвазивным патогенным возбудителем (диарея, вызванная Salmonella, Shigella, Campylobacter, Yersinia или Entamoeba), мы не обнаружили различий в продолжительности диареи между группой, получавшей Lactobacillus GG, и группой плацебо. Однако, в подгруппе пациентов, в стуле которых не был обнаружен патогенный возбудитель (всего у 99 детей), применение ORS, содержащего Lactobacillus GG, привело к существенному уменьшению продолжительности диареи.
В связи с тем, что была продемонстрирована эффективность Lactobacillus GG у пациентов с диареей ротавирусной этиологии, мы можем предположить, что положительный результат терапии данным пробиотиком у пациентов с неустановленным патогенным возбудителем может быть объяснен его эффективностью против патогенов неидентифицированного вирусного происхождения. Таким образом, оказывается, что данный штамм лактобацилл способен предотвратить и нейтрализовать патофизиологические изменения в тонком кишечнике, развившиеся в результате вирусной инфекции, однако менее эффективен в отношении патофизиологических изменений, вызванных инвазивной бактериальной инфекцией в толстом кишечнике.
Мы можем только предположить причину этого явления. Mack и соавторы21 недавно представили подтверждения, что в эпителиальных клетках кишечника in vitro бактерии-пробиотики могут усиливать экспрессию иРНК двух преобладающих муцинов, MUC2 и MUC3. Известно, что такие гликопротеины имеют защитное действие против инфекций кишечника, и этот механизм может иметь значение в пробиотик-индуцированной защите от вирусов. Бактерии, продуцирующие муциназу, с одной стороны, эффективно подавляют этот превентивный механизм.
Общеизвестно положительное влияние Lactobacillus GG на иммунную систему. Это свойство использовано в препарате Мультитабс® Иммуно (Ферросан, Дания) который создан благодаря уникальной технологии: комбинации в одной двухслойной таблетке витаминно-минерального комплекса и Lactobacillus GG.
Согласно дизайну проведенного нами исследования Lactobacillus GG были добавлены в ORS. Данный метод назначения Lactobacillus GG был применен впервые. Мы считаем, что этот инновационный подход может гарантировать раннюю колонизацию данной бактерии. Кроме того, в связи с тем, что прием ORS отчетливо коррелирует со степенью дегидратации, поместив данный пробиотик в ORS, мы получили средство доставки доз данного микроорганизма пропорционально тяжести дегидратации. Большинство пациентов прекратили прием существенного количества ORS на вторые сутки. В среднем, в обеих группах, только около 300 мл ORS в целом было принято после этого времени. Таким образом, прием Lactobacillus GG может быть рассчитан на уровне 3 x 1010 колониеобразующих единиц в течение первых 24 часов (около 1,5 x 1010 колониеобразующих единиц в течение первых 4 часов).
Эффективность данного подхода у инфицированных ротавирусом пациентов была сопоставима с результатами многих исследований 12,13,15,16,17. В частности данные, представленные Rautanen и соавторами17 показали, что раннее назначение Lactobacillus GG является эффективным, и даже прием однократной дозы может быть максимально эффективным и обеспечивать максимальную колонизацию.
Очень интересны результаты существенного снижения количества пациентов с затяжной формой течения диареи. В контрольной группе пациентов более чем у 10% детей отмечалась диарея в течение более 10 дней. В группе пациентов, которые получали Lactobacillus GG, диарея в течение более 10 дней отмечалась у менее 3% детей. Риск затяжного течения диареи на протяжении более недели уменьшился практически в 4 раза в группе лечения Lactobacillus GG. Эти данные демонстрируют способность данного пробиотика предотвращать затяжную форму течения диареи, которая является одним из наиболее неблагоприятных исходов острой диареи у детей. Позволим себе предположить, что улучшенная барьерная функция кишечника, (было продемонстрировано при применении Lactobacillus GGу животных22), а также противовоспалительное действие (доказано у пациентов с пищевой аллергией23), могут быть факторами, способствующими скорейшему излечению острой диареи у детей.
В заключение, следует отметить, что в группе исследованных нами пациентов, продолжительность госпитализации была существенно и достоверно сокращена при применении ORS, содержащего Lactobacillus GG. Это позволяет существенно снизить затраты, связанные с госпитализацией, а также уменьшить риск госпитального распространения ротавирусной инфекции.
Таким образом, на основе представленных нами данных можно сделать следующие выводы: В заключение, мы считаем, что в современный метод лечения диареи может быть включено применение Lactobacillus GG с раствором ORS.
De Marco G, Guarino A.Passariello A, Manguso F.
Department of Paediatrics, University of Naples Federico II, Naples, Italy.
Литература
- Booth I., Cunha Ferreina R., DesjeuxJ. Recommendations for composition of oral rehydration solutions for the ildren of Europe. J Pediatr Gastroenterol Nutr 2002; 14:113-5.
- Saavedra J.M. Microbes to fight microbes: A not so novel approach to controlling diarrheal disease (editorial and mment). J Pediatr Gastroenterol Nutr 2005; 21:125-9
- Lewis S.J., Freedman A.R. Review article: The use of biotherapeutic agents in the prevention and treatment of gastrointestinal disease. Aliment Pharmacol Ther 2001; 12:807-22.
- Bengmark S. Ecological control of the gastrointestinal tract: The role of probiotic flora. Gut 1998:2-7.
- Goldin B.R., Gorbach S.L., Saxelin M., Barakat S., Gualtieri L., Salminen S. Survival of Lactobacillus species (strain GG) in human gastrointestinal tract. Dig Dis Sci 1999; 37:121-8
- DuPont HL. Lactobacillus GG in prevention of traveler's diarrhea: An encouraging first step.J Travel Med 1997; 1-2. 4
- Hilton E, Kolakowoski P, Singer C, Smith M. Efficacy of Lactobacillus GG as a diarrheal preventive in travelers. J Travel Med 1999; 4:41-3.
- Guandalini S. Probiotics in the treatment of diarrheal diseases in children. Gastroenterol Int 1998; 11:87-90.
- Vanderhoof JA, Young RJ. Use of probiotics in childhood gastrointestinal disorders. J Pediatr Gastroenterol Nutr 1998; 27:323-32.
- Elmer GW, Surawicz CM, McFarland LV. Biotherapeutic agents: A neglected modality for the treatment and prevention of selected intestinal and vaginal infections (review). JAMA 2000; 275:870-6.
- Guarino A, Canani RB, Spagnuolo MI, Albano F, Di Benedetto L. Oral bacterial therapy reduces the duration of symptoms and of viral excretion in children with mild diarrhea. J Pediatr Gastroenterol Nutr 2004; 25:516-9.
- Isolauri E, Juntunen M, Rautanen T, Sillanaukee P, Koivula T. A human Lactobacillus strain (Lactobacillus casei strain GG) promotes recovery from acute diarrhea in children. Pediatrics 1999; 88:90-7.
- Isolauri E, Kaila M, Mykkanen H, Ling WH, Salminen S. Oral bacteriotherapy for viral gastroenteritis. Dig Dis Sci 1999; 39:2595-600.
- Kaila M, Isolauri E, Soppi E, Virtanen E, Laine S, Arvilommi H. Enhancement of the circulating antibody secreting cell response in human diarrhea by a human Lactobacillus strai
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


