
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 11.10.2024 Штучний інтелект у фармації: перспективи, переваги та потенційні ризики
- Новини 27.08.2024 Вакансії медсестри у Вінниці: особливості та вимоги до кандидатів
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
Клинические примеры эффективности ибандроновой кислоты (препарат Бонвива) при постменопаузальном остеопорозе: от доказательной медицины к постели больного

В статье даны описание трех клинических случаев применения ибандроновой кислоты для профилактики и лечения постменопаузального остеопороза с хорошим клиническим эффектом. Представлены данные изменений минеральной плотности костной ткани при наблюдении от 12 до 27 месяцев, а также риск возникновения переломов костей по системе FRAX. Клинический опыт применения препарата Бонвива в комплексной терапии постменопаузального остеопороза приводит не только прогрессивное увеличение минеральной плотности кости в поясничном отделе позвоночника и проксимальном отделе бедренной кости, но и снижения риска переломов позвонков.
Остеопороз (ОП) как системное метаболическое заболевание скелета характеризуется снижением минеральной плотности кости с нарушением ее архитектоники, повышением риска переломов при неадекватной травме/физической нагрузке и стоит в одном ряду с сердечно-сосудистой, дыхательной, онкологической патологией по причине смертности и инвалидности [5].
Постменопаузальный остеопороз (ПМО) - наиболее распространенная форма заболевания, при котором прогрессирующее снижение прочности кости ассоциировано с наступлением менопаузы (естественной или хирургической) [8]. Согласно международной классификации ПМО относится к первичному ОП I типа и характеризуется высоким костным обменом с интенсивными процессами костной резорбции при нормальном или повышенном костеобразовании. Отличительная особенность ПМО - преимущественное поражение трабекулярной костной ткани. В связи с этим наиболее уязвимыми областями являются позвоночник, состоящий на 95% из трабекулярной кости, и дис-тальный отдел лучевой кости [4]. По мере прогресс и рования остеопороза помимо нарушений в трабекулярных костях происходит ускорение костной резорбции и нарушение внутренней архитектоники кортикальных костей. При этом сначала преобладает эндокортикальная резорбция, вызывающая увеличение объема костномозгового пространства и уменьшение кортикальной толщины, позднее увеличивается кортикальная порозность. Эти изменения постепенно приводяткослаблению кортикальных костей и возрастанию количества переломов в этих костях.
Менопауза - сложный физиологический период в жизни женщины, часто сопровождающийся развитием широкого спектра вазомоторно-вегетативных. урогенитальных и метаболических нарушений. ОП относится к поздним постменопаузальным осложнениям, основной причиной которых является недостаточный синтез эстрогенов [8]. Как известно, эстрогены являются мощными системными факторами, подавляющими костную резорбцию. Дефицит эстрогенов приводит к снижению ингибирующего влияния на остеокласты и снижению активности остеобластов, повышению чувствительности костных клеток к действию паратире-оидного гормона, прорезорбтивных цитокинов (интерлейкины-1. 6.11. фактор некроза опухоли а и др.). что способствует ускорению и разобщению процессов костного ремоделирования [7.8]. В последние годы значительно расширились знания относительно патогенетических механизмов потери костной ткани на фоне эстрогендефицита.Наскоростьпрогрессированияостеопороза при недостаточности эстрогенов могут оказывать влияние наследственные дефекты механизмов, регулирующих синтез белкового костного матрикса и его минерализацию. Предполагается, что у пациенток с сочетанием аллелей ВВ в гене VDR вероятность индукции остеопороза в постменопаузальный период оказывается более высокой, чем при иных аллельных сочетаниях [7].
ПМО - междисциплинарная проблема, с которой сталкиваются врачи разных специальностей, прежде всего - гинекологи, ревматологи, эндокринологи и травматологи [4].
Структурно-функциональное состояние костной ткани в постменопаузальный период определяется уровнем пиковой костной массы, достигнутым в молодые годы, а также воздействием внешних и внутренних факторов, способствующих чрезмерной ее потере. Традиционно такие факторы разделяются на модифицируемые и немодифицируемые. среди которых наибольшее значение имеют семейный анамнез переломов, ранняя менопауза, гипогонадизм. хронические воспалительные заболевания, курение, злоупотребление алкоголем, дефицит витамина D. Определенное влияние на состояние костной ткани оказывают факторы, связанные с репродуктивной функцией женщин: первичное бесплодие, патология становления оварио-менструальной функции в анамнезе (позднее менархе - старше 15 лет), значительная продолжительность периода лактации и др. Однако их значение в развитии ПМО остается до конца не выясненным.
В настоящее время существуют эффективные программы профилактики и лечения остеопороза. включающие сочетание нефармакологических методов с современными противоостео-поротическими препаратами [3].
Основными задачами при лечении ПМО являются нормализация процессов костного ремоделирования. замедление или прекращение потери минеральной плотности костной ткани (МКПТ). предотвращение возникновения новых переломов костей, а также улучшение качества жизни пациентки (уменьшение болевого синдрома, расширение двигательной активности).
В соответствии с современными взглядами основным критерием эффективности лечебного препарата при терапии остеопороза является снижение частоты переломов при длительном (3-5-летнем) использовании, о чем судят на основе данных продолжительных рандомизированных контролируемых испытаний [7]. На основании результатов таких исследований к препаратам первой линии терапии ПМО относятся, прежде всего, бисфос-фонаты (БФ).
Основным фармакологическим эффектом БФ является снижение костного ремоделирования с более выраженным угнетением костной резорбции, чем костеобразования. а также снижение частоты активации ремоделирования. Препараты снижают или предупреждают отрицательное влияние на кость практически всех известных стимуляторов резорбции, втом числе паратгормона [1. 16]. Клеточный механизм действия БФ заключается в прямом ингибировании активности остеокластов, их подвижности, а также блокировании связывания остеокластов с костной тканью [1.16]. Присутствие атома азота в боковой цепи объясняет особый механизм действия азотсодержащих БФ. связанный со способностью ингибировать процесс модификации белков в остеокластах, что ведет к апоптозу зрелых клеток и подтверждается появлением специфических изменений в клетке и структуре ядра [1. 5]. Остеобласты также являются потенциальными мишенями для БФ. поскольку влияют на функциональную активность остеокластов. Данные in vitro свидетельствуют, что под влиянием БФ остеобласты снижают секрецию остеокласт-стимулирующего фактора [9].
Терапия остеопороза. являющегося тяжелым хроническим заболеванием, должна проводиться в течение длительного времени. В связи с этим нередко возникает проблема приверженности больных лечению, тесным образом связанная с его эффективностью [3]. Широкие клинические перспективы имеет БФ нового поколения - препарат Бонвива (ибандроновая кислота), основное преимущество которого заключается не только в большей антирезорбтивной активности, но и в возможности применения 1 таблетки один раз в месяц [9.11.15]. Кроме того, предложенный препарат для лечения должен иметь достаточную доказательную базу относительно реального снижения риска вертебральных и невертебральних переломов костей [6].
Клиническая эффективность препарата Бонвива была подтверждена данными ряда многоцентровых исследований по изучению влияния различных доз и схем приема ибандроната на минеральную плотность и качество кости, риск развития новых переломов и переносимость препарата, в которых участвовали более 13 тысяч пациентов из разных стран [2.9.12.14]. Так. результаты многоцентрового рандомизированного двойного слепого исследования MOBILE (Monthly Oral Ibandronate in Ladies) показали, что при частоте введения ибандроната 1 раз в месяцу женщин с постменопаузальным остеопорозом минерализация костной ткани поясничного отдела позвоночника повышается в той же степени, что и при ежедневном приеме 2.5 мг [12.13].
В исследовании BONE (Oral iBandronate Osteoporosis Vertebral Fracture Trial in North America and Europe) была подтверждена эффективность ибандроновой кислоты по предупреждению позвоночных и внепозвоночных переломов. Было установлено, что Бонвива по сравнению с другими БФ максимально снижает риск переломов тел позвонков - на 62%. Важно подчеркнуть, что ретроспективный анализ, включавший 375 пациенток с высоким риском внепозвоночных переломов (исходный Т-показатель МПКТ шейки бедра <-3.0). показал, что прием препарата достоверно снижает риск внепозвоночных переломов на 69% [10].
Однако эффективность терапии любого хронического заболевания тесно связана с приверженностью пациента лечению. Результаты многоцентрового исследования BALTO. посвященного сравнительной оценке приверженности пациентов лечению, показали, что 66.1% женщин с постменопаузальным остеопорозом предпочитаютежемесячный прием 150 мгпрепарата Бонвива еженедельному приему 70 мг алендроновой кислоты [11].
Клинический опыт применения препарата Бонвива в комплексной терапии ПМО приводит не только к прогрессивному увеличению МПКТ в поясничном отделе позвоночника и проксимальном отделе бедренной кости, но и снижению риска переломов позвонков. Ниже представлены наиболее яркие клинические примеры использования препарата Бонвива в лечении и профилактике ПМО.
Случай 1
Пациентка Д.. 50 лет. при очередном визите к гинекологу отметила появление боли в костях, суставах, поясничной области, не связанной с физической нагрузкой, а также ограничение подвижности в утреннее время, что продолжается втечение 20-30 мин. Из анамнеза известно, что менопауза наступила в 47 лет. Вегетативные расстройства выражены незначительно. Заместительную гормональную терапию не получала.
При объективном обследовании: рост 170 см. масса тела 67 кг При расчете риска возникновения переломов по системе FRAX выявлены следующие факторы риска: курение, наличие перелома лучевой кости втипичном месте (3 года назад, падение с высоты роста во время гололеда на улице), наличие перелома бедренной кости у матери. Расчет риска переломов выявил следующие показатели: риск возникновения остеопоротических переломов в течение следующих 10лет-10%. переломов шейки бедренной кости -1.4%. Для определения МПКТ пациентка была направлена на костную денситометрию. Полученные результаты выявили значительное снижение МПКТ в поясничной области -0.924 г/см2, Т-индекс -USD. Однако более значительные изменения были выявлены в шейке бедренной кости: МПК -0.607 г/см2. Т-индекс -2.2SD. Полученные данные явились основанием для пересчета риска переломов по системе FRAX. С учетом данных МПКТ шейки бедренной кости установлено, что риск возникновения остеопоротических переломов составил 15%. переломов шейки бедренной кости - 3.8%. Таким образом, низкие показатели минеральной плотности шейки бедренной кости значительно увеличили риск возникновения переломов, что стало основанием для назначения противоостеопоротической терапии. Пациентке был назначен препарат Бонвива в дозе 150 мг1 раз в месяц утром натощак. Была проведена беседа относительно необходимости тщательного соблюдения правил приема препарата. Дополнительно были назначены препараты кальция в дозе 1200 мг в сутки (в перерасчете на элементарный кальций) и даны рекомендации по диетическому питанию с акцентом на кальцийсодержащие продукты.
Через 10 месяцев терапии отмечен значительный достоверный прирост костной массы, что объективно отобразили показатели МПКТ поясничной области и шейки бедренной кости (рис. 1. 2). Так. прирост костной массы в поясничной отделе позвоночника составил 6.9%. МПКТ возросла с 0.924 до 0.988 г/см2, Т-индекс также уменьшился до -0.5 SD. В шейке бедренной кости изменения МПКТ были такими же динамичными: минеральная плотность возросла на 2.8% - с 0.607 до 0.639 г/см2. Однако самое главное, что данная терапия способствовала снижению риска переломов по системе FRAX. Через 10 месяцев риск основных остеопоротичес-ких переломов снизился до 13%. а риск переломов шейки бедренной кости -до 2.5%.
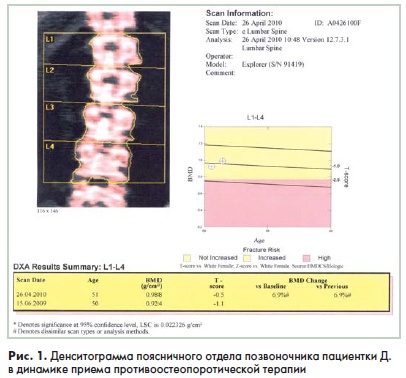
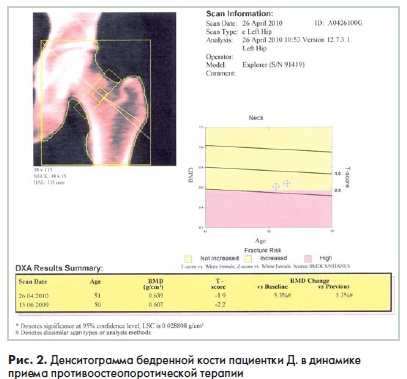
Полученные данные свидетельствуют об эффективности препарата Бонвива в профилактике ПМО и снижении риска остеопоротических переломов.
Случай 2
Пациентка Л.. 48 лет. Хирургическая менопауза с 46 лет. Жалуется на сильную боль в позвоночнике, особенно в грудном и поясничном отделе, которая возникла почти сразу после оперативного вмешательства. При оценке факторов риска установлено: пациентка не курит, не принимает глюкокортикоиды. не имеет заболеваний, которые способствовали развитию вторичного остеопороза. семейный анамнез не отягощен, также в анамнезе у пациентки не было переломов костей. В связи с длительным болевым синдромом, связанным с наступлением менопаузы, пациентке было проведено определение МПКТ методом двухфотонной рентгеновской денситометрии (DXA). что считается «золотым» стандартом в диагностике остеопороза.
При проведении денситометрии по результатам анализа показателей в поясничном отделе позвоночника у пациентки был установлен остеопороз. Так. МПК составляла 0774 г/см2. Т-индекс -2.5SD. В области шейки бедренной кости зафиксированы более высокие результаты: Т-индекс равнялся -0.7 GD. При оценке риска переломов по системе FRAX риск возникновения остеопороти-ческих переломов в течение 10 лет составлял 2.5%. а риск перелома шейки бедренной кости - 0.1%.
Учитывая низкие показатели МПКТ поясничного отдела позвоночника, которые соответствовали диагнозу остеопороза. пациентке был выставлен диагноз ПМО и назначено лечение с применением препарата Бонвива в дозе 150 мг в месяц и препараты кальция -1200 мг в сутки.
Через 7 месяцев было проведено повторное исследование МПК в динамике. К сожалению, значительных изменений в поясничном отделе позвоночника не было зафиксировано (рис. 3): изменение МПК составило 0.4%. Наоборот, в области шейки бедренной кости в течение 7 месяцев терапии препаратом отмечен значительный прирост минеральной плотности - +5.5%. Показатель Т-индекса изменился с -0,7SD до -0.XD (рис. 4).
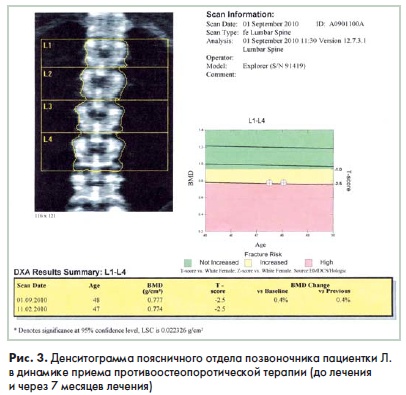
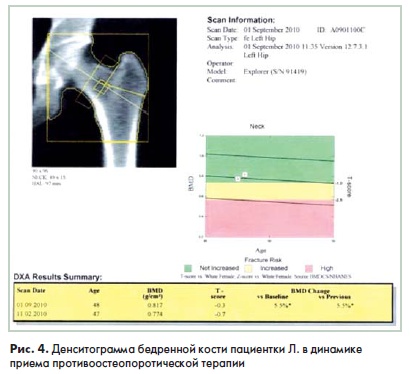
Учитывая наличие прироста костной массы в шейке бедренной кости, пациенте было рекомендовано продолжить прием препаратов. Повторное исследование через 17 месяцев лечения выявило значительную позитивную динамику в поясничном отделе позвоночника. Так. прирост МПК составил 7.9%. а Т-индекс снизился с -2,5SD до -1.9SD (рис. 5).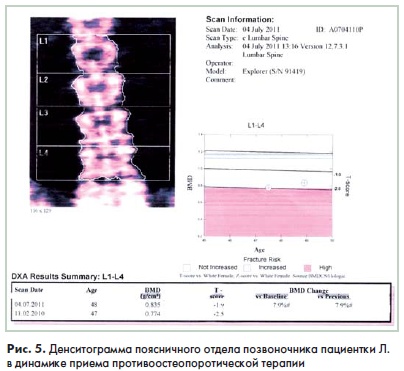
Таким образом, применение препарата Бонвива продемонстрировало высокую эффективность в лечении ПМО. Отсутствие положительного результата терапии в поясничном отделе через 7 месяцев лечения указывает на необходимость установления реальных временных рамок для оценки эффективности лечения БФ.
Одновременно следует отметить, что значение пиковой костной массы и потери костной массы в репродуктивный период являются важными предикторами развития ПМО. В представленном клиническом случае имеет место нетипичное и быстрое развитие ПМО через 2 года наступления менопаузы. Это свидетельствует, что пациента подошла к периоду менопаузы с низкими показателями костной массы, а дефицит эстрогенов только ускорил костные потери и привел к возникновению остеопороза. Таким образом, оценку факторов риска развития остеопороза и оценку состояния костной ткани необходимо проводить не только с наступлением менопаузы, но и в репродуктивный период.
Случай 3
Пациентка М.. 51 год. Менопауза естественная с 45 лет. Жалобы на снижение роста на 3 см за последние 3-4 года, постоянная боль в поясничном отделе позвоночника и появление его тутоподвижности. боль в периферических суставах без признаков их воспаления. Других факторов риска остеопороза у пациентки не выявлено. Рост 160 см. масса тела 52 кг. При тестировании по системе FRAX риск возникновения остеопоротичес-ких переломов составляет 6.4% в течение последующих 10 лет. риск развития переломов шейки бедренной кости - 1.1%. При проведении денситометри чес кого исследования установлены следующие результаты: общая МПКТв поясничном отделе составляет 0.768 г/см2. Т-индекс -2.5SD. В разных позвонках Т-индекс колебался от -2.XD до -2.85D (рис. 6). В шейке бедренной кости Т-индекс равнялся: справа -1.55D. слева -1.6SD.
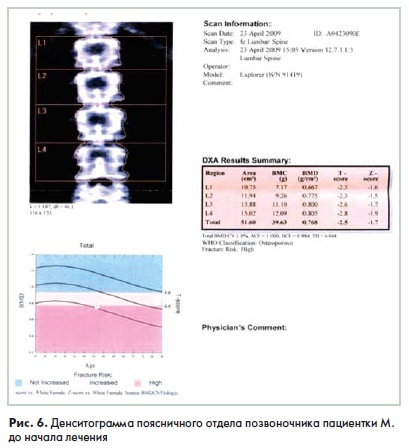
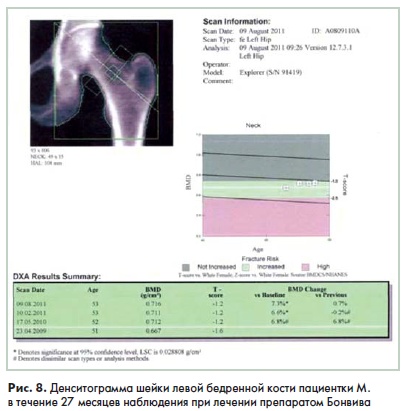
Пациентке назначена терапия препаратом Бонвива в дозе 150 мг 1 раз в месяц с препаратами кальция (1200 мг в суши) и витамин D (800 ME в сутки). Оценка эффективности терапии проведена через 12 месяцев лечения. В поясничном отделе позвоночника прирост костной массы составил +5.6%; в области шейки бедренной кости +6.8%. Т-индекс в поясничном отделе составил -2.1 SD. в области шейки левой бедренной кости -1.2SD. Через 27 месяцев терапии прирост МПК в поясничном отделе составил +6.9% (рис. 7). в области шейки левой бедренной кости +7,3% (рис. 8). Риск возникновения переломов снизился до 5,5%. риск переломов шейки бедренной кости -до 0.6%.
Данный случай демонстрирует стойкий положительный эффект применения препарата Бонвива в течение 27 месяцев непрерывной терапии, что привело к повышению МПКТ и снижению риска переломов. Необходимо отметить, чтоза весьпериод наблюдение у пациентки не отмечено появление новых переломов.
Таким образом, применение ибандроновой кислоты (препарат Бонвива) приводит к снижению риска остеопоротических переломов костей, стойкому повышению МПКТ поясничного отдела позвоночника и бедренной кости и может с успехом применяться в профилактике и лечении пациенток с ПМО.

Литература
- Головач І.Ю. Еволюція бісфосфонатів: сходження на вершину // Мистецтво лікування. – 2009. – №9–10. – С. 68–74.
- Головач І.Ю. Лікування остеопорозу у контексті профілактики переломів: впровадження даних доказової медицини в клінічну практику. У ракурсі – ібандронова кислота // Ліки України. – 2011. – №1 (147). – С. 64–69.
- Мкртумян А.М., Бирюкова Е.В. Новые перспективы успешного лечения постме- нопаузального остеопороза // Эффективная фармакотерапия в эндокриноло- гии. – 2007. – №4. – С. 2–7.
- Мурадянц А.А., Шостак Н.А., Клименко А.А. Постменопаузальный остеопороз в практике клинициста: диагностика и лечение // Клиницист. – 2007. – №3. – С. 30–37.
- Поворознюк В.В. Бисфосфонаты: роль ибандроновой кислоты в лечении пост- менопаузального остеопороза // Здоров'я України. – 2007. – №5. – С. 57–58.
- Торопцова Н.В., Никитинская О.А., Беневоленская Л.И. Новый препарат бонви- ва для лечения постменопаузального остеопороза // Остеопороз и остеопа- тии. – 2006. – №2. – С. 42–45.
- Юренева С.В. Лечение и профилактика постменопаузального остеопороза // Consilium Medicum. – 2004. – Т. 6, №9. – С. 702–707.
- Яшина Е.Г. Актуальные вопросы климактерия, современное состояние пробле- мы // Новости медицины и фармации. – 2004. – №8. – С. 20–21.
- Barrett J., Worth E., Bauss F., Epstein S. Ibandronate: a clinical pharmacological and pharmacokinetic update // J. Clin. Pharmacol. – 2004. – Vol. 44. – P. 951–965.
- Chesnut III C.H., Skag A., Christiansen C. et al. Effects of oral ibandronate administered daily or intermittently on fracture risk in postmenopausal osteoporosis // J. Bone Miner. Res. – 2004. – Vol. 19. – P. 1241–1249.
- Emkey R., Koltun W., Beusterien K. et al. Patient preference for once-monthly ibandronate versus once-weekly alendronate in a randomized, open-label, cross-over trial: the Boniva Alendronate Trial in Osteoporosis (BALTO) // Curr. Med. Res. Opin. – 2005. – Vol. 21 (12). – P. 1895–1903.
- Miller P.D., Epstein S., Sedarati F., Reginster J.Y. Once-monthly oral ibandronate compared with weekly oral alendronate in postmenopausal osteoporosis: results from the head-to-head MOTION study // Curr. Med. Res. Opin. – 2008. – Vol. 24 (1). – P. 207–213.
- Miller P.D., McClung M., Macovei I. et al. Monthly oral ibandronate therapy in postmenopausal osteoporosis: 1-year results from the MOBILE study // J. Bone Miner. Res. – 2005. – Vol. 20. – P. 1315–1322.
- Papapoulos S.E. Ibandronate: a potent new bisphosphonate in the management of postmenopausal osteoporosis // IJCP. – 2003. – Vol. 57. – P. 417–422.
- Reginster J.-Y., Adami S., Lakatos P. et al. Efficacy and tolerability of oncemonthly oral ibandronate in postmenopausal osteoporosis // Ann. Rheum. Dis. – 2006. – Vol. 65. – P. 654–661.
- Rogers M.J. New insights into molecular mechanisms of action of bisphosphonates // Curr. Pham Des. – 2003. – Vol. 9. – P. 2643–2658.
- Russell R.G., Watts N.B., Ebetino F.H., Rogers M.J. Mechanisms of action of bisphosphonates: similarities and differences and their potential influence on clinical efficacy // Osteoporos Int. – 2008. – Vol. 19 (6). – P. 733–759.
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


