
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
- Новини 26.10.2021 Аппаратура для УЗИ: применение, принципы работы, разновидности
- Новини 23.10.2021 Интимная пластика после родов: когда необходима операция
Прогестагенные эффекты дидрогестерона
Молекулярная структура дидрогестерона сходна по строению с эндогенным прогестероном и имеет уникальные особенности, которые повышают его пероральную доступность. Гормональный профиль и прогестагенная активность были определены in vitro, in vivo и у людей в комбинации с эстрогенами и без них. В составе ЗГТ циклический прием 10 мг дидрогестерона обеспечивал адекватную защиту эндометрия от гиперплазии у женщин в постменопаузе, получавших 2 мг эстрадиола. Аналогичный эффект наблюдался при использовании 5 мг дидрогестерона в непрерывном режиме в комбинации с 1 мг эстрадиола. Также был отмечен хороший эффект дидрогестерона у женщин с аменореей/олигоменореей, дисфункциональными маточными кровотечениями и нерегулярным циклом. В заключение необходимо отметить, что имея профиль, аналогичный прогестерону, но с лучшей пероральной доступностью, дидрогестерон успешно используется в лечении нарушений, связанных с абсолютным или относительным дефицитом прогестерона.
Прогестагенные эффекты, общие для всех гестагенов, хорошо известны для прогестерона, основного эндогенного прогестагенного стероидного гормона. Прогестерон синтезируется главным образом желтым телом яичника и плацентой. Физиологическое увеличение секреции прогестерона происходит в лютеиновую фазу менструального цикла и во время беременности. Снижение секреции прогестерона у женщин в возрасте, приближающемся к менопаузальному, является первым признаком приближающегося нарушения овуляции. Незначительное количество прогестерона также продуцируется корой надпочечников [1]. Синтез прогестерона регулируется рядом факторов, включая р-адренергические сигналы, фолликулостимулирующий гормон (ФСГ), лютеинизирующий гормон (ЛГ), хорионический гонадотропин человека (ХГЧ), гонадотропин-релизинг-гормон (ГнРГ), дегидроэпиандростерон (ДГЭА) и эстрогены [2-7].
Прогестерон воздействует на матку, молочные железы и мозг. Он необходим для имплантации эмбриона, сохранения беременности и развития тканей молочных желез. Он может взаимодействовать с эстрогенами, как синергист или антагонист; однако соотношение гормонов значительно варьирует в различных органах-мишенях. Таким образом, в зависимости от клетки или ткани, прогестерон может стимулировать пролиферацию клеток (например, в молочных железах), или ингибировать пролиферацию и индуцировать дифференцировку (например, в эндометрии матки) [8].
У женщин во время менструльного цикла прогестерон необходим для секреторной трансформации эндометрия и возникновения менструального кровотечения, которое является кровотечением отмены прогестерона.
Во время беременности прогестерон защищает плод, который является аллогенным (чужеродным) для организма матери, от иммунологического отторжения, подавляет сократительную активность миометрия путем снижения чувствительности миометрия к стимулированию окситоцином, а также готовит эндометрий к имплантации [8-11].
Прогестерон выявляет свою прогестагенную активность не только путем связывания с двумя изоформами (А и В) ядерного рецептора прогестерона (ПР), но и путем взаимодействия с мембранными прогестиновыми рецепторами (mPRu, mPRp и mPR-v), которые могут быть ответственными за опосредование быстрых негеномных действий прогестагенов в разных тканях-мишенях, а также с другими рецепторами стероидных гормонов, например, рецепторами глюкокортикоидов и минералокортикоидов (табл. 1).
Учитывая основную функцию прогестерона, его относительная или абсолютная недостаточность (недостаточность лютеиновой фазы) приводит к нарушению репродуктивной функции или менструального цикла. Дефицит прогестерона по отношению к эстрогенам может привести к гиперплазии эндометрия и повышению риска рака эндометрия, например, у женщин в период постменопаузы, которые принимают исключительно эстрогены для лечения климактерических симптомов или для профилактики постклимактерического остеопороза.
Относительный или абсолютный дефицит прогестерона можно устранить с помощью экзогенных прогестагенов. В настоящее время они используются для лечения различных гинекологических патологий, например, бесплодия, угрозы выкидыша/привычного невынашивания, аменореи, дисфункциональных маточных кровотечений, дисменореи, предменструального синдрома, эндометриоза и гиперплазии эндометрия (табл. 2). При заместительной гормональной терапии (ЗГТ) добавляют прогестагены для противодействия пролиферативным эффектам эстрогенов на эндометрий, поскольку монотерапия эстрогенами связана с повышенным риском гиперплазии эндометрия [12].
Различия между прогестагенами
Прогестагены отличаются активностью и гормональным профилем.
В зависимости от способа введения прогестагены проявляют различные биологические эффекты, что вызвано различиями в метаболизме и способности связываться с ПР и другими стероидными рецепторами. Также существуют различия в связывании с белками сыворотки (например, секс-стероидсвязывающий глобулин или кортикостероидсвязы-вающий глобулин) [1].
Прогестагенная активность значительно отличается и очень часто выражается в дозе, необходимой для секреторной трансформации эстрогенстимулированного эндометрия человека, такая доза называется дозой трансформации.
Уникальные свойства прогестагена дидрогестерона Дидрогестерон (6-дегидро-ретропрогестерон) является гормонально-активным неадрогенным стероидом, который был синтезирован в 50-х годах ученым Риринком (Reerink) и др. [15]. Он уникален, потому что является единственным серийно выпускаемым ретростероидом. Его молекулярная структура сходна по строению с природным прогестероном (рис. 1) и имеет уникальные особенности, которые повышают его пероральную доступность. В молекуле дидрогестерона перевернута конфигурация на С9 и С10, т.е. расположена наоборот по сравнению с прогестероном. Кроме того, существует дополнительная двойная связь С6-С7 [16], которая сжимает молекулу в структуру, максимально подходящую для связывания с ПР, повышает его селективность, тогда как прогестерон, структура которого обеспечивает более легкое связывание с различными рецепторами, менее избирателен. Благодаря высокой биодоступности и прогестагенной активности основного метаболита дидрогестерона, для обеспечения одного и того же эффекта необходима его доза в 10-20 раз меньше, чем доза микронизированного прогестерона [1].
Таблица 1
Связывание прогестагенов со стероидными рецепторами [1]
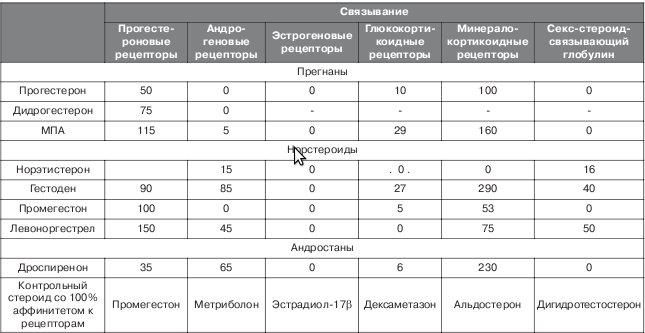
Таблица 2
Фармакологические свойства прогестагенов [1]
| Дидрогестерон | Тестостерон и производные 19-нортестостерона | Производные прогестерона | Прогестерон | ||
| Блокирование овуляции | Люди | –а | + | + | + |
| Эстрогенные | Люди/животные | – | + | – | ± |
| Андрогенные | Животные | – | + | + | – |
| Маскулинизация плода | Животные/люди | – | + | + | – |
| Расслабление миометрия | Животные/люди | + | – | ± | + |
| Адренальная атрофия | Животные | – | + | + | – |
| Термогенность | Люди | – | + | + | + |
| Коагуляция крови | Люди | – | + | + | – |
| Липиды крови | Люди | – | + | – | – |
«+» – наличие эффекта, «—» – отсутствие эффекта и «±» – двойственный а – в нормальных дозах.
Дидрогестерон оыстро аосороируется и полностью мета-болизируется [17-19]. После перорального приема максимальные плазменные концентрации дидрогестерона и его основного метаболита 20а-дигиродидрогестерона (ДГД) достигаются через 0,5-2,5 часа, причем плазменные концентрации ДГД значительно выше концентраций исходного лекарственного вещества. Средний период полувыведения дидрогестерона и ДГД составляет 5-7 и 14-17 ч соответственно. Каких-либо клинически значимых фармакокинетических взаимодействий дидрогестерона не выявлено. Доклинические исследования не выявили мутагенного, тератогенного или канцерогенного потенциала дидрогестерона, а результаты фармаконадзора не содержат данных о врожденных пороках развития, связанных с приемом дидрогестерона во время беременности [20].
Дидрогестерон отличается от других прогестагенов способностью связываться исключительно с ПР (табл. 1) [16]. Он не имеет эстрогенной, андрогенной или адренокор-тикоидной активности, не может метаболизироваться в эстрогены, кроме того, обладает антиэстрогенной активностью только в некоторых органах-мишенях (например, эндометрий) (табл. 2). Несмотря на то что он является сильнодействующим прогестагеном с эндометриальным ответом, практически аналогичным ответу эндогенного прогестерона, дидрогестерон не влияет на систему гипоталамус - гипофиз - яичники и не ингибирует овуляцию, что часто наблюдается под действием других прогестагенов [21-23]. Дидрогестерон не изменяет параметры коагуляции, липидов крови или глюкозы/инсулина, не является гепатотоксичным, не обладает термогенным эффектом, не оказывает значительного влияния на водный и электролитный баланс |24]. В отличие от прогестерона, дидрогестерон не выводится в качестве пре-гнандиола с мочой. Следовательно, измерение прегнандиола в моче в качестве показателя эндогенной секреции прогестерона остается возможным у женщин, принимающих дидрогестерон [25].
Влияние на образование прогестерона в желтом теле на ранних сроках беременности
Saure и др. [38] исследовали степень влияния различных прогестагенов на ингибирование образования прогестерона из прегненолона в желтом теле человека на ранних сроках беременности. Ткани, полученные из 26 желтых тел, взятых на 7-14-й неделе беременности (полученные при лапарото-мии в связи с медицинскими абортами) инкубировались с различными концентрациями прегненолона. Дидрогестерон и производные 19-нортестостерона линестренол и норэтино-дрел оказывали меньшее ингибирующее действие по сравнению с прогестероном, тогда как степень ингибирования МПА и норгестрела была сопоставима с показателями прогестерона.
Влияние на клетки эндотелия
Simoncini и др. [48] исследовали воздействие нескольких прогестагенов на индукцию эндотелиальной синтазы оксида азота (eNOS) в клетках эндотелия человека из пупочной вены. Дидрогестерон в качестве монотерапии или в комбинации с эстрогеном имели нейтральное действие на синтез и активность N0, а также экспрессию eNOS. Стабильный метаболит дидрогестерона — ДГД имел аналогичное эндогенному прогестерону действие, усиливая экспрессию и синтез eNOS.

Рис. 1. Молекулярное строение (а) прогестерона и (б) дидрогестерона
Воздействие на иммуномодуляцию
Снижение уровня эндогенного прогестерона во время беременности ведет к снижению синтеза прогестеронинду-цированного блокирующего фактора (ПИБФ) и значительно повышает частоту выкидышей. В случае применения дидрогестерона беременность сохранялась, а уровни ПИБФ повышались. Дидрогестерон также резко повышал процентное содержание интерлейкина (ИЛ)-4 (положительные децидуальные иммуноциты), а его защитный эффект, как было показано, был опосредован CD8+ клетками. Аналогичный иммуномодулирующий ответ дидрогестерона наблюдался в ex vivo исследовании с использованием моно-нуклеаров периферической крови женщин с привычным невынашиванием [53]. Выработка ПИБФ повышалась, а баланс Thl/Th2 смещался путем ингибирования продукции цитокинов ТЫ и активирования цитокинов Th2 IL-4 и IL-6, что помогало сохранить беременность [51-53].
Влияние на гипоталамо-гипофизарно-яичниковую ось
Блокирование гипоталамо-гипофизарно-яичниковой оси с последующим подавлением овуляции является основой механизма действия гормональных контрацептивов. Прогестагенные соединения в качестве монотерапии в высоких дозах препятствуют всплеску ЛГ в середине цикла, а впоследствии овуляции, тогда как при использовании низких доз считается, что их действие, главным образом, периферическое [38].
Swyer [54] исследовал относительную активность различных прогестагенов (с или без этинилэстрадиола 0,1 мг) в отношении контроля цикла и ингибирования овуляции у женщин с регулярным менструальным циклом. Не было получено положительного ответа (т.е. отсутствие задержки менструации) при приеме дидрогестерона 40 мг. Не было выявлено, чтобы дидрогестерон в дозах 5 и 20 мг ингибиро-вал овуляцию в каком-либо из пяти циклов, в которых он оценивался (табл. 3) [1].
Влияние на эндометрий
1. Влияние на эстроген-стимулированный эндометрий человека
Whitehead [55-56], Lane и др. [57], а позже Siddle и др. [58] и Rees и др. [59] показали, что дидрогестерон 10 мг и 20 мг эффективны в снижении эпителиатьного синтеза ДНК и уровней ядерных рецепторов эстрадиола до значений в рамках секреторной фазы, вызывая полную секреторную трансформацию. Доза 20 мг дидрогестерона способствовала полной секреторной трансформации, тогда как 10 мг МПА и 300 мг микро-низированного прогестерона не выявили такого свойства.
2. Аменорея/Ълигоменорея
Считается, что пациентки с вторичной аменореей имеют повышенный риск развития гиперплазии эндометрия или рака, особенно если они имеют нормальные/ высокие уровни эндогенного эстрогена и НЛФ [72]. К ним также относятся пациентки с олигоменореей, которая определяется как менструация с интервалом от 35 дней до б месяцев. Лечение прогестагенами может защитить эндометрий от пролифера-тивного действия эстрогена и вызывать менструацию при отмене гестагенов.
Последовательное лечение дидрогестероном 10 мг в течение 14 дней/цикл на протяжении 6 циклов оценивалось в двойном слепом рандомизированном плацебо-контролируемом исследовании при участии 104 женщин с вторичной аменореей или олигоменореей и нормальными уровнями эстрогена [73]. У женщин, принимавших дидрогестерон, значительно чаще, чем при приеме плацебо, наблюдалась менструация на фоне отмены в первом цикле (65,4% по сравнению с 30,8%; р=0,0004) и регулярность менструации в течение шести циклов была выше у принимавших дидрогестерон (р<0,0001).
Таблица 3
Пероральные дозы прогестагенов (мг/день), необходимые для трансформации эндометрия и ингибирования овуляции у женщин [1]
| Трансформация эндометрия | Ингибирование овуляции | ||
| Последовательная терапия | Непрерывная терапия | ||
| Микронизированный прогестерон | 200-300 | 100 | 300 |
| Дидрогестерон | 10-20 | 5-10 | >30 |
| МПА | 5-10 | 2,5 | 10 |
| Медрогестон | 10 | / | 10 |
| Хлормадиона ацетат | 10 | / | 1,5-2,0 |
| Ципротерона ацетат | 1 | / | 1 |
| Номегестрола ацетат | 5 | 2,5 | 5 |
| Промегестон | 0,5 | 0,25 | 0,5 |
| Тримегестон | 0,25-0,5 | / | 0,5 |
| Норэтистерон | 1 | 0,5 | 0,5 |
3. Дисфункциональные маточные кровотечения и нерегулярный цикл
Ановуляция - это состояние, связанное с дефицитом прогестерона, которое может привести к дисфункциональному или нерегулярному маточному кровотечению (нерегулярное, длительное или чрезмерное кровотечение), оставляя тем самым эндометрий под воздействие эстрогена. В ряде исследований оценивались различные режимы дозирования дидрогесте-рона (10 мгодин или два раза вдень на 11-25,14-28, 16-25 и 19-25 дни) с или без эстрогенов [75-80]. Наблюдалось последовательное улучшение регулярности менструального цикла в комбинации с уменьшенной продолжительностью и тяжестью кровотечения и меньшей дисменореей.
4. Защита эндометрия при использовании ЗГТ
Основной опасностью монотерапии эстрогенами в период постменопаузы является гиперстимуляция эндометрия. Это действие дозозависимое, частота возникновения рака зависит как от дозы, так и продолжительности воздействия |67|. Было выявлено, что только добавление прогестагена является эффективным в профилактике рака эндометрия. Непрерывное комбинированное лечение с эстрогеном и про-гестагеном позволяет предупредить пролиферацию эндометрия, поддерживая эндометрий в атрофичном или пассивном состоянии. Дозировки прогестагена в таком режиме могут быть более низкими по сравнению с циклической терапией, хотя общее количество прогестагена на цикл довольно схоже, если не идентично.
Оценка долговременной защиты эндометрия, полученная с помощью биопсии, наиболее точно прогнозирует клиническую активность прогестагенов. Было признано, что полная секреторная трансформация не требуется для обеспечения защиты эндометрия. Приведение эндометрия в «истощенное» атрофическое/пассивное состояние без стимуляции также обеспечивает безопасность.
Таблица 4
Пероральные дозы прогестерона (мг/день), необходимые для выявления изменений, эквивалентных эндометрию в секреторной фазе в период пременопаузы [56]
| Маркерный индекс | ЯРЭ | Эстрадиол дегидрогеназа | Изолимонная дегидрогеназа | Морфология | Консенсусное значение | |
| Норэтистерон | < 0,35 | <0,35 | <0,35 | <0,35 | 0,35 | 0,35 |
| D/L-норгестрел | < 0,075 | 0,15 | < 0,075 | < 0,075 | 0,075 | 0,075 |
| МПА | 5 | <23 | <2,5 | <2,5 | > 10 | 5 |
| Дидрогестерон | 20 | 10 | <5 | 10 | 20 | 10 |
| Прогестерон | 1506 | 200 | 250 | 200 | >300 | 20 |
Таблица 5
Ответ эндометрия при S, 10,15 и 20 мг дидрогестерона, комбинированного с 2 мг эстрадиола [62]
| Доза дидрогестерона (мг) | ||||
| 5 | 10 | 15 | 20 | |
| Биопсии(n) | 50 | 90 | 96 | 50 |
| Адекватная защита эндометрия (n) | 47 | 87 | 94 | 49 |
| Неудачный исход (n) | 3 | 3 | 2 | 1 |
| Уровень успешности (%) | 94,0 | 96,7 | 97,9 | 98,0 |
| Доверительный интервал ниже 95% | 85,2 | 91,6 | 93,6 | 90,9 |
Несколько больших исследований сравнивали действие дидрогестерона и МПА, последовательно комбинируемых с различными эстрогенами (трансдермальный эс-традиол, пероральный КЛЭ). Delzanno и др. [68] выявили превосходящее действие 10 мг дидрогестерона по сравнению с 10 мг МПА (оба в комбинации с трансдермальным эстрадиолом 50 мкг), что проявлялось в более высоком процентном соотношении трансформации в секреторный эндометрий без развития гиперплазии. Через б месяцев не было случаев гиперплазии среди 143 женщин, принимающих дидрогестерон, тогда как у 4/85, принимающих МПА, была выявлена гиперплазия эндометрия. Celfand и др. [60] сравнивали 10 мг дидрогестерона и 10 мг МПА, оба последовательно комбинируемые с 0,625 КЛЭ, в 1-годич-ном исследовании среди 77 женщин в период постменопаузы. Дидрогестерон и МПА проявили аналогичное защитное действие в отношении эндометрия, без случаев развития гиперплазии, хотя дидрогестерон имел превосходящее действие относительно МПА в отношении менструальноподобной реакции.
6-месячное исследование с различными дозировками дидрогестерона (5, 10, 15 и 20 мг), последовательно комбинируемыми с 2 мг эстрадиола среди 371 женщин в период постменопаузы, показало, что 10 мг дидрогестерона –оптимальная доза для защиты эндометрия (табл. 5) [62]. Этот эффект был подтвержден в 1-годичном исследовании, в котором 188 женщин принимали 10 мг дидрогестерона, последовательно комбинируемого с 2 мг эстрадиола [65]. Уровень адекватного прогестагенного ответа (секреторный или атрофический эндометрий) составлял 97,2%. Мета-анализ двух двойных слепых 6-месячных исследований и двух открытых долгосрочных (1 или 2 года) исследований с участием 369 женщин, которые принимали 10 мг дидрогестерона, последовательно комбинируемого с 2 мг эстрадиола, показали, что уровень успешности составляет 99,7% [65]. Это сопоставимо с данными, полученными среди женщин в период постменопаузы без лечения в общей популяции [69]. Исследование, изучающее безопасность эндометрия через 1 год лечения комбинацией 1 мг эстрадиола с 5 или 10 мг дидрогестерона, также показало, что обе дозировки дидрогестерона обеспечивали адекватную защиту эндометрия [70].
Исследования с подбором доз также было проведено для определения самой низкой эффективной дозы дидрогестерона при постоянном приеме в комбинации с 1 или 2 мг эстрадиола [67]. Данные получены в исследовании при участии 650 женщин в 3 одногодичных исследованиях при использовании 1 мг эстрадиола, при участии 310 женщин в двух 24-недельных исследованиях при использовании 2 мг эстрадиола. Для подтверждения безопасности эндометрия при постоянном комбинированном приеме 5 мг дидрогестерона и 1 мг эстрадиола Quereux и др. [65] провели 1-годичное исследование среди 290 женщин. Уровень успешности в этом случае составлял 99,6%.
Влияние на клетки рака молочной железы
Доминирующее большинство клеток рака молочной железы на ранних стадиях являются гормонозависимыми, известно, что эстрадиол (Э2) играет важную роль в возникновении и развитии опухоли. Количественные данные показывают, что «сульфатазный путь», превращающий сульфаты эстрогена в биоактивный неконъюгированный Э2, в 100-500 раз превышает «ароматазный путь», который превращает андрогены в эстрогены. Антиэстрогены (например, тамоксифен), различные прогестагены (например, дидрогестерон и его активный метаболит ДГД), медрогестон, промегестон и номегестрола ацетат), тибо-лон и его метаболиты, а также другие стероидные и нестероидные соединения являются сильными ингибиторами сульфатазы [41]. Эти прогестагены также могут блокировать конверсию эстрона в эстрадиол. Основываясь на этих данных, Pasqualini и Chetrite предложили концепцию селективных модуляторов эстрогеновых рецепторов (СМЭР) [42]
СМЭР (например, тамоксифен или ралоксифен) снижают риск развития рака молочной железы в результате индукции апоптоза (потеря ядерной ДНК), но могут усилить или вызвать климактерические симптомы. ЗГТ могла бы смягчить эти симптомы. Исследования in vitro Franke и Vermes [43, 44], а также Werner и др. [45] показывают, что не все прогестагены одинаково действуют на клетки рака молочной железы. Так, МПА, норэтистерона ацетат и диеногест в качестве монотерапии или в комбинации с Э2 стимулируют пролиферацию клеток рака молочной железы, тогда как дидрогестерон, тиболон или прогестерон в качестве монотерапии или в комбинации с Э2 вызывают апоптоз [43].
ЛИТЕРАТУРА
1. Schindler AE, Campagnoli C, Druckmann R, et al. Classification and pharmacology of progestins. Maturitas 2008:61:171 -80.
2. Jalkancn J. Interaction of 17 beta-estradiol and progesterone production in human granulosa-lutcal cells. Eur J Obstet Gynecol Reprod Biol 1990;37:143-53.
3. Lobb DK, Soliman SR, Daya S, Younglai EV. Steroidogenesis in luteinized granulosa cell cultures varies with follicular priming regimen. Hum Reprod 1998:13:2064-7.
4. Branchaud CL, Goodyer CG, Lipowski LS. Progesterone and estrogen production by placental monolay-er cultures: effect of dehy-droepiandrosterone and luteinizing hormone-releasing hormone. J Clin Endocrinol Metab 1983;56:761-6.
5. Selvaraj N, Dantes A, Amsterdam A. Establishment and characterization of steroidogenic granulosa cells expressing beta(2)-adrcncrgic receptor: regulation of adrenodoxin and steroidogenic acute regulatory protein by adrenergic agents. Mo'i Cell Endocrinol 2000; 168:53-63.
6. Devoto L, Kohen P, Vega M, et al. Control of human luteal steroidogene-sis. Cell Endocrinol 2002; 186:137-41.
7. Hillensjo T, Sjogren A, Strander B, et al. Effect of gonadofrophins on progesterone secretion by cultured granulosa cells obtained from human preovulatory follicles. Acta Endocrinol (Copenh) 1985;110:401-7.
8. Warden SE, Edwards DP. Mechanisms controlling agonist and antagonist potential of selective progesterone receptor modulators (SPRMs). Semin Reprod Med 2005;23:9-21.
9. Schindler AE. Endocrinology of pregnancy: consequences for the diagnosis and treatment of pregnancy disorders. J Steroid Biochem Mo'i Biol 2005;97:386-8.
10. Schindler AE. immunology and progestins in pregnancy. Gynecol Endocrinol 1999; 3(Suppl.4):47-50.
11. Schindler AE. Gestagene, endometrium und endometriosc. Gestagene und endometrium. Zentralbl Gynakol 1997;119:59-63.
12. Writing Group for the PEPi Trial. Effects of hormone replacement therapy on endometrial histology in post-menopausal women. The post-menopausal estro-gen/progestin intervention trial. JAMA 1996; 275:370-5.
13. Tamaya T, Furuta N, Ohono Y, Ide N, Tsurusaki T, Okada H. Chromatin transcription by progesto-gen-receplor in rabbit uterus. Endocrinol Jpn 1979;26:117-22.
14. Tamaya T, Tsurusaki T, Ide N, et al. Nucleartranslocation of progesterone receptor-progestogen complex in vitro. Acta Obstet Gynaecol Jpn 1983;35:77-82.
15. Reerink EH, Scholcr HFL Westerhof P, et al. A new class of hormonally active steroids. Nature 1960;186:168-9.
16. Colombo D, Fcrraboschi P, Prestileo P, Torna L. A comparative molecular modeling study of dydro-gesterone with other progestational agents through theoretical calculations and nuclear magnetic resonance spectroscopy! Steroid Biochem Mo'i Biol 2006;98:56-62.
17. Van Amsterdam PH, Overmars H, Scherpenisse PM, de Bree H. Dydrogcsterone: metabolism in man. EurJ Drug Metab Pharmacokinet 1980;5:173-84.
18. Okada H. Iwasaki S, Take H, Matsuyoshi K, Houki N. Liver metabolism of 6-dehydroretroproges-terone in rats. 1. Reduction of C20-ketonc. Nippon Nai-bunpi Gakkai Zasshi 1965;41:856-9.
19. Houki N. Study on the metabolism of progestins, pregnane compounds, in vivo. Nippon Naibunpi Gakkai Zasshi 1966;42:900-17.
20. Queisser-Lull A. Dydrogesterone use during pregnancy: overview of birth defects reported since 1977. Early Hum Dev 2009;85:375-7.
21. Baiasch J, Vanrell J, Marquez M, Gonzalez-MerloJ. Dchydrogcsteronc treatment of endometrial luteal phase deficiency after ovulation induced by clomiphene citrate and human chori-onic gonadotropin. Fcrtil Steril 1983;40:469-71.
22. Cohen MR, Perez-Pelaez M. The effect of norethindrone acetate-ethinyl estradiol, clomiphene citrate, and dydrogesterone on spinnbarkeit. Fcrtil Steril 1965; 16:141-50.
23. Okada H. Metabolism, structure and biological activity of sex steroids. Folia Endocrinol 1993;69:67-79.
24. Picolet II, Girard P, Ncmoz C, Boissel JP. Effects of dydroges-terone on hydro-electrolytic metabolism: a randomized double-blind study. Gynecol Endocrinol 1990;4:219-24.
25. Satake M, Sakai K, Takano J, el al. Urinary excretion of steroid hormones in menstruation disorders and its significance. Horumon To Rinsho 1971; 19:548-52.
26. Hulley S, Grady D, Bush T, et al. Randomized trial of estrogen plus progestin for secondary prevention of coronary heart disease in post-menopausal women. Heart and Estrogen/progestin Replacement Study (HERS) Research Group. JAMA 1998;280:605-13.
27. Grady D, Herrington D, BittnerV, et al. Cardiovascular disease outcomes during 6.8 years of hormone therapy: heart and estrogen/progestin replacement study follow-up (HERS II). JAMA 2002; 288:49-57.
28. Rossouw JE, Anderson GL, Prentice RL, et al. Risks and bchefils of estrogen plus progestin in healthy postmenopausal women: principal results from the Women's Health Initiative randomized controlled trial. JAMA 2002;288:321-33.
29. Beral V. Million Women Study CollaborBt ore. Breast cancer and hormone-replacement therapy in the Million Women Study. Lancet 2003;362:419-27.
30. Anderson GL, Limacher M, Assaf AR, et al. Effects of conjugated equine estrogen in postmenopausal women with hysterectomy: the Women's Health Initiative randomized controlled trial. JAMA2004;291: 1701-12.
31. Schindler AE. Differential effects of progestins. Maturitas 2003; 46S1: S3-5.
32. European Progestin Club: Editorial. Progestins: present and future. J Steroid Biochem Mo'i Biol 1996;59:357-63.
33. Junkmann K. Experimented Gesichtspunkte bei der Prbfung Synthetischer Gestagene. Dtsch Med Wschr 1963;88:629-38.
34. Kontula K, Janne O, Vihko Ft, de Jager E, de Visser J, Zeelen F. Progesterone binding proteins: in vitro binding and biological activity of different steroidal ligands. Acta Endocrinol 1975;78:574-92.
35. Wilks JW, Spilman CH, Campbell JA. Steroid binding specificity of the hamster uterine progesterone receptor. Steroids 1980;35:697-706.
36. Meglioli G, Desaullcs PA. Modifications induced by progesto-gen treatment in the action of rat uterine secretion on corona cells in vitro. Hormone Res 1973;4:288-92.
37. Meglioli G, Kalvoda J, Desaullcs PA. Effects of progesto-genic substances on the uterine secretion of spayed rats primed with oestradiol. Hormone Res 1973;4: 97-106.
38. Saure A, Karjalainen 0, Tcravainen T. The effect of synthetic gestagens on progesterone formation in vitro in human corpus luteum of early pregnancy. EurJ Obstet Gynecol Reprod Biol 1976;6: 223-34.
39. Madjcrek Z, Smit-Vis JH. Assessment of a bioassay of proges-tational activity, J Endocrinol 1975; 66:135-6.
40. Madjcrek ZS, Smit-Vis JH. Further studies on a new bioassay of progestational activity (Traumatic deciduoma formation in immature rats). Acta Morphol Neer-Scand 1977;15:65-74.
41. Chetrite GS, Thole HH, Philippe JC, Pasqualini JR. Dydrogesterone (Duphas-ton) and its 20-di-hydro-derivative as selective estrogen enzyme modulators in human breast cancer cell lines. Effect on sulfa-tasc and on 17bcta-hydroxysteroid dehydrogenase (17bcta-HSD) activity. Anticancer Res 2004;24:1433-8.
42. Pasqualini JR. Chetrite GS. Recent insights on the control of enzymes involved in estrogen formation and transformation in human breast cancer. J Steroid Biochem Mo'iBiol 2005;93:221-36.
43. Franke HR, Kole S, Ciftci Z, Haanen C, Vermes 1. In vitro effects of estradiol, dydrogesterone, tamoxifen and cyclophosphamide on proliferation vs. death in human breast cancer cells. Cancer Lett 2003; 190:113-8.
44. Franke HR, Vermes I. Differential effects of progestogens on breast cancer cell lines. Maturitas 2003;46SI:55-8.
45. Werner HM, Franke HR, Vermes I. Apoptosis and proliferation in breast cancer cells, cultured in vitro: effects of SERMs. Climacteric 2005;8:294-9.
46. Sugawa H, Moriyama I, Kakita M. The action of delta-6-retroproges-teronc (Duphaston) on DNA synthesis of the uterine endometrium. Clin Endocrinol 1969;17:876-7.
47. Maiiioli F, Garbero C, Gosmar M, et al. DNA fragmentation, DNA repair and apoptosis induced in primari rat hepatocytes by dicnogest, dydrogesterone and 1,4,6-Androstalriene-17ij-ol-3-one acetate. Mutat Res 2004;564:21-9.
48. Simoncini T, Caruso A, Giretti MS, et al. Effects of dydroges-terone and of its stable metabolite, 20-alpha-dihydrodydrogestcrone, on nitric oxide synthesis in human endothelial cells. Fcrtil Steril 2006;86(Suppl. 4): 1235-42.
49. Kumasaka T, Itoh E, Watanabe H, lloshino K, Yoshinaka A, Masawa N. Effects of various forms of progestin on the endometrium of the estrogen-primed, ovariectomized rat. EndocrJ 1994;41:161-9.
50. Neumann F. Chemische Konstitution und pharmakologische Wirkung. In: Handbuch der Experimented Pharmakologie (Handbook of Experimental Pharmacology), Kapitel VI, Teil 1, Die Gestagene. Berlin, Heidelberg, New York: Springer Verlag: 1968.
51. Joachim R, Zenclusscn AC, Polgar B, el al. The progesterone derivative dydro-gesterone abrogates murine stress-triggered abortion by inducing a Th2 biased local immune response. Steroids 2003;68:931-40.
52. Blois SM, Joachim Ft, Kandil J, et al. Depletion of CD8+ cells abolishes the pregnancy protective effect of progesterone substitution with dydrogesterone in mice by altering the Thl/Th2 cytokine profile. J Immunol 2004:172: 5893-9.
53. Raghupathy R, Al Mutawa E, Makhseed M, Azizieh F, Szekercs-Bartho J. Modu-lation of cytokine production by dydrogesterone in lymphocytes from women with recurrent miscarriage. BJOG 2005:112:1096-101.
54. Swyer GIM. Small-scale clinical trials of progestogens for control of conception. IntJFertil 1964;9:11-6.
55. King R, Whitehead M. Assessment of the potency of orally administered progestins in women. Fcrtil Steril 1986;46:1062-6.
56. Ryder T, Mobberley M, Whitehead M. The endometrial nucleolar channel system as an indicator of progestin potency in HRT. Maturitas 1995;22:31-6.
57. Lane G, Siddle NC, Ryder TA, Pryse-Davies J, King RJ, Whitehead Ml. Effects of dydrogesterone on the ocstrogenized post-menopausal endometrium. Br J Obstet Gynaecol 1986;93:55-62.
58. Siddle N, FrAser D, Whitehead M, et al. Endometrial, physical and psychological effects of postmenopausal oestrogen therapy with added dydrogesterone. Br J Obstet Gynaecol 1990;97:1101-7.
59. Rees M, Leather A, Pryse-Davies J, Collins SA, Barlow DH, Studd JW. A first study to compare two dosages of dydrogesterone in opposing the 50 mg oestradiol implant. Maturitas 1991;14:9-15.
60. Gelfand M, Fugere P, Bissonette F, et al. Conjugated estrogens combined with sequential dydrogesterone or medroxyproges-terone acetate in postmenopausal women: effects on lipoproteins, glucose tolerance, endometrial histology and bleeding. Menopause 1997;4:10-8.
61. Burch DJ, Spowart KJM, Jesinger DK, Randall S, Smith SK. A dose-ranging study of the use of cyclical dydrogesterone wilhcontinu-ous 17beta-oestradioL BrJ Obstet Gynaecol 1995;102:243-8.
62. van der Mooren MJ, Hanselaar AGJM, Bonn GF, Rolland R. Changes in the withdrawal bleeding pattern and endometrial histology during 17bcta-eslradiol-dydrogesterone therapy in postmenopausal women: a 2-year prospective study. Maturitas 1995;20:175-80.
63. Bergeron C, Fox H. Low incidence of endometrial hyperplasia with acceptable bleeding patterns in women taking sequential hormone replacement therapy with dydrogesterone. Gynecol Endocrinol 2000;14:275-81.
64. Ferenczy A, Gelfand MM. Endometrial histology and bleeding patterns in post-menopausal women taking sequential, combined estradi-ol and dydrogesterone. Maturitas 1997;26:219-26.
65. Quereux C, Pornel B, Bergeron C, Ferenczy A. Continuous combined hormone replacement therapy with I mg 17p-oestradiol and 5 mg dydrogesterone (Fcmoston®-conti): endometrial safety and bleeding profile. Maturitas 2006:53: 299-305.
66. Bergeron C, Ferenczy A. Endometrial safety of continuous combined hormone replacement therapy with 17beta-oestradiol (I or 2mg) and dydrogesterone. Maturitas 2001;37:191-9.
67. Whitehead Ml, FrAser D. The effects of estrogens and progesto-gens on the endometrium. Modern approach to treatment. Obstel Gynecol Clin North Am 1987; 14:299-320.
68. Delzanno G, Paoletti R, Gaudiano L, Bertinelli G, Ventrella CA, Dell'ElceC Dihydro-gesterone versus medroxyproges-terone acetate in association with transdermal oestradiol in post-menopausal replacement therapy. Minerva Ginecol 1994;46:179-82.
69. Korhonen MO, Symons JP, Hyde BM, Rowan JP, Wilborn WH. Histologic classification and pathologic findings for endometrial biopsy specimens obtained from 2964 peri-menopausal and postmenopausal women undergoing screening for continuous hormones as replacement therapy (CHART 2 Study). Am J Obstet Gynecol 1997;176:377-80.
70. van de Weijer PHM, Schulten PC, van der Mooren MJ, Barentscn R, Kcncmans P. Bleeding patterns and endometrial histology during administration of lowdosc estradiol sequentially combined with dydrogesterone. Climacteric 1999;2:101-9.
71. Woodruff JD, Pickar JH. Incidence of endometrial hyperplasia in postmenopausal women taking conjugated estrogens (Premarin) with medroxyprogesterone acetate or conjugated estrogens alone. Am J Obstet Gynecol 1994; 170:1213-23.
72. J Modan B, Ron E, Lcrncr-Geva L, et al. Cancer incidence in a cohort of infertile women. Am J Epidemiol 1998;147:1038-42.
73. Panay N, Pritsch M, Alt J. Cyclical dydrogesterone in secondary amenorrhea: results of a double-blind, placebo-controlled, randomized study. Gynecol Endocrinol 2007;23:611-8.
74. Battino S, Ben-Ami M, Geslevich Y, Weiner E, Shalev E. Factors associated with withdrawal bleeding after administration of oral dydrogesterone or medroxyprogesterone acetate i n women with secondary amenorrhoea. Gynecol Obstet Invest 1996;42:113-6.
75. Tabaste JL, Servaud M, Steiner E, Dabir P, Bene B, Pouzet M. Action of dydro-gesterone in postpuberal menstruation disorders. Rev Fr Gynecol Obstet 1984;79:19-25.
76. Sipowicz I, Chomczyk 1. The efficacy of dydrogesterone in the treatment of menstrual cycle disturbances in girls. Ginekol Pol 1998;69:767-70.
77. Chomczyk I, Sipowicz M, Sipowicz 1. Dydrogesterone in the regulation of cycle disturbances in adolescence. Ginekol Pol 1999;70:343-7.
78. Anklesaria B, Balamba P, Banerjee B. Cycle regulation with dydrogesterone in Indian women. Obstet Gynaecol 1999; IV: 559-64.
79. Naib JM, Siddiqui Ml, Ajmal W. The role of dydrogesterone in the medical man-agement of 100 cases of dysfunctional uterine bleeding (DUB) above 35 years of age. J Postgrad Med Inst Peshawar 2003;17(2).
80. Dutta DK. Management of luteal phase defect (LPD) in adolescent girls. Asian J Obstet Gynaecol Pract 2001;5:3-5.
(Печатается с сокращениями, полная версия статьи - Maturitas2009:65)
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


