
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
- Новини 26.10.2021 Аппаратура для УЗИ: применение, принципы работы, разновидности
- Новини 23.10.2021 Интимная пластика после родов: когда необходима операция
Медикаментозная терапия при гиперхолестеринемии. Ключевые положения американского руководства ATP III
Додати статью Роздрукувати
Начиная с 1995 г. в Украине отмечается прогрессирующий рост смертности от сердечно-сосудистых заболеваний (ССЗ), достигшей в 2008 г. одного из наивысших уровней в Европе — 63,6%, причем в структуре смертности от ССЗ первое место (66,8%) занимает ишемическая болезнь сердца (ИБС). Ежегодно в Украине регистрируют около 50 тыс. новых случаев инфаркта миокарда (в 2008 г. — 50 368) (Бабушкина А.В., 2009).
Актуальность проблемы
В настоящее время необходимость коррекции гиперхолестеринемии у пациентов с ССЗ не вызывает сомнений. С появлением статинов — группы препаратов, благодаря которой в конце XX в. стал возможен поистине революционный переворот в кардиологии, и с развитием доказательной медицины стало очевидным, что сегодня существует единственный путь патогенетического лечения атеросклероза — эффективная гиполипидемическая терапия и снижение в крови уровня атерогенного холестерина липопротеинов низкой плотности (ХС ЛПНП) (Солошенко О., 2009).
Таким образом, в сложившейся ситуации, когда в Украине ССЗ лидируют среди причин смертности и инвалидности, применение статинов особенно актуально. Однако, несмотря на обширную доказательную базу исследований, подтверждающих эффективность статинов при первичной и вторичной профилактике ССЗ, возможности этой группы препаратов до сих пор используются в нашей стране не в полной мере. Юрий Николаевич Сиренко, доктор медицинских наук, профессор, главный кардиолог МЗ Украины, заведующий отделом симптоматических гипертензий Национального научного центра «Институт кардиологии имени академика Н.Д. Стражеско АМН Украины» считает, что сегодня в Украине сложилась катастрофическая ситуация с назначением препаратов этой группы. Так, по приблизительным подсчетам, в 2008 г. < 1% пациентов получили столь необходимое лечение. А поскольку применение статинов доказано способствует снижению смертности вследствие ССЗ, это является недопустимым. Вот почему в сложившейся ситуации нельзя оставаться равнодушным! (Солошенко О., 2009).
Данной публикацией, подготовленной при поддержке компании «Берлин-Хеми Менарини», мы хотим еще раз привлечь внимание практикующих врачей к обсуждаемой проблеме и напомнить ключевые положения одного из основных мировых руководств по ведению пациентов с гиперхолестеринемией — американского доказательного клинического руководства АТР III (от краткого названия 3-го руководства 2001 г. — Adult Treatment Panel III), подготовленного Комиссией экспертов Национальной образовательной программы США по холестерину (National Cholesterol Education Program — NCEP) (Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults, 2001; National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III), 2002), а также дополнения к этому руководству, опубликованному Координационным комитетом NCEP в 2004 г. (Grundy S.M. et al., 2004).
Важно подчеркнуть, что основные рекомендации по ведению пациентов с гиперхолестеринемией, изложенные в АТР III, находят отражение и в современных национальных рекомендациях по диагностике, профилактике и лечению дислипидемий (Коваленко В.М. (ред.), 2009).
АТР III (Adult Treatment Panel III)
Одна из основных целей АТР III — на основании научных данных составить руководство, помогающее специалистам и общественности принимать надлежащие меры для снижения риска ИБС и ССЗ.
Подчеркивается, что эффективное выявление, оценка и терапия гиперхолестеринемии у взрослых могут способствовать снижению заболеваемости и смертности вследствие ИБС.
Польза от снижения уровня ХС в отношении смертности. Терапия, направленная на снижение уровня ЛПНП, способствует снижению общей смертности (то есть продлевает жизнь за счет снижения заболеваемости ИБС). Эта польза от терапии не была точно установлена в ранее проведенных испытаниях, в которых применяли вмешательства с ограниченным снижением уровня ХС (на 10%); в некоторых из указанных испытаний установлены неблагоприятные эффекты в отношении заболеваний, не относимых к ИБС. Однако в клинических испытаниях с применением статинов, в которых уровень ХС снижался на 20% и не повышалась смертность вследствие заболеваний, не относимых к ИБС, неопровержимо доказано снижение смертности.
Польза от снижения уровня ХС при вторичной профилактике в отношении смертности. Данные о пользе снижения уровня ХС для продолжительности жизни особенно убедительны у пациентов с ИБС и других групп высокого риска, что обусловлено высокой смертностью в ближайший период при отсутствии лечения пациентов данных групп, а также большой долей случаев смерти вследствие ИБС. У лиц с установленной ИБС уменьшение количества случаев смерти вследствие ИБС в результате проведения эффективной гипохолестеринемической терапии неоспоримо превышает значимость какихлибо побочных эффектов медикаментозного лечения.
Польза от снижения уровня ХС при первичной профилактике в отношении смертности. Результаты клинических испытаний, касающиеся первичной профилактики с применением статинов, продемонстрировали значительное снижение смертности вследствие ИБС, отсутствие повышения смертности, не обусловленной ИБС, а также отчетливую тенденцию к снижению общей смертности. В связи с меньшей долей случаев смерти, обусловленных ИБС, в испытаниях по первичной профилактике (по сравнению с отмечаемой при вторичной профилактике) последняя тенденция не является значимой. Клинические испытания с применением статинов проводили в среднем в течение 5 лет; обсервационные исследования большей продолжительности служат более наглядным свидетельством потенциального влияния на протяжении всей жизни пациента снижения ХС на смертность. Отсутствие общего снижения смертности при проведении клинических испытаний по первичной профилактике до открытия статинов можно объяснить незначительным снижением уровня ХС (< 10%) и в некоторых случаях — неблагоприятными эффектами в отношении заболеваний, не относимых к ИБС, которые не отмечали при терапии статинами.
В руководстве рассматриваются следующие вмешательства и практики:
- Определение уровня липопротеинов натощак (общего холестерина — ХС, холестерина липопротеинов низкой (ХС ЛПНП) и высокой (ХС ЛПВП) плотности и триглицеридов — ТГ).
- Выявление основных факторов риска, а также факторов риска, обусловленных «нездоровым» образом жизни, и новых факторов риска.
- Определение 10-летнего риска ИБС по Фрэмингемской шкале оценки риска (Framingham scoring).
Оценка риска — первый этап в системе мер по снижению риска
Базовый принцип профилактики состоит в корректировке в зависимости от величины абсолютного риска у каждого пациента интенсивности терапии, направленной на снижение риска. Следовательно, первым этапом в выборе гиполипидемической терапии для снижения ЛПНП является оценка степени риска у данного пациента. Оценка риска требует определения уровня ХС ЛПНП в рамках комплексного анализа липопротеинов и выявления сопутствующих факторов риска.
ХС ЛПНП — первостепенная цель терапии
Результаты экспериментов на животных, лабораторных и эпидемиологических исследований, а также изучение генетических форм гиперхолестеринемии свидетельствуют о том, что повышенный уровень ХС ЛПНП является основной причиной ИБС. Кроме того, в недавно проведенных исследованиях получены устойчиво воспроизводимые результаты, доказывающие, что терапия, направленная на уменьшение уровня ЛПНП, снижает риск развития ИБС. Исходя из этого, в АТР III сохранено определение, согласно которому повышенный уровень ХС ЛПНП является первостепенной целью гиполипидемической терапии. Поэтому первостепенные цели терапии и критические уровни, при которых необходимо ее начинать, указаны по отношению к ХС ЛПНП.
Первичная и вторичная профилактика ИБС посредством гиполипидемической терапии, направленной на снижение уровня ХС ЛПНП, предполагает
- Лечебные изменения образа жизни (therapeutic lifestyle changes) (ЛИОЖ), в том числе диетотерапию, уменьшение массы тела и повышение физической активности (схема 1).
- Медикаментозную терапию, включающую ингибиторы 3-гидрокси-3-метил-глютарил-коэнзим А (ГМГ-КоА) редуктазы (статины), секвестранты желчных кислот, никотиновую кислоту и производные фиброевой кислоты (фибраты).
Схена 1
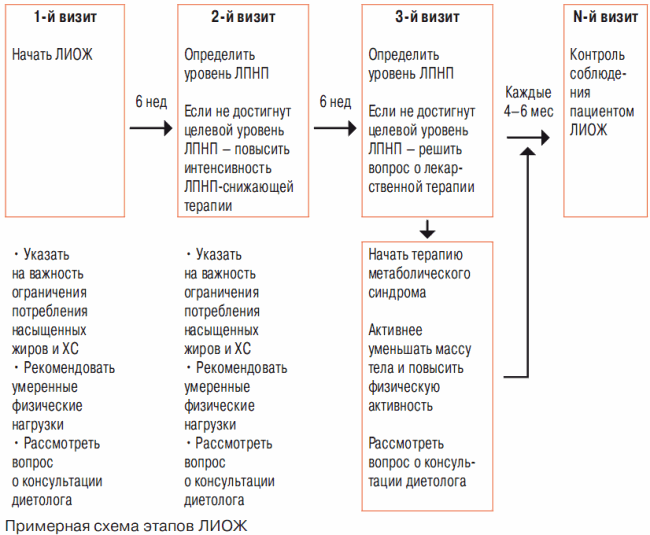
Медикаментозная терапия для достижения целевого уровня ХС ЛПНП
Часть пациентов с высоким ближайшим и отдаленным риском развития ИБС дополнительно к проведению ЛИОЖ нуждаются в назначении гиполипидемических средств для достижения целевого уровня ХС ЛПНП (табл. 1). В табл. 2 приведены целевые и критические уровни ХС ЛПНП из АТР III, а также предлагаемые в дополнении 2004 г. изменения алгоритма лечения в отношении ХС ЛПНП на основании доказательств, полученных в последних клинических испытаниях (Grundy S.M. et al., 2004). Важные изменения указаны в примечаниях к табл. 2 и резюмированы ниже в табл. 3.
Таблица 1. Целевые и критические уровни ХС ЛПНП для ЛИОЖ и медикаментозной терапии у лиц 3 групп риска
|
Группа риска |
Целевой уровень ХС ЛПНП, мг/дл |
Уровень ЛПНП для начала ЛИОЖ, мг/дл |
Уровень ЛПНП, при котором рекомендуется фармакотерапия, мг/дл |
|
ИБС или риски, эквивалентные ИБС (10-летний риск > 20%) |
< 100 |
≥ 100 |
≥ 130 (при 100–129 мг/дл: рассмотреть вопрос о вариантах фармакотерапии)1 |
|
> 2 факторов риска (10-летний риск ≤ 20%) |
< 130 |
> 130 |
При 10-летнем риске 10–20%: ≥ 130 |
|
0–1 фактор риска2 |
< 160 |
> 160 |
≥ 190 (при 160–190 мг/дл: рассмотреть вопрос о вариантах фармакотерапии, снижающей ЛПНП) |
1 Некоторые специалисты рекомендуют в данной группе применение лекарственных препаратов для снижения ЛПНП в случаях, когда посредством ЛИОЖ невозможно достичь целевого уровня ХС ЛПНП < 100 мг/дл. Другие специалисты предпочитают применять лекарственные средства, преимущественно влияющие на уровень ТГ и ЛПВП, например никотиновую кислоту или фибраты. Также возможно принятие клинического решения об отсрочке проведения фармакотерапии в этой подгруппе пациентов.
2 Почти у всех лиц с 0–1 фактором риска 10-летний риск составляет < 10%, поэтому необходимость в его оценке отсутствует.
Таблица 2. Целевые и критические уровни ХС ЛПНП (из ATP III) для проведения ЛИОЖ и медикаментозной терапии у пациентов различных групп риска, а также предлагаемые изменения на основании данных последних клинических испытаний
|
Группа риска |
Целевой уровень ХС ЛПНП, мг/дл |
Критический уровень ХС ЛПНП, при котором рекомендуется принятие мер, мг/дл |
|
|
ЛИОЖ |
Медикаментозная терапия |
||
|
Высокий риск: ИБС1 или риск, эквивалентный ИБС2 (10-летний риск >20%) |
< 100 (по усмотрению: <70)6 |
≥ 1008 |
≥ 10010 (<100 мг/дл: рассмотреть вопрос о вариантах медикаментозной терапии)9 |
|
Умеренно высокий риск: >2 факторов риска3 (10-летний риск 10–20%)4 |
<1307 |
≥1308 |
≥130 (100–129 мг/дл: рассмотреть вопрос о вариантах медикаментозной терапии)11 |
|
Умеренный риск: > 2 факторов риска3 (10-летний риск < 10%)4 |
< 130 |
≥ 130 |
≥ 160 |
|
Низкий риск: 0–1 факторов риска5 |
< 160 |
≥ 160 |
≥ 190 (160–189 мг/дл: гиполипидемическая терапия по усмотрению) |
1 ИБС включает наличие в анамнезе указаний на инфаркт миокарда, нестабильную или стабильную стенокардию, хирургические вмешательства на коронарных артериях (ангиопластика или шунтирование) или же доказательств клинически значимой ишемии миокарда.
2 Риски, эквивалентные ИБС, включают клинические проявления некоронарных форм атеросклероза (атеросклероз периферических артерий, аневризма брюшной аорты и атеросклероз сонных артерий [транзиторные ишемические атаки или инсульт в результате поражения сонных артерий, или обструкция сонной артерии > 50%]), сахарный диабет и множественные (>2) факторы риска при 10-летнем риске развития тяжелых форм ИБС > 20%.
3 Факторы риска включают табакокурение, артериальную гипертензию (АД ≥ 140/90 мм рт.ст. или прием антигипертензивных лекарственных средств), низкий уровень ХС ЛПВП (< 40 мг/дл), раннее развитие ИБС в семейном анамнезе (ИБС у родственника первой степени родства по мужской линии в возрасте < 55 лет; ИБС у родственницы первой степени родства по женской линии в возрасте < 65 лет) и возраст (мужчины ≥ 45 лет; женщины ≥ 55 лет).
4 В сети Интернет имеются специальные электронные калькуляторы для подсчета 10-летнего риска, которые можно найти по адресу: www.nhlbi.nih.gov/guidelines/cholesterol.
5 Почти все лица с 0–1 фактором риска имеют 10-летний риск < 10%, поэтому нет необходимости в оценке у них этого показателя.
6 Наличие очень высокого риска свидетельствует о целесообразности достижения необязательного целевого уровня ХС ЛПНП порядка < 70 мг/дл, а у пациентов с высоким уровнем ТГ—достижения ХС липопротеинов невысокой плотности (сумма ХС липопротеинов очень низкой плотности (ЛПОНП) и ХС ЛПНП) порядка < 100 мг/дл.
7 Целевой уровень ХС ЛПНП по усмотрению — < 100 мг/дл.
8 Каждый пациент группы высокого или умеренно высокого риска, имеющий факторы риска, связанные с образом жизни (например ожирение, низкая физическая активность, повышенный уровень ТГ, низкий уровень ХС ЛПВП или метаболический синдром), является, независимо от уровня ХС ЛПНП, кандидатом для проведения ЛИОЖ для изменения этих факторов риска.
9 Гиполипидемическую терапию для снижения уровня ЛПНП рекомендуется проводить с интенсивностью, позволяющей достичь не менее 30–40% снижения уровня ХС ЛПНП.
10 Если исходный уровень ХС ЛПНП составляет < 100 мг/дл, то назначение гиполипидемического средства для снижения уровня ЛПНП является терапией по усмотрению на основании результатов имеющихся клинических испытаний. Если у пациента группы высокого риска низкий уровень ХС ЛПВП или высокий уровень ТГ, можно рассмотреть вопрос о целесообразности назначения препарата группы фибратов или никотиновой кислоты в комбинации с гиполипидемическим средством для снижения ЛПНП.
11 Если у пациентов группы умеренно высокого риска уровень ХС ЛПНП (исходный или при проведении ЛИОЖ) составляет 100–129 мг/дл, то назначение гиполипидемического средства для достижения уровня ХС ЛПНП < 100 мг/дл является терапией по усмотрению, исходя из результатов имеющихся клинических испытаний.
Таблица 3. Рекомендации по изменению примечаний к алгоритму лечения (из ATP III) для снижения уровня ХС ЛПНП
- ЛИОЖ остается важным методом клинического ведения пациентов. ЛИОЖ способствует снижению риска сердечно-сосудистой патологии посредством нескольких механизмов дополнительно к снижению уровня ЛПНП.
- У лиц группы высокого риска рекомендуемый целевой уровень ХС ЛПНП составляет < 100 мг/дл.
- Целевой уровень ХС ЛПНП <70 мг/дл является терапией по усмотрению на основании данных имеющихся клинических испытаний, в особенности для пациентов группы очень высокого риска.
- Если ХС ЛПНП оставляет ≥ 100 мг/дл, то одновременно с изменениями образа жизни показано назначение гиполипидемического средства для снижения содержания ЛПНП.
- Если исходный уровень ХС ЛПНП составляет < 100 мг/дл, то назначение гиполипидемического средства для достижения уровня ХС ЛПНП < 70 мг/дл является терапией по усмотрению на основании данных имеющихся клинических испытаний.
- Если у пациента группы высокого риска низкий уровень ХС ЛПВП или высокий уровень ТГ, можно рассмотреть вопрос о целесообразности назначения препарата группы фибратов или никотиновой кислоты в комбинации с гиполипидемическим средством для снижения содержания ЛПНП. Если уровень ТГ составляет ≥ 200 мг/дл, то ХС липопротеинов невысокой плотности (ХС ЛПНП и ХС ЛПОНП) является второстепенной целью терапии, с целевым уровнем на 30 мг/дл выше установленного целевого уровня ХС ЛПНП.
- Для пациентов группы умеренно высокого риска (> 2 факторов риска, 10-летний риск составляет 10–20%) рекомендуемый целевой уровень ХС ЛПНП составляет <130 мг/дл; целевой уровень ХС ЛПНП < 100 мг/дл является терапией по усмотрению на основании данных имеющихся клинических испытаний. Если уровень ХС ЛПНП (исходный или в случае ЛИОЖ) составляет 100–129 мг/дл, то назначение гиполипидемического средства для достижения уровня ХС ЛПНП < 100 мг/дл является терапией по усмотрению на основании данных имеющихся клинических испытаний.
- Каждый пациент группы высокого или умеренно высокого риска, имеющий факторы риска, связанные с образом жизни (например ожирение, низкая физическая активность, повышенный уровень ТГ, низкий уровень ХС ЛПВП или метаболический синдром), является, независимо от уровня ХС ЛПНП, кандидатом для проведения ЛИОЖ для изменения этих факторов риска.
- Лицам группы высокого или умеренно высокого риска рекомендуется проводить гиполипидемическую терапию для снижения содержания ЛПНП с интенсивностью, позволяющей достичь не менее 30–40% снижения уровня ХС ЛПНП.
- Что касается лиц групп более низкого риска, то данные последних клинических испытаний не дают оснований для изменения целевых и критических уровней для проведения терапии.
При медикаментозной терапии всегда необходимо неукоснительно продолжать проведение ЛИОЖ. К средствам, влияющим на метаболизм липопротеинов, в настоящее время относятся ингибиторы ГМГ-КоАредуктазы (статины), секвестранты желчных кислот, никотиновая кислота и фибраты (табл. 4).
Таблица 4. Лекарственные средства, влияющие на обмен липопротеинов
|
Группа лекарственных средств |
Ингибиторы ГМГ-КоА редуктазы (статины)1 |
Секвестранты |
Препараты никотиновой кислоты4 |
Фибраты5 |
|
Влияние на уровень липидов/ |
ЛПНП:↓ на 18–55% ЛПВП: ↑ на 5–15% ТГ: ↓ на 7–30% |
ЛПНП: ↓ на 15–30% |
ЛПНП: ↓ на 5–25% ЛПВП: ↑ на 15–35% ТГ:↓ на 20–50% |
ЛПНП: ↓ на 5–20% (возможно повышение при высоком уровне ТГ) ЛПВП: ↑ на 10–20% ТГ:↓ на 20–50% |
|
Побочные эффекты |
|
|
|
|
|
Противопо- |
Абсолютные:
Относительные:
|
Абсолютные:
Относительные:
|
Абсолютные:
Относительные:
|
Абсолютные:
Относительные:
|
|
Результаты |
Уменьшение количества случаев развития основных коронарных событий, смерти вследствие ИБС, необходимости в проведении операций на коронарных сосудах, случаев инсульта, снижение общей смертности |
Уменьшение количества основных коронарных событий и случаев смерти вследствие ИБС |
Уменьшение количества основных коронарных событий и, возможно, общей смертности |
Уменьшение количества основных коронарных событий |
1 Суточные дозы: ловастатин — 20–80 мг, симвастатин — 20–80 мг, флувастатин — 20–80 мг, аторвастатин — 10–80 мг, церивастатин — 0,4–0,8 мг.
2 Циклоспорин, макролидные антибиотики, различные противогрибковые препараты и средства, ингибирующие ферменты системы цитохрома Р450 (необходима осторожность при назначении фибратов и препаратов никотиновой кислоты).
3 Суточные дозы: колестирамин — 4–16 г, колестипол — 5–20 г, колезевелам — 2,6–3,8 г.
4 Суточные дозы препаратов никотиновой кислоты: с немедленным высвобождением (в кристаллической форме) — 1,5–3 г, с замедленным высвобождением — 1–2 г, с длительным высвобождением — 1–2 г.
5 Суточные дозы: гемфиброзил — по 600 мг 2 раза в сутки, фенофибрат — 200 мг, клофибрат — по 1000 мг 2 раза в сутки.
Вторичная профилактика: медикаментозная терапия при иБС и рисках, эквивалентных иБС
Улиц с ИБС и рисками, эквивалентными ИБС, цель терапии состоит в достижении уровня ХС ЛПНП < 100 мг/дл (см. табл. 1 и 2). Большинству пациентов с ИБС необходимо проведение медикаментозного лечения для снижения ЛПНП. Другие липидные факторы риска также могут стать основанием для назначения фармакотерапии. Независимо от того, применяют или не применяют фармакотерапию для изменения уровня липидов в крови, наличие нелипидных факторов риска требует внимания врача и принятия мер для их устранения.
У лиц, госпитализированных по поводу основного коронарного события, необходимо при госпитализации или в течение 24 ч после нее измерить уровень ХС ЛПНП. На основании этого можно при нимать решение о тактике лечения. В целом, лицам, госпитализированным по поводу коронарного события или хирургического вмешательства на коронарных артериях, следует перед выпиской назначить медикаментозное лечение в случае, если уровень ХС ЛПНП ≥130 мг/дл. При уровне ЛПНП 100–129 мг/дл следует принять клинически обоснованное решение о целесообразности назначения медикаментозной терапии до выписки из больницы, учитывая, что уровень ХС ЛПНП начинает снижаться на протяжении нескольких часов после развития события и значительно снижается через 1–2 сут после этого и может оставаться низким в течение многих недель. Поэтому исходный уровень ХС ЛПНП, установленный при госпитализации, может быть значительно ниже обычно отмечаемого у данного пациента. Некоторые специалисты полагают, что медикаментозную терапию следует проводить всякий раз, когда при госпитализации по поводу патологического состояния, связанного с ИБС, уровень ХС ЛПНП составляет > 100 мг/дл. Начало фармакотерапии до выписки пациента имеет 2 преимущества. Во-первых, в это время у больных особенно высокая мотивация для выполнения всех вмешательств, направленных на снижение риска. Во-вторых, неудача на начальном этапе проведения лечения является одной из причин «пробела в терапии», поскольку амбулаторное наблюдение часто менее адекватно и систематично.
ЛПНП-снижающая терапия в целях первичной профилактики
Критические уровни ЛПНП для решения вопроса о медикаментозной терапии при первичной профилактике — см. табл. 1 и 2. Общий подход к проведению лекарственной терапии отражен на схеме 2.
Схема 2
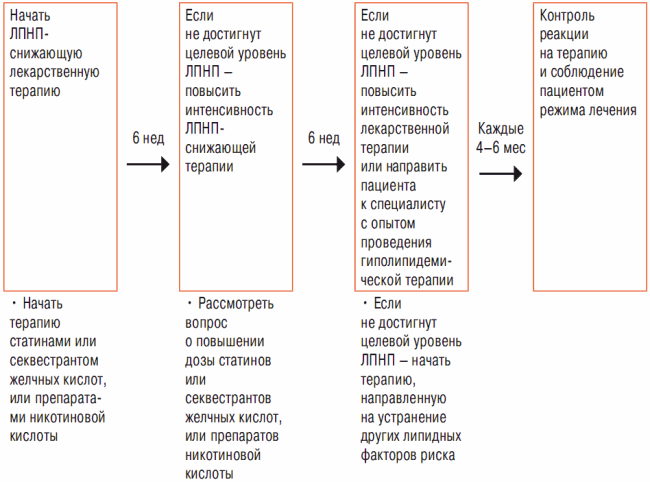
Последовательность проведения медикаментозной терапии
Вопрос о начале проведения лекарственной терапии в целях первичной профилактики, как правило, решается при 3-м посещении врача в рамках проведения диетотерапии (приблизительно через 12 нед после начала ЛИОЖ и ее неэффективности в достижении целевого уровня ЛПНП) (см. схему 1). Даже после начала медикаментозной терапии следует продолжать ЛИОЖ. Как и в случае ЛИОЖ, главной целью медикаментозной терапии является достижение целевого уровня ХС ЛПНП. В связи с этим необходимо применение фармакотерапии. Обычно начинают с препаратов группы статинов, но можно назначить и секвестрант желчных кислот или никотиновую кислоту. В большинстве случаев лечение статинами необходимо начинать с невысоких доз. У многих пациентов это способствует достижению целевого уровня ХС ЛПНП без применения более высоких доз. Реакцию организма на лечение следует проверить через 6 нед после начала медикаментозной терапии. Если целевой уровень достигнут, можно продолжать поддерживающую терапию препаратом в данной дозе. Однако если не удалось достичь целевого уровня, можно повысить интенсивность ЛПНП-снижающей терапии за счет повышения дозы статина либо путем комбинации статина с секвестрантом желчных кислот или никотиновой кислотой.
Через 12 нед после начала медикаментозной терапии следует опять проверить реакцию на лечение. Если все еще не удалось достичь целевого уровня ХС ЛПНП, можно рассмотреть вопрос о дальнейшем повышении интенсивности фармакотерапии. Если целевого уровня нельзя достичь посредством стандартной ЛПНП-снижающей терапии, рекомендуется направить пациента к специалисту с опытом проведения гиполипидемической терапии. После достижения целевого уровня ХС ЛПНП следует уделить внимание другим липидным и нелипидным факторам риска. После этого можно осуществлять периодический контроль за состоянием здоровья пациентов каждые 4–6 мес, а при необходимости и чаще.
Особые замечания в отношении различных подгрупп пациентов
Мужчины среднего возраста (35–65 лет). В целом у мужчин риск развития ИБС выше, чем у женщин. У мужчин среднего возраста особенно высока распространенность основных факторов риска, они предрасположены к абдоминальному ожирению и развитию метаболического синдрома. Значительная доля всех случаев ИБС приходится на мужчин среднего возраста. В связи с этим у многих мужчин данной возрастной группы высок риск развития ИБС, и тем, у кого уже имеется ИБС, требуется проведение интенсивной ЛПНП-снижающей терапии.
Женщины в возрасте 45–75 лет. У женщин ИБС обычно развивается на 10–15 лет позже по сравнению с мужчинами; поэтому большинство случаев ИБС фиксируют у женщин в возрасте старше 65 лет. Все факторы риска влияют на развитие ИБС у женщин, и большая часть случаев раннего развития ИБС (в возрасте < 65 лет) у них отмечается при на личии множественных факторов риска и метаболического синдрома. Вопреки ранее существовавшему мнению о том, что половые различия в степени риска развития ИБС отражают защитный эффект эстрогенов у женщин, результаты недавно проведенных испытаний по первичной и вторичной профилактике заставили сомневаться в пользе замес тительной гормональной терапии для снижения риска ИБС у женщин в постменопаузальный период. Напротив, благоприятные эффекты терапии статинами у женщин, установленные в результате клинических испытаний, свидетельствуют о предпочтительности применения для снижения риска развития ИБС гипохолестеринемических средств по сравнению с гормонозаместительной терапией. В целях вторичной профилактики лечение женщин проводят так же, как и мужчин. При первичной профилактике общий подход руководства АТР III применим равным образом как к женщинам, так и мужчинам. Однако при принятии клинически обоснованных решений о применении гипохолестеринемических средств следует учитывать более позднее развитие ИБС у женщин.
Лица пожилого возраста (мужчины в возрасте > 65 лет и женщины > 75 лет). В целом большинство новых случаев коронарных ишемических событий и коронарной смерти отмечают у лиц пожилого возраста (>65 лет). Высокий уровень ХС ЛПНП и низкий уровень ХС ЛПВП еще сохраняют прогностическую ценность в отношении развития ИБС у лиц пожилого возраста. Однако выявление прогрессирующего субклинического атеросклероза посредством неинвазивного исследования может оказаться полезным для подтверждения наличия высокого риска ИБС у лиц пожилого возраста. В клинические испытания по применению статинов при вторичной профилактике было включено значительное количество лиц пожилого возраста, преимущественно 65–75 лет. В этих испытаниях доказано существенное снижение риска ИБС у лиц пожилого возраста в результате терапии статинами. Таким образом, по- видимому, нет необходимости в каких-либо жестких возрастных ограничениях при отборе пациентов с наличием ИБС для проведения ЛПНП-снижающей терапии. В целях проведения первичной профилактики у лиц пожилого возраста ЛИОЖ является терапией первой линии. Тем не менее, применение лекарственных средств, снижающих ЛПНП, также возможно в отношении лиц пожилого возраста группы повышенного риска в связи с наличием множественных факторов риска или при прогрессирующем субклиническом атеросклерозе.
Взрослые молодого возраста (мужчины 20–35 лет, женщины 25–45 лет). В данной группе ИБС отмечают редко, за исключением случаев наличия у пациента сильных факторов риска (например семейная гиперхолестеринемия, курение большого количества сигарет или сахарный диабет). Несмотря на то что клиническую форму ИБС выявляют в таком возрасте относительно редко, возможно быстрое прогрессирование коронарного атеросклероза ранних стадий. Частота развития коронарного атеросклероза в более раннем возрасте коррелирует с основными факторами риска. В частности, результаты длительных проспективных исследований свидетельствуют, что повышенный уровень ХС в сыворотке крови у взрослых молодого возраста является прогнозом повышенной частоты раннего развития ИБС в среднем возрасте. Таким образом, выявление факторов риска у взрослых молодого возраста является важной целью, поскольку снижение ХС ЛПНП посредством изменения образа жизни предоставляет возможность замедлить или предотвратить развитие ИБС в более позднем возрасте. Взрослым молодого возраста с уровнем ХС ЛПНП ≥ 130 мг/дл следует назначить ЛИОЖ и акцентировать внимание на важности его значения.
Особого внимания требуют курящие мужчины молодого возраста с высоким уровнем ХС ЛПНП (160–189 мг/дл); они могут являться кандидатами на терапию лекарственными средствами, снижающими ЛПНП. При наличии очень высокого уровня ХС ЛПНП (≥ 190 мг/дл) у взрослых молодого возраста рекомендуется проведение медикаментозной терапии по схеме, используемой при лечении взрослых других возрастных групп. Лицам с тяжелыми генетическими формами гиперхолестеринемии может потребоваться назначение лекарственных средств, снижающих ЛПНП (например статин + секвестрант желчных кислот).
Заключение
В заключение считаем важным привести ряд положений американского руководства организационного характера, многие из которых, безусловно, являются чрезвычайно актуальными и для нашей страны. Так, в отношении соблюдения рекомендаций по ЛПНП- снижающей терапии в АТР III рекомендуется использовать современные многопрофильные методы охвата целевых групп пациентов, врачей и систем оказания медицинской помощи для достижения эффективности рекомендаций руководства по первичной и вторичной профилактике на уровне всего населения страны (табл. 5).
Таблица 5. Вмешательства для улучшения соблюдения рекомендаций
В отношении пациента
- упрощение схем медикаментозного лечения;
- обеспечение пациента исчерпывающими инструкциями и использование надлежащих методов консультирования для обучения пациента правильному соблюдению режима лечения;
- содействие использованию памяток, помогающих пациенту не забывать схему лечения;
- использование методов для улучшения соблюдения режима лечения и для сохранения контактов с пациентом;
- содействие поддержке пациента со стороны родных и близких;
- улучшение и поощрение соблюдения режима лечения;
- повышение частоты посещений для пациентов, не способных достичь целевых уровней;
- улучшение качества и доступности медицинской помощи;
- вовлечение пациентов в процесс лечения путем проведения пациентом самостоятельного мониторинга.
В отношении врача и медицинского учреждения
- обучение врачей мерам по внедрению клинических руководств по гиполипидемической терапии;
- использование памяток, побуждающих врачей уделять внимание гиполипидемической терапии;
- определение в учреждении лица, помогающего своевременному оказанию медицинской помощи пациенту;
- привлечение пациентов для содействия мерам профилактики;
- разработка стандартного плана лечения, позволяющего упорядочить оказание медицинской помощи;
- оценка приобретенного опыта, стимулирующая внесение изменений в оказание медицинской помощи;
- напоминание пациентам о запланированных посещениях врача и отслеживание пропущенных визитов.
В отношении системы оказания медицинской помощи
- ведение пациентов с гиперхолестеринемией в рамках системы специальных амбулаторий по проведению гиполипидемической терапии;
- ведение конкретных пациентов медицинскими сестрами;
- внедрение телемедицины.
Внимание соблюдению рекомендаций необходимо уделять в целях достижения по возможности самой высокой степени снижения риска развития ИБС. Соблюдение рекомендаций как пациентами, так и медицинскими работниками является решающим фактором для приближения к той эффективности лечения, польза от которого была продемонстрирована в клинических испытаниях по гиполипидемической терапии.
Литература
- Бабушкина А.В. (2009) Инфаркт миокарда: от фундаментальных исследований — к практическим достижениям (по материалам X Национального конгресса кардиологов Украины). Укр. мед. часопис, 5(73): 10–13 (http://www.umj.com.ua/archive/73/1506.html; http://www.umj.com.ua/archive/73/pdf/1506_rus.pdf).
- Коваленко В.М. (ред.) (2009) Настанова з кардіології. МОРІОН, Київ, 1368 с.
- Солошенко О. (2009) Когда возможности используются недостаточно, или как убедить врача назначать статины? Укр. мед. часопис, 2(70): 15–17 (http://www.umj.com.ua/rus/archive/70/1413.html; http://www.umj.com.ua/archive/70/pdf/1413_rus.pdf).
- Спасокукоцкий А.Л. (пер. и ред.) (2005) Ведение пациентов с гиперхолестеринемией (реферат руководства). Укр. мед. часопис, 1(45): 5–25 (http://www.umj.com.ua/rus/archive/45/386.html; http://www.umj.com.ua/archive/45/pdf/386_rus.pdf).
- Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (2001) Executive Summary of The Third Report of The National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, And Treatment of High Blood Cholesterol In Adults (Adult Treatment Panel III). JAMA, 285(19): 2486–2497.
- Grundy S.M., Cleeman J.I., Merz C.N. et al.; National Heart, Lung, and Blood Institute; American College of Cardiology Foundation; American Heart Association (2004) Implications of recent clinical trials for the National Cholesterol Education Program Adult Treatment Panel III guidelines. Circulation, 110(2): 227–239 (http://circ.ahajournals.org/cgi/content/full/110/2/227; http://circ.ahajournals.org/cgi/reprint/110/2/227.pdf).
- National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III) (2002) Third Report of the National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III) fnal report. Circulation, 106(25): 3143–3421 (http://circ.ahajournals.org/cgi/reprint/106/25/3143.pdf).
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»



