
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
- Новини 26.10.2021 Аппаратура для УЗИ: применение, принципы работы, разновидности
- Новини 23.10.2021 Интимная пластика после родов: когда необходима операция
Новые подходы в лечении инфекций мочевыводящих путей у детей с использованием препарата Икзим Н.Л. Аряев, Н.Ю. Горностаева, Л.И. Дмитриева
Резюме. Исследовалась эффективность и безопасности препарата «Икзим» для перорального применения у детей различного возраста с инфекциями мочевыводящих путей. Широкий спектр антимикробного действия обуславливает высокую эффективность применения одного курса препарата у детей на стационарном и амбулаторном этапе лечения при отсутствии побочных эффектов у детей с инфекций мочевыводящих путей.
Введение
Проблема инфекций мочевыводящих путей (ИМВП) у детей является актуальной как в Украине, так и за рубежом, что определяется большой распространенностью заболевания, хроническим течением, формированием хронической почечной недостаточности и, следовательно, инвалидности детей [1,6,7].
Согласно данным Министерства здравоохранения Украины, частота ИМВП у детей с 2005 г. возрастает на 4–5% ежегодно и занимает седьмое место в структуре общей заболеваемости детского населения Украины. Согласно данным Американской Академии Педиатрии (1999), ИМВП встречаются в 8,1% случаев у девочек и в 1,9% у мальчиков старше года [6]. У детей первого года жизни ИМВП встречаются в 2,9%, при этом мальчики и девочки болеют одинаково часто [1,4,6,7].
У 40–45% детей ИМВП рецидивирует на протяжении первого года после первого эпизода, в 10–12% случаев переходит в хроническую форму, у 4–5% больных формируется хроническая почечная недостаточность [1,6,7].
Медико-социальный аспект проблемы определяет интерес нефрологов и педиатров в контексте повышения эффективности терапии ИМВП [1–4,7].
Инфекция чаще всего развивается в результате попадания в уретру микроорганизмов, которые содержатся в фекалиях [6–8], после закрепления их на слизистой уретры, восходящим путем инфекция попадает в мочевой пузырь и почки, вызывая их воспаление [8]. Гораздо реже отмечается гематогенный или лимфогенный путь передачи инфекции [6–8].
Учитывая преимущественно восходящий путь инфекции, у детей при острых и хронических ИМВП в этиологии доминирует E. coli (63–67%) и энтерококки (21–23%). Удельный вес других возбудителей (стафилококки, стрептококки, клебсиела, гемофильная палочка, моракселла катаралис) значительно ниже [3,4,6,7]. Следует отметить, что в последние годы значительно возросла роль синегнойной палочки у больных с хроническим вариантом течения ИВМП на фоне инвазивных методов диагностики и лечения [2–5].
В результате целого ряда факторов (широкое и часто нерациональное использование антибиотиков, сложная экологическая ситуация в нашей стране, приводящая к снижению иммунной защиты у детей) привели к изменению этиологической структуры возбудителей, повышению удельного веса микробных ассоциаций, к увеличению количества антибиотикорезистентных штаммов [2,4–6,8]. Поэтому в современных схемах лечения ИМВП важную роль играет правильный выбор антибиотика. Учитывая этиологическую структуру возбудителей ИМВП при острых и при хронических формах, наиболее оптимально требованиям к выбору антибиотика отвечают цефалоспорины III поколения для перорального пути введения [2–6].
Цель исследования заключалась в определении эффективности и безопасности препарата «Икзим» — антибиотика цефалоспоринового ряда III поколения для перорального применения у детей с инфекциями мочевыводящих путей.
Материал и методы исследования
Проведено двуцентровое сравнительное контролируемое исследование в параллельных группах, отобранных методом стратифицированной рандомизации по нозоформам среди 156 пациентов с ИМВП, находящихся на стационарном и амбулаторном лечении в базовых лечебных учреждениях кафедры госпитальной педиатрии и неонатологии Одесского государственного медицинского университета — Одесской областной детской клинической больнице и консультативной поликлинике ООДКБ. Протокол исследования был одобрен региональным комитетом по биоэтике при ОГМУ. Родители включенных в исследование детей получили устную информацию обо всех процедурах исследования и дали информированное согласие на участие в исследовании.
Критерии включения
- возраст от 6 месяцев до 18 лет;
- диагноз острой неосложненной инфекции мочевыводящих путей легкой или средней степени тяжести;
- диагноз обострения хронического пиелонефрита, цистита легкой или средней степени тяжести;
- информированное согласие на участие пациента в исследовании.
Критерии исключения
- дети в возрасте до 6 месяцев;
- острые и хронические инфекции мочевыводящих путей тяжелой степени тяжести;
- язвенная болезнь в стадии обострения;
- острые заболевания печени;
- гиперчувствительность к препарату в анамнезе;
- прием других антибиотиков;
- отказ выполнять основные процедуры исследования и соблюдать режим приема препарата.
Диагноз ИМВП верифицировался на основании анализа клинико-анамнестических данных, результатов параклинических методов исследований: ультразвукового исследования почек и мочевого пузыря, микционной цистографии, внутривенной урографии. Всем больным проводились клинические исследования крови и мочи, пробы мочи по Зимницкому, по Нечипоренко, посев мочи на стерильность, биохимические исследования (общий билирубин и его фракции, АсТ, АлТ, щелочная фосфатаза, тимоловая проба, общий белок, протеинограмма, клиренс-тесты, уровень мочевины и креатинина крови).
Возраст больных находился в пределах от 6 месяцев до 18 лет, среди исследуемых было 116 девочек и 40 мальчиков.
По результатам стратифицированной рандомизации пациенты были разделены на 2 группы. 80 пациентов основной группы в качестве основного антибактериального препарата получали цефалоспорин III поколения для перорального приема «Икзим» (действующее начало — цефиксим) в следующих дозировках: дети от 6 месяцев до 12 лет — по 8 мг на кг массы тела в сутки, дети с 12 лет — по 400 мг в сутки. Контрольная группа включала 76 больных, получавших антибиотики для перорального введения других групп (цефалоспорины II поколения; пенициллины, защищенные клавулановой кислотой; макролиды) в возрастных дозировках. Статистически значимых клинических, возрастных и половых различий между группами не было. Длительность наблюдения в обоих центрах составила 2 недели.
Эффективность лечебного действия препарата оценивали по динамике интоксикационного синдрома (гипертермия, снижение аппетита, головные боли), по динамике болевого синдрома, дизурических проявлений (болезненное и учащенное мочеиспускание), ультразвуковой картины чашечно-лоханочной системы.
Основные симптомы оценивались по выраженности в баллах от 0 до 3 с применением аналоговой шкалы, в соответствии с которой 0 баллов — симптомов нет, 1 балл — симптом слабо выражен, 2 балла — симптом умеренно выражен, 3 балла — симптом резко выражен. Оценка проводилась до начала лечения, на 3, 7 и 14 дни терапии. После окончания исследования производили субъективную оценку клинического эффекта препарата по шкале: эффективный, малоэффективный, неэффективный. Безопасность и переносимость препарата оценивались по наличию или отсутствию ожидаемых побочных действий, включая диарею, аллергические реакции, случаи индивидуальной непереносимости, изменение параклинических показателей (лейкопения, эозинофилия, лимфоцитоз, увеличение активности трансаминаз, креатинина).
Статистическая обработка полученных данных выполнена с использованием стандартных пакетов программ Microsoft Excel.
Результаты исследования и их обсуждение
Инфекция мочевыводящих путей легкой и средней степени тяжести диагностирована у всех больных. В соответствии с нозологическими формами ИМВП распределились следующим образом (рис.1).
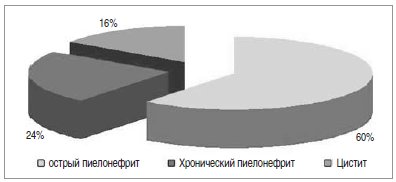
Рис. 1. Структура распределения инфекции мочевыводящих путей по нозоформам у наблюдаемых больных
До начала лечения у всех больных (100%) отмечались абдоминальные разлитые боли различной интенсивности, у 22% пациентов (дети старше 10 лет) на фоне абдоминального болевого синдрома отмечались боли в пояснице. Боли были в основном умеренной интенсивности, усиливающиеся после незначительной физической нагрузки.
На дизурические проявления указывали 95 (68,8%) больных: учащенное мочеиспускание — 59 (42,6%) пациентов, болезненное мочеиспускание — 36 (26,2%). Снижение аппетита наблюдалось у 135 (86,7%) больных. При клиническом обследовании детей с ИМВП пальпаторно отмечена болезненность в области мочевого пузыря у 50 больных (32%), перкуторно — боли в области проекции почек (положительный симптом Пастернацкого) у 87 (56%) детей.
У 134 (86%) пациентов имелась гипертермия выше 38,5° С.
У 100% больных в общем анализе крови был отмечен лейкоцитоз со сдвигом формулы влево, ускоренное СОЭ, в общем анализе мочи отмечалась лейкоцитурия, бактериурия. Протеинурию имели 94 (60%) человека. В анализе мочи по Нечипоренко у всех (100%) пациентов имелась лейкоцитурия. Изменений в остальных параклинических показателях у наблюдаемых нами детей с ИМВП не установлено.
При проведении УЗИ почек у 153 детей с ИМВП (98%) было выявлено расширение размеров чашечно-лоханочной системы обеих почек. На фоне приема препарата «Икзим» у детей с инфекциями мочевыводящих путей по сравнению с контрольной группой отмечена более быстрая положительная динамика в виде регресса болевого синдрома (на 5–7 день от начала лечения) и купирования дизурических проявлений (на 6–7 день от начала лечения) (рис. 2,3).
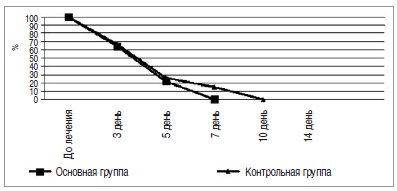
Рис. 2. Динамика болевого синдрома
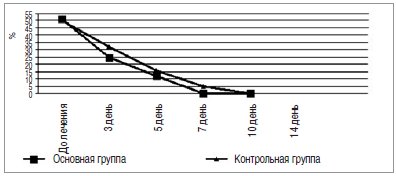
Рис. 3. Динамика дизурического синдрома
У всех пациентов прием антибиотика «Икзим» способствовал более быстрому регрессу интоксикационного синдрома: нормализации температуры на 2–3 день от начала лечения, восстановлению аппетита на 4–5 день от начала лечения, исчезновению головных болей, улучшению самочувствия пациентов (рис.4).
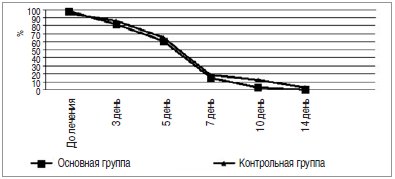
Рис. 4. Динамика интоксикационного синдрома
У детей основной группы, принимавших препарат «Икзим», отмечена более быстрая нормализации показателей общего анализа мочи (на 9–10 день от начала лечения), восстановление показателей общего анализа крови (на 6–8 день от начала лечения), восстановление размеров чашечно-лоханочной системы по данным УЗИ органов брюшной полости (на 10–14 день от начала лечения) (рис.5,6).
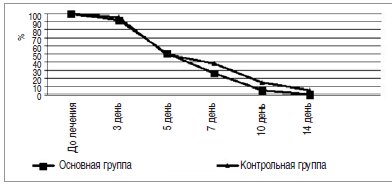
Рис. 5. Динамика лабораторных показателей
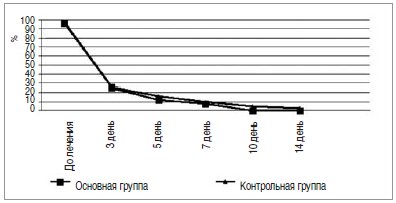
Рис. 6. Динамика уменьшения размеров чашечно-лоханочной системы
Степень выраженности основных симптомов заболевания (болевой, дизурический, интоксикационный) оценивались в баллах от 0 до 3 в соответствии с аналоговой шкалой. Динамика их изменений в результате лечения в основной и контрольной группах детей с ИМВП проводились на 3, 7 и 14-й день лечения. Результаты представлены на рисунках 7,8,9.
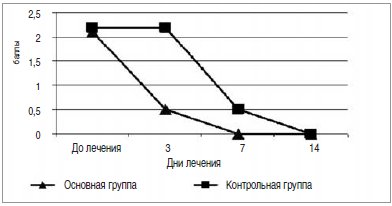
Рис. 7. Динамика болевого синдрома на фоне лечения препаратом «Икзим»
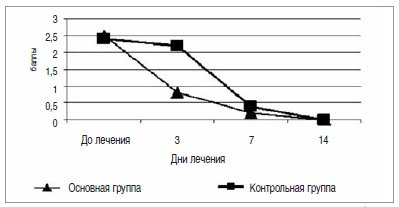
Рис. 8. Динамика дизурических проявлений у детей на фоне лечения препаратом «Икзим»
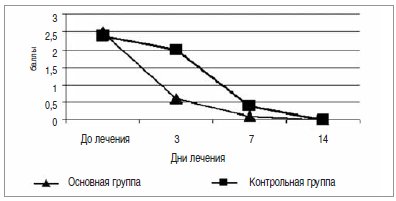
Рис. 9. Динамика интоксикационного синдрома у детей на фоне лечения препаратом «Икзим»
В результате проведенного лечения у 100% детей основной и у 94% контрольной группы была получена клинико-параклиническая ремиссия заболевания в течение 10–14 дней.
Лабораторные показатели функционального состояния печени и почек после проведенного лечения у всех больных (100%) были в пределах нормы.
В ходе мониторинга нежелательных явлений побочное действие препарата в виде аллергических реакций, случаев индивидуальной непереносимости, диареи не зафиксировано. Препарат «Икзим» хорошо переносился детьми, отказов детей от приема препарата не было.
Выводы
- Прием антибактериального препарата цефалоспоринового ряда III поколения «Икзим» способствует выраженной положительной динамике клинических проявлений инфекций мочевыводящих путей у детей за счет купирования дизурического, интоксикационного и болевого синдромов.
- Препарат «Икзим» имеет широкий спектр антимикробного действия, что обуславливает высокую эффективность применения одного курса препарата «Икзим» при отсутствии побочных эффектов у детей с инфекций мочевыводящих путей.
- Препарат «Икзим» отличается хорошей индивидуальной переносимостью, отсутствием побочных реакций.
- Удобная форма выпуска (суспензия), хорошие органолептические свойства, возможность однократного приема в течение суток позволяют снизить психотравмирующий эффект от терапии и достигнуть лучшего комплаенса.
- Антибактериальный препарат «Икзим» является высокоэффективным и безопасным средством патогенетической терапии инфекций мочевыводящих путей у детей на стационарном и амбулаторном этапе лечения.
Литература
- Екосистема великого промислового міста України та діти першого року життя / О. М. Лук'янова, Ю. Г. Резніченко, Ю. Г. Антипкін та ін.]. — Запоріжжя, 2005. — 222 с.
- Няньковський С. Л. Ефективність і безпечність пероральної антибіотико терапії при інфекції сечовивідних шляхів у детей / С. Л. Няньковський, С.В. Герасимов // Совр. педиатрия. — 2007. — № 2 (15). — С. 101—105.
- Самсыгина Г. М. Цефалоспорины в педиатрии / Г.М. Самсыгина // В мире лекарств. — 2000. — № 1. — С. 18—21
- Эффективность применения «Икзима» при лечении обострений рецидивирующих бронхитов в сочетании с воспалительными заболеваниями ЛОР-органов у детей / Ю. Г. Резниченко, Т. И. Окул, В. Г. Малюга [и др.] // Совр. педиатрия. — 2007. — №2(15). — С. 42–44.
- Яковлев С. В. Современное значение цефалоспориновых антибиотиков при лечении инфекций в стационаре / С. В. Яковлев // Антибиотики и химиотерапия. —2001. — Т. 46. — № 9. — С. 4—11.
- American academy of pediatrics, Committee on quality improvement, Subcommittee urinary tract infection: Practice parameter: The diagnosis, treatment, and evaluation of the initial urinary tract infection in febrile infants and young children // Pediatrics. — 1999. — Vol. 103 — P. 843—852.
- Epidemiology of symptomatic urinary tract infection in childhood / J. Winberg, H. J. Andersen, T. Bergstrom [et al.] // Acta Paediatr Scand. — 1974. — Suppl. 252. — P. 1—20.
- Untreated asymptomatic bacteriuria in girls: Effect of phenoxymethylpenicillinand erythromycin givenfor intercurrent infections / S. Hansson, U. Jodal, K. Lincoln [et al.] // BMJ. — 1989. — Vol. 298. — P. 856—859.
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


