
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»
Лікарська практика
Нове на порталі
- Новини 07.11.2023 Мезотерапія - що це за процедура, особливості проведення і коли потрібна?
- Новини 31.07.2023 Безопераційні методики корекції нижнього повіка
- Новини 31.05.2023 Лечение метастазов в печени на поздних стадиях рака
- Новини 16.05.2023 Лікувальна фізкультура та профілактика варикозу
- Новини 23.03.2023 Що не можна робити онкологічним хворим
- Новини 05.12.2022 Лазерна корекція зору: лікар клініки “Новий Зір” розвінчує необґрунтовані страхи
- Новини 15.07.2022 Лечение синдрома вагинальной релаксации
- Новини 24.11.2021 Нашего малыша принес не аист: женщина поделилась опытом ЭКО
- Новини 26.10.2021 Аппаратура для УЗИ: применение, принципы работы, разновидности
- Новини 23.10.2021 Интимная пластика после родов: когда необходима операция
Биоактивные компоненты растений и лечение климактерического синдрома

Для оценки эффективности, переносимости и безопасности изофлавоноидов сои для лечения вазомоторных и эмоционально-вегетативных проявлений климактерического синдрома (КС) с изучением влияния изофлавонов на липидный спектр крови было проведено исследование, в ходе которого препарат, содержащий 40 мг изофлавонов сои, назначили 2 раза в день в течение 3 месяцев 40 женщинам с КС.
Из лекарственных растений, применяемых в традиционной медицине на протяжении длительного времени, выделено большое количество активных веществ. Это послужило поводом для их активного изучения, а также промышленного производства синтетических аналогов биологически активных компонентов растений. Широко известными и распространенными примерами природных биологически активных веществ являются сердечные гликозиды, хинин, винкристин, атропин, кокаин, эрготамин и целый ряд других лекарственных препаратов, которые имеют растительное происхождение.
Углубленное изучение механизма действия различных растений и их компонентов, влияния этих веществ на различные ткани, органы и системы, исследование эффективности и безопасности при лечении патологических процессов проводятся во многих научных учреждениях мира, что значительно повышает уровень достоверности результатов фитомедицины.
Основными активными составляющими растительных препаратов являются органическиевещества: углеводы (крахмал, сахара), безазотистые основания (гликозиды, лигнин, целлюлоза, эфирные масла, танины), азотсодержащие соединения (аминокислоты, амины, холин, пурины, алкалоиды), микроэлементы (железо, кальций, магний, калий, натрий, марганец, силиций, хлор) и другие вещества.
В настоящее время значительный интерес для медицины представляют флавоноиды – естественные полифенольные бензогаммапироновые компоненты, которые входят в состав многих растений [11, 22, 37, 39]. Играя важную роль в биологических процессах растений, они отвечают за яркую окраску цветов и фруктов [12, 20],регулируют процессы размножения [40] и роста растений, входят в состав УФ-фильтров [20].
Благоприятное влияние богатых флавоноидами продуктов на здоровье человека было известно значительно раньше, чем эти соединения были выделены как активные составляющие растений [33]. Дополнительным импульсом к исследованию флавоноидов послужило открытие в начале 90-х годов прошлого века французского парадокса: у жителей Средиземноморья, употребляющих большое количество жирной пищи, которая способна вызывать раннее развитие сердечной патологии, наблюдается низкая смертность от сердечно-сосудистых заболеваний, что связывается с традиционно высоким потреблением красного вина [13, 16, 35].
По данным разных авторов, из растений выделено от 4000 до 5000 и даже 8000 видов флавоноидов, которые в зависимости от структуры подразделяются на 10–13 классов [7, 21, 24, 38].Различия в строении гетероциклического кольца С в структуре полифенолов дают начало классам флавонолов, флавонов, катехинов, флаванонов, антоцианов и изофлавонов, которые считаются основными [33].
В многочисленных экспериментальных исследованиях было показано, что флавоноиды могут как ингибировать, так и стимулировать большое количество ферментных систем, включенных в важнейшие пути регулирования пролиферации и деления клеток, гормональную функцию,детоксикацию и воспалительный ответ. Выявлено и продолжает изучаться антиоксидантное, антиканцерогенное действие флавоноидов, а также их влияние на иммунную систему [30]. Установлено, что флавоноиды способны тормозить развитие, а также уничтожать многие бактериальные штаммы, ингибировать вирусные ферменты, например обратную транскриптазу и протеазу, способны вызывать повреждение некоторых патогенных простейших. При этом токсическое действие флавоноидов на клетки человека является незначительным [20].
Флавоноиды, выделенные из соевых бобов, красного клевера, орехов, зерен и некоторых другихрастений, относят к группе фитоэстрогенов в связи со структурным сходством их молекул с молекулой эстрадиола. Выделено несколько классов фитоэстрогенов, основными из которых считаются изофлавоны (большое количество их найдено в сое, красном клевере, цимицифуге), лигнаны (обнаружены в наружном слое зерен пшеницы, ржи и риса, семенах льна, в орехах, в некоторых ягодах, фруктах и овощах) и куместаны (содержатся в соевых бобах, люцерне). Наиболее перспективными в связи с высоким содержанием флавоноидов являются соевые бобы. В 1 г соевого белка содержится до 1–2 мг изофлавоноидов, из которых примерно 60% генистеина, 30% даидзенина и 10% других изофлавонов.
Первоначальный интерес к соевым бобам был связан с тем, что добавление сои в корм животным приводило к значительному увеличению их массы, что предположительно было связано с эстрогенным действием активных компонентов бобов [6]. Y. Folman и соавт. в экспериментальных моделях на мышах было подтверждено, что выделенные из сои изофлавоноиды обладают слабой эстрогенной активностью [18]. S.I. Mäkela и соавт. установили, что данные соединения оказывают двоякое биологическое действие: антиэстрогенное – при повышенном исходном уровне эстрогенов, например у женщин в перименопаузе, и проэстрогенное при низком уровне гормонов, например в постменопаузе [28].Эстрогеновый эффект этих соединений объясняется несколькими биологическими механизмами их действия: они связываются с эстрогеновыми рецепторами (ER), преимущественно ER-β [3, 15, 26], а также оказывают влияние на гипоталамо-гипофизарно-яичниковую систему, приводя к изменению секреции гормонов. В целом их действие сравнимо с эффектами селективных модуляторов эстрогеновых рецепторов [17], в связи с чем изофлавоноиды нашли применение в лечении КС.
Обладая слабой эстрогенной и антиэстрогенной активностью, изофлавоноиды связываются с эстрогеновыми рецепторами, которые являются потенциальными медиаторами, влияющими на возникновение горячих приливов в условиях дефицита эстрогенов [31]. Кроме того, изофлавоноиды сои обладают антиоксидантной активностью, а также способны ингибировать рост опухолевых клеток вследствие антоангиогенной и антипролиферативной активности [41], они, в частности, оказывают протективное действие в отношении рака молочной железы [10]. В экспериментальных условиях было выявлено, что протективное действие в отношении рака молочной железы может появляться даже в том случае, если соевые продукты и препараты принимали в препубертатном возрасте [27]. S. M. Potter и соавт. [34], Y. M. Chenи соавт. [9] установили положительное влияние изофлавонов на костную ткань. Так, употребление 40 мг соевого белка в сутки на протяжении 6 мес приводит к достоверному повышению минеральной плотности костной ткани у женщин в постменопаузе.
Кардиопротективный эффект этих соединений связан с положительным действием на липидный профиль крови [18, 29]. Прием изофлавоноидов способствует снижению артериального давления [36], положительно влияет на эндотелиальную функцию, настроение [8], массу тела и индекс массы тела [5]. Кроме того, согласно результатам SOPHIA-исследования, изофлавоноиды значительно улучшают вербальную память [25], а также способствуют предотвращению старения кожи [4] .
Поэтому обоснованным является то, что во многих странах Европы и в США в последние годы значительно увеличилось число женщин, применяющих препараты на растительной основе, в частности, содержащие изофлавоноиды сои, для профилактики и лечения различных, в том числе гинекологических, заболеваний: климактерического и предменструального синдромов, гиперпролактинемии и других патологических состояний. Такие препараты являются альтернативой медикаментозному лечению.
Хотя изофлавоны сои наиболее часто применяется для облегчения симптомов менопаузы, данные клинических исследований не позволяют сделать однозначного вывода об их эффективности при лечении КС. Сравнительный анализ многочисленных результатов затруднен в связи с тем, что в исследованиях препараты сои назначались по различным схемам, в разных лечебных дозах, при различной длительности и форме приема [23, 32].
Нами проведена оценка препарата, содержащего 40 мг изофлавонов сои, для лечения женщин с вазомоторными и эмоционально-вегетативными проявлениями КС.
Цель исследования
Цель исследования – провести оценку эффективности, переносимости и безопасности изофлавонов сои (иноклим) для лечения вазомоторных и эмоционально-вегетативных проявлений КС с изучением влияния изофлавонов на липидный спектр крови.
Материал и методы исследования
Исследование было проспективным, открытым, несравнительным. Под наблюдением находились 40 пациенток с КС, обратившихся в научно-поликлиническое отделение ФГУ Научный центр акушерства, гинекологии и перинатологии им. академика В.И.Кулакова. Возраст включенных в исследование женщин колебался от 45 до 56 лет, средний возраст составил 51,8±1,3 года.
Пациентки находились под наблюдением 4 мес, в течение которых ежедневно заполняли дневники. Визиты к врачу осуществлялись за 1 мес и непосредственно перед началом лечения, через 4, 8 и 12 нед лечения. Все изменения состояния за время наблюдения фиксировались в дневниках и медицинских документах, все неблагоприятные явления расценивались как осложнения или побочные эффекты и также заносились в дневник. Контроль за пациентками осуществлялся путем телефонных контактов, а также во время заключительного визита после окончания лечения.
В период набора с целью определения соответствия пациенток критериям включения/исключения все женщины прошли обследование, которое включало тщательный сбор анамнеза для оценки общего состояния здоровья и перенесенных заболеваний, общий осмотр, измерение артериального давления и пульса, гинекологическое, цитологическое, гормональное, клиническое обследование, ультразвуковое исследование органов малого таза и молочных желез. Клинически значимые отклонения от возрастных нормативных показателей не выявлены. По результатам биохимического исследования выявлены изменения липидного спектра крови, которые проявлялись в повышении уровня общего холестерина (ХС), ХС липопротеиновХС липопротеинов высокой плотности (ЛПВП) в сыворотке крови. Коэффициент атерогенности до лечения составил 3,07±1,42.
В исследование были включены пациентки, которые соответствовали следующим критериям: возраст 45 лет и старше, наличие более 7 приливов в день и признаков КС при отсутствии менструаций по меньшей мере в течение 2 лет; без серьезной соматической патологии; получившие полную информацию о целях исследования и используемых препаратах.
Критерии исключения из исследования: прием в течение предыдущих 6 мес гормональных препаратов, нейролептиков и антидепрессантов, ингибиторов обратного захвата серотонина; любое психиатрическое лечение; наличие эндокринных заболеваний (сахарный диабет, гипо- или гипертиреоз, опухоль гипофиза); тяжелых хронических заболеваний; эндометриоза, миомы матки с узлами более 3 см в диаметре, патологии или подозрения на патологию эндометрия; заболеваний молочных желез; предшествующее началу исследования хирургическое лечение, любое лечение КС в период набора.
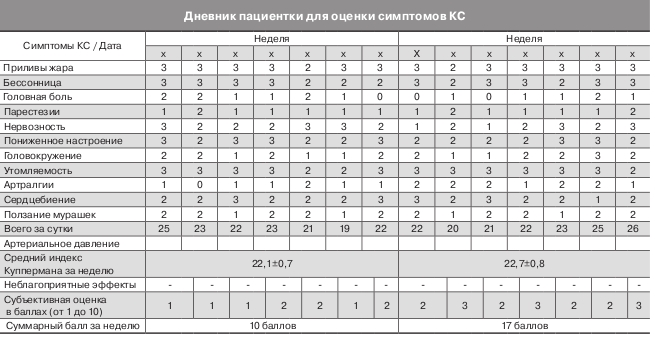
В процессе наблюдения все пациентки заполняли дневники (см. рисунок) для оценки тяжести КС и эффективности препаратов через 4, 8 и 12 нед лечения в сравнении с соответствующими исходными показателями, отмечали возникшие побочные реакции и проводили оценку эффективности препарата по субъективным ощущениям.
Эффективность лечения определялась по изменению индекса Куппермана, частоты горячих приливов и улучшению самочувствия больных, положительному влиянию на липидный спектр крови.
Для определения тяжести КС суммировались результаты 11 симптомов, указанных в дневнике, в баллах за неделю до лечения, показатели 4, 8 и 12-й недель лечения. Средний суммарный показатель этих 7 дней, рассчитанный до начала лечения и на 12-й неделе приема препаратов, был взят для сравнения и оценки результатов лечения. Кроме того, проводился анализ субъективной оценки эффективности, приемлемости препарата и его безопасности. Всем пациенткам, включенным в исследование, был назначен препарат, содержащий 40 мг/сут изофлавонов сои, по 2 таблетки в день, при этом лечение проводилось на фоне гипохолестериновой диеты. Длительность лечения составила 3 мес.
Результаты исследования и обсуждение
В период набора для предварительного определения соответствия критериям включения/исключения были опрошены 54 пациентки, из которых 9 женщин не вошли в исследование в связи с несоответствием критериям включения/исключения и 4 пациентки отказались от лечения по разным причинам. Из анамнеза выяснено, что 11 женщин страдали гипертонической болезнью с эпизодическим повышением артериального давления до 185/110 мм рт. ст., 14 женщин – хроническим гастритом в стадии ремиссии, 8 – хроническим холециститом в стадии ремиссии, у 4 женщин анамнез был отягощен мочекаменной болезнью и у 5 – хроническим пиелонефритом. На болезни органов дыхания (пневмония, бронхит, бронхиальная астма), перенесенные ранее, указывали 2 женщины, на стенокардию – 1, на аллергические реакции в виде крапивницы и кожные заболевания (нейродермит, псориаз) – 2 женщины Оперативные вмешательства (тонзиллэктомия, аппендэктомия, холецистэктомия) былиу 11 женщин (табл.1).
Уровень систолического артериального давления у обследованных пациенток до лечения колебался от 120 до 185 мм рт.ст., диастолического артериального давления — от 80 до 110 мм рт.ст., при этом средний уровень артериального давления был 155/100±8,2/5,9 мм рт. ст. Уровни гормонов были в пределах возрастной нормы: фолликулостимулирующийгормон (ФСГ) 85,05±17,6 МЕ/л, эстрадиол 28,3±8,7 пмоль/л. Цитологические мазки по Папаниколау соответствовали I, II типу. По данным ультразвукового исследования (с применением вагинального датчика), толщина эндометрия у женщин с интактной маткой в среднем составляла 0,34±0,08 см (от 1 до 5 мм), что соответствовалонорме. Повторное ультразвуковое исследование органов малого таза проводилось после лечения.
| Перенесенные ранее болезни | Число женщин (n=40) | |
| n | % | |
| Гипертоническая болезнь | 11 | 27,5 |
| Хронический гастрит в стадии ремиссии | 14 | 35,0 |
| Хронический холецистит в стадии ремиссии | 8 | 20,0 |
| Оперативные вмешательства | 11 | 27,5 |
| Хронический пиелонефрит в стадии ремиссии | 5 | 12,5 |
| Мочекаменная болезнь | 4 | 10 |
| Болезни органов дыхания | 2 | 5,0 |
| Стенокардия напряжения | 1 | 2,5 |
| Аллергические реакции | 1 | 2,5 |
| Кожные болезни | 2 | 5,0 |
| Количество приливов в день | До лечения | Через 4 нед | Через 8 нед | Через 12 нед | ||||
| абс. | % | абс. | % | абс. | % | абс. | % | |
| 15‒20 | 13 | 32,5 | 11 | 27,5 | 3 | 7,5* | 2 | 5,0* |
| 10‒15 | 18 | 45,0 | 14 | 35,0 | 10 | 25,0 | 6 | 15,0* |
| 7‒10 | 9 | 22,5 | 12 | 30,0 | 11 | 27,5 | 7 | 17,5 |
| Отсутствуют или слабые | – | – | 3 | 7,5 | 16 | 40,0* | 25 | 62,5* |
* Статистически значимые различия по сравнению с исходными данными (р<0,05).
| Нарушение сна | Число женщин ( n=40) | |||
| до лечения | после лечения | |||
| абс. | % | абс. | % | |
| Выраженное | 14 | 35,0 | 2 | 5,0* |
| Умеренное | 13 | 32,5 | 9 | 22,5 |
| Всего | 27 | 67,5 | 11 | 27,5* |
Индекс Куппермана, представленный как средний суммарный за 7 дней, предшествовавших началу лечения, составил 23,2±0,3 балла.
При анализе жалоб наиболее частыми проявлениями КС были вазомоторные (приливы, потливость, головная боль и др.) и эмоциональновегетативные (раздражительность, повышенная утомляемость, снижение трудоспособности). Эти проявления КС наблюдались у всех 40 женщин. Обменно-эндокринные нарушения (повышение массы тела) выявлены у 13 (32,5%) женщин, при этом ИМТ составил 24,9±1,7 кг/м2. На расстройство функции кишечника (запоры) и дизурические расстройства жаловались 5 (12,5%) пациенток.
Эффективность иноклима оценивалась по следующим критериям: исчезновение или значительное уменьшение интенсивности симптомов КС, уменьшение коэффициента атерогенности, улучшение самочувствия на основе субъективной оценки пациенток; безопасность – по наличию неблагоприятных и побочных эффектов. При обращении пациентки жаловались в основном на горячие приливы, нарушение сна, слабость, чувство тревоги. Перед началом лечения у 13 (32,5%) женщин приливы возникали более 15 раз в сутки, у 18 (45 %) – 10–15 раз в сутки, у 9 (22,5%) пациенток – 7–10 раз в сутки (табл. 2).
Через 4 нед от начала терапии у 21 (52,5%) женщины на фоне применения изофлавонов сои улучшилось самочувствие, у 3 (7,5%) женщин исчезли жалобы на наличие горячих приливов или приливы были слабыми, не нарушающими общего самочувствия. 16 (40%) пациенток через 4 нед лечения по результатам анализа дневников не отметили значительного улучшения самочувствия, однако указали на уменьшение интенсивности приливов, особенно по ночам, и в связи с этим на улучшение сна. Через 8 нед умеренные приливы до 15 раз в сутки отмечались у 10 (25%) пациенток, реже 10 раз – у 11 (27,5%) пациенток. Приливы практически полностью исчезли у 16 (40%) женщин. К окончанию срока наблюдения (через 12 нед) у 6 (15%) женщин оставались умеренные приливы, которые возникали до 10—15 раз в сутки, у 7 (17,5%) – приливыдо 10 раз в день. Двух женщин продолжали беспокоить частые приливы, плохой сон, раздражительность, которые значительно нарушали общее состояние. К окончанию лечения 25 (62,5%) пациенток практически перестали жаловаться на горячие приливы ( см. табл. 2).
До лечения значительное нарушение сна различной степени выраженности отмечались у 27 женщин, что, как правило, было связано с возникающими по ночам горячими приливами, повышенной потливостью. При этом 14 (35%) пациенток жаловались на очень плохой, поверхностный сон с частыми пробуждениями; умеренное нарушение сна было у 13 (32,5%) женщин. К концу курса лечения только 9 (22,5%) пациенток жаловались на нарушения сна умеренной тяжести, у 2 женщин оставались значительные проблемы со сном (табл. 3).
Плохой сон, недосыпания, частые приливы были причиной повышенной усталости, слабости, снижения работоспособности у 31 (77,5%) женщины, при этом 8 (20%) женщин характеризовали это состояние как сильную слабость, приводящую к значительному снижению работоспособности, 9 (32,1%) – как постоянную и 14 (35%) – как умеренную слабость. К концу курса лечения 6 (15%) женщин указывали а наличие умеренной слабости, 34 (85%) женщины чувствовали себя удовлетворительно (табл. 4).
При оценке действия иноклима через 3 мес 85% женщин дали ему положительную оценку, отметили значительное улучшение самочувствия, уменьшение интенсивности различных симптомов КС: уменьшение частоты и выраженности горячих приливов у 62,5%, нарушений сна у 40% пациенток, что привело к повышению трудоспособности у 85% наблюдаемых. Причем действие Иноклима стало проявляться с 3–4-й недели лечения. Индекс Куппермана через 12 нед составил 17,9±1,2.
| Снижение работоспособности | Число женщин (n=40) | |||
| до лечения | после лечения | |||
| абс. | % | абс. | % | |
| Значительное | 8 | 20,0 | 0 | 0* |
| Постоянное | 9 | 32,1 | 6 | 15,0 |
| Умеренное | 14 | 35,0 | 11 | 27,5 |
| Всего | 31 | 77,5 | 17 | 42,5* |
* Статистически значимые различия по сравнению с исходными данными (р<0,05).
Неблагоприятное влияние дефицита эстрогенов в период менопаузы проявляется в возникновении гипертензии, кардиоваскулярной патологии, развитии остеопороза и других нарушений, при лечении которых заместительная гормональная терапия (ЗГТ) дает быстрый клинический эффект. Опубликованные результаты исследований свидетельствуют о ряде серьезных побочных эффектов при проведении ЗГТ, что сужает перечень показаний к назначению гормональной терапии и расширяет возможности применения нетрадиционной терапии.
Изофлавоны могут быть альтернативой ЗГТ при лечении дислипидемии, их положительное действие на липидный спектр крови подтверждено в исследованиях некоторых авторов [13, 32].
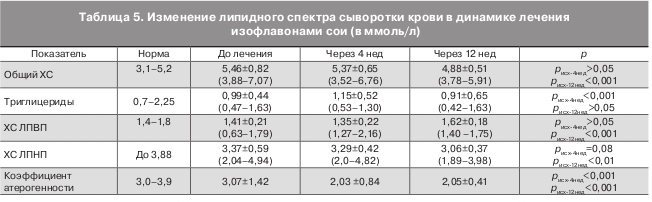
Нами проведено исследование липидного спектра крови в динамике лечения изофлавонами сои через 4 и 12 нед. Анализ результатов биохимического исследования показал, что у 14 (35%) женщин до лечения уровень общегоХС был выше нормы (>5,46 ммоль/л), у 8 (20%) женщин показатель находился на верхней границе нормы. Повышенный уровень ХС ЛПНП был у 9 (22,5%), у 6 (15%) женщин уровень ХС ЛПНП был на верхней границе нормы. До лечения уровень ХС ЛПВП был ниже возрастной нормы у 6 (15%) женщин. Коэффициент атерогенностидо лечения в среднем составил 3,07±1,42 (табл. 5).
После лечения выявлены положительные изменения липидного спектра крови, которые проявлялись в снижении атерогенного потенциала: средний уровень общего ХС снизился с 5,46±0,82 до 4,88±0,51 ммоль/л, при этом превышения уровня ХС выше возрастной нормы не выявлено ни у одной женщины. Уровень ХС ЛПНП снизился с 3,37+0,59 до 3,06±0,37 ммоль/л. После 12 нед лечения незначительно повысился уровень ХС ЛПВП – с 1,41±0,21 до 1,62±0,18 ммоль/л.Коэффициент атерогенности после лечения составил 2,05±0,41 (см. табл. 5).
Безопасность препарата оценивалась по отсутствию его отрицательного воздействия на эндометрий, молочные железы. По результатам ультразвукового исследования до начала лечения толщина эндометрия составила в среднем 0,34±0,08 см (от 1 до 5 мм). При повторном ультразвуковом исследовании, проведенном сразу после окончания лечения, не установлено достоверного изменения данного показателя, толщина эндометрия составила 0,32±0,03 см (p>0,05). Не выявлено изменения структуры молочных желез по данным ультразвукового исследования в динамике лечения. При наблюдении во время лечения отмечена тенденция к стабилизации артериального давления, при этом уровни артериального давления в течение 8–12-й недели лечения не превышали 150/100 мм рт.ст. при исходном уровне 155/100 мм рт.ст.
Переносимость и безопасность препарата определяли по результатам оценки графы побочной симптоматики, которую заполняли пациентки в дневниках в течение 4 мес и которая включала описание нежелательных явлений, дату их начала, продолжительность, возможную связь с исследуемым препаратом, степень тяжести.
Побочные реакции при применении препаратов наблюдались у 2 (5%) пациенток. У одной из них отмечалась тошнота и у одной – кожный зуд, которые были расценены как незначительные, сами женщины с высокой степенью вероятности связывали возникновение данных проявлений с приемом препарата. Во время лечения у 3 пациенток на протяжении 3–5 дней были отмечены явления ОРЗ. Указанные проявления были расценены как незначительные неблагоприятные и не были связаны с приемом препаратов.
Ни одна пациентка не прекратила досрочно лечение.
Таким образом, лечение КС является одним из наиболее обсуждаемых вопросов современной гинекологии. Это вызвано тем, что получившие широкое применение гормональные препараты, которые остаются основным методом лечения вазомоторных симптомов в пери- и постменопаузе [1, 2], с одной стороны, дают быстрый клинический эффект при лечении различных проявлений КС, с другой – не оправдали надежд при профилактике некоторых, в частности сосудистых, заболеваний у женщин в пери- и постменопаузе, а при их применении был выявлен ряд неблагоприятных эффектов.
Проведенное исследование по оценке эффективности и безопасности изофлавонов сои при лечении КС показало, что на фоне лечения с высокой степенью достоверности (р<0,005) улучшается общее состояние пациенток, снижается выраженность психоэмоциональных и вегетососудистых расстройств. Полученные результаты согласуются с данными зарубежных исследователей, изучавших влияние изофлавонов на течение КС [24]. Исследование липидного спектра крови показало положительное действие флавоноидов на уровень ХС, ХС ЛПВП и ХС ЛПНП, а также коэффициент атерогенности, что является важным фактором в профилактике сердечно-сосудистых осложнений у женщин в постменопаузе. При изучении безопасности препарата установлено, что его пероральный прием редко сопровождается неблагоприятными и побочными явлениями. Важный результат исследования – отсутствие значительного влияния фитоэстрогенов на эндометрий и изменений его толщины по результатам ультразвукового исследования. Полученные результаты согласуются с данными зарубежных и российских ученых, изучавших влияние изофлавонов на течение КС.
Таким образом, флавоноиды являются важной группой препаратов для лечения и предотвращения ряда заболеваний, вызванных эстрогеновым дефицитом. Кроме того, изофлавоны способны оказывать ингибирующее действие на ангиогенез, канцерогенез и другие пролиферативные процессы. Хотя действие флавоноидов не является специфичным, а механизм действия является комплексным, эти натуральные компоненты имеют ряд преимуществ перед синтетическими, в том числе гормональными, препаратами.
Во-первых, их можно включать в ежедневную диету. Во-вторых, они хорошо усваиваются не только в виде лекарственного препарата или биологически активной добавки, но и в качестве продукта питания. В-третьих, их употребление редко дает побочные эффекты; в-четвертых, они могут быть идеальными агентами для длительного применения в профилактике поздних проявлений КС. По нашему мнению, целесообразно дальнейшее изучение этой важной группы лекарственных средств.
А. В. Ледина, В.Н. Прилепская
ФГУ Научный центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова Минздравсоцразвития России, Москва
Правова інформація: htts://medstrana.com.ua/page/lawinfo/
«Информация для медицинских работников / первый живой профессиональный портал для практикующих врачей»


